Clear Sky Science · fr
Développement et validation d’un radiotraceur PET activable rapportant l’activité extracellulaire de la myéloperoxydase pour la détection de la plaque athéroscléreuse instable
Pourquoi c’est important pour la santé cardiaque
La plupart des crises cardiaques et des AVC ne sont pas déclenchés par les obstructions artérielles les plus larges, mais par de petits foyers fragiles d’accumulation lipidique qui se déchirent ou s’érodent soudainement. Les médecins ont aujourd’hui du mal à identifier quelles plaques sont sur le point de poser problème. Cette étude présente un nouvel agent d’imagerie pour la TEP conçu pour s’allumer uniquement dans ces plaques « dangereuses » pilotées par une enzyme inflammatoire particulière, aidant potentiellement les cliniciens à repérer les zones artérielles à haut risque avant qu’elles ne provoquent une urgence.
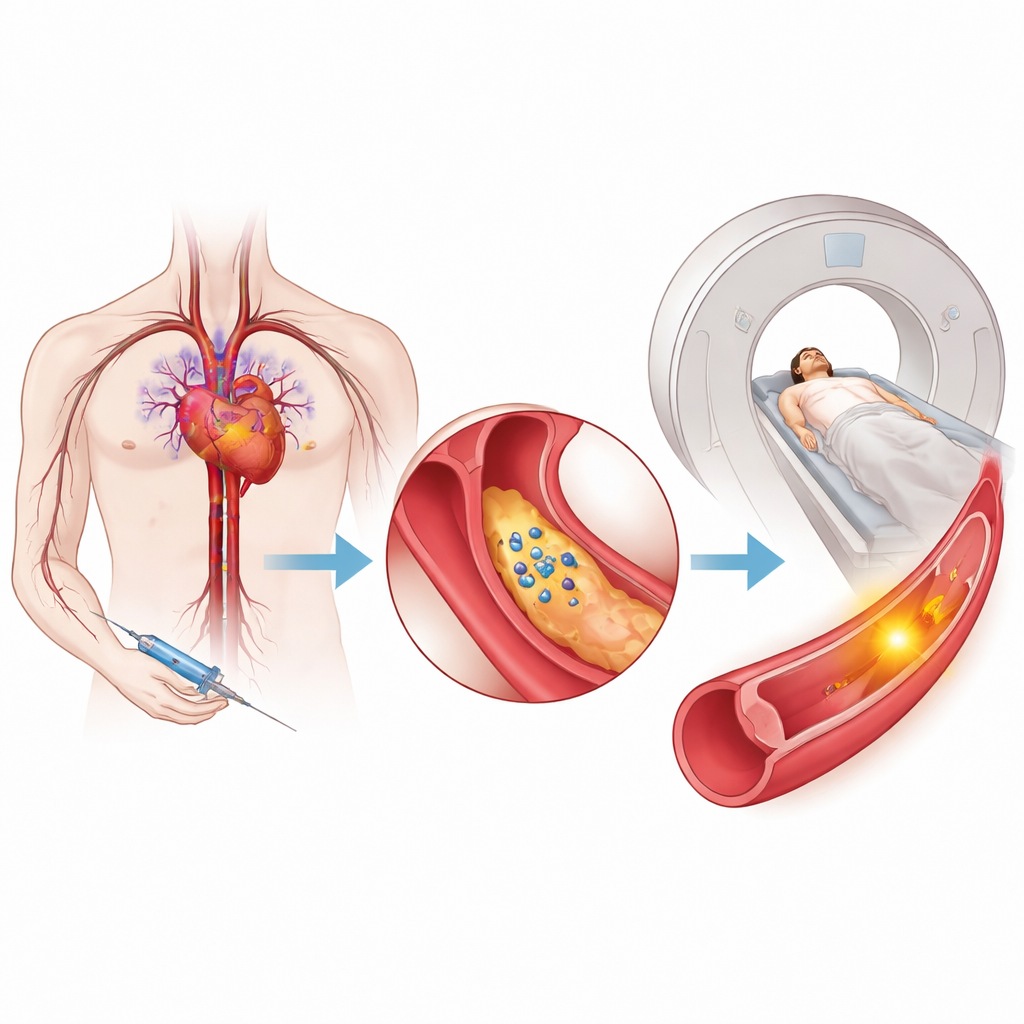
Le danger caché à l’intérieur de la plaque artérielle
L’athérosclérose — accumulation lipidique à l’intérieur des artères — est une cause majeure d’invalidité et de décès prématuré dans le monde. Toutes les plaques ne sont pas également dangereuses : certains dépôts sont relativement stables, tandis que d’autres développent une fine coiffe, s’enflamment et sont susceptibles de se rompre, déclenchant des caillots qui peuvent obstruer l’apport sanguin au cœur ou au cerveau. Les examens standards montrent généralement dans quelle mesure une artère est rétrécie ou la quantité de plaque présente, mais n’indiquent pas de manière fiable si cette plaque est activement lésée et instable. Les traceurs TEP existants mettent surtout en évidence une activité immunitaire générale et ne permettent pas de distinguer clairement l’inflammation nuisible de l’inflammation faisant partie d’un processus réparateur sain.
Une enzyme qui marque l’inflammation réellement dangereuse
Les chercheurs se sont concentrés sur la myéloperoxydase (MPO), une enzyme libérée par certains globules blancs lors d’une réponse agressive et délétère pour les tissus. La MPO participe à l’élimination des microbes, mais lorsqu’elle se répand autour d’une plaque artérielle, elle peut amincir la coiffe protectrice, éroder la surface et favoriser la formation de caillots. Des études animales et humaines ont montré que les plaques présentant une activité MPO élevée sont plus susceptibles d’être instables, et que le blocage de la MPO peut stabiliser les plaques sans nécessairement modifier le nombre de cellules immunitaires présentes. Cela fait de l’activité extracellulaire de la MPO un marqueur prometteur du comportement véritablement dangereux d’une plaque, plutôt que de la simple présence d’inflammation.
Concevoir un traceur intelligent qui reste là où se trouve le problème
Pour capter ce signal, l’équipe a créé un nouveau traceur TEP appelé [68Ga]Ga‑IEMA. Chimiquement, il est conçu pour rester dissous dans le sang et ne pas pénétrer dans les cellules. En tests de laboratoire, le traceur était stable dans le sérum humain et présentait des propriétés l’empêchant de traverser les membranes cellulaires, ce qui signifie qu’il rapporte principalement des événements extracellulaires. Lorsqu’il rencontre une MPO active en présence de ses oxydants habituels, les molécules du traceur se lient entre elles et aux protéines voisines, formant des complexes plus volumineux qui se retrouvent piégés dans le tissu local. Ce comportement « activation‑et‑adhésion » transforme l’activité de la MPO en un signal TEP lumineux au niveau des sites de plaque instable.
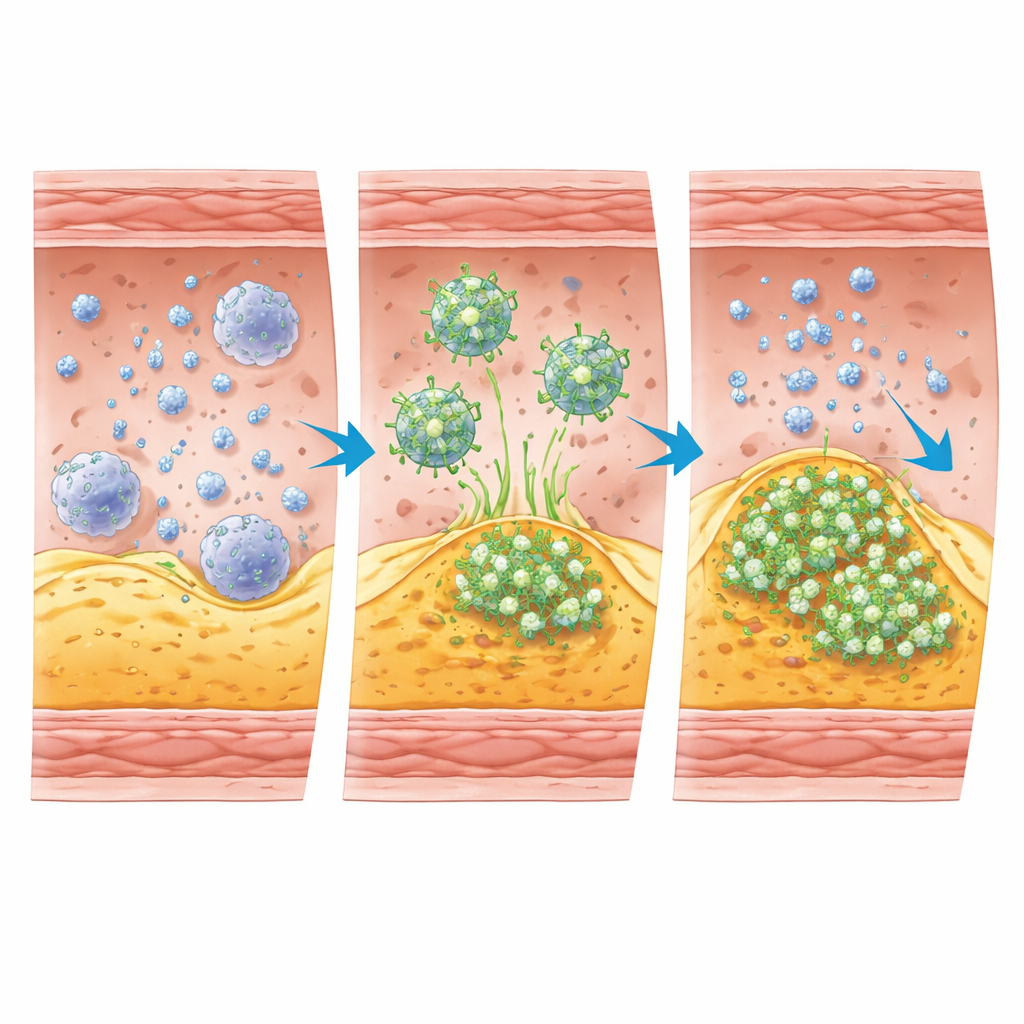
Ce que les études animales ont révélé
Les scientifiques ont d’abord confirmé que [68Ga]Ga‑IEMA pouvait être produit rapidement et proprement, avec une pureté radiochimique élevée, et qu’il s’éliminait principalement par les reins chez la souris. Ils ont ensuite utilisé un modèle murin bien établi qui développe à la fois des plaques stables et instables dans différents segments artériels. Les scans PET/TDM ont montré que le traceur s’accumulait bien plus fortement dans la région artérielle connue pour héberger des plaques instables que dans des régions avec des plaques stables ou sans plaque. Chez des lapins atteints d’athérosclérose avancée, une version non radioactive du traceur était présente à des niveaux plus élevés dans les plaques ayant rompu ou érodé et formé des caillots, comparativement aux plaques plus stables, correspondant là encore au schéma attendu pour une activité MPO élevée.
Perspectives d’utilisation chez les patients
Pris ensemble, les résultats indiquent que [68Ga]Ga‑IEMA agit comme un traceur d’imagerie de l’activité extracellulaire de la MPO, mettant en évidence les plaques plus susceptibles d’être dangereuses plutôt que simplement volumineuses. Parce qu’il utilise le gallium‑68 et une chimie de chélateur déjà familière en médecine nucléaire clinique, le traceur pourrait être transposé aux études humaines avec des obstacles réglementaires relativement modestes et des doses de radiation comparables à celles des agents TEP couramment utilisés. Si des essais ultérieurs confirment sa sécurité et ses performances chez l’homme, ce traceur pourrait aider les cardiologues à localiser les plaques vulnérables et à évaluer si les traitements anti‑inflammatoires apaisent réellement l’inflammation artérielle nocive, rapprochant la prise en charge d’une approche de précision fondée sur le risque.
Citation: Keeling, G.P., Wang, X., Chen, W. et al. Development and validation of an activatable PET radiotracer reporting extracellular myeloperoxidase activity for the detection of unstable atherosclerotic plaque. npj Imaging 4, 23 (2026). https://doi.org/10.1038/s44303-026-00156-9
Mots-clés: athérosclérose, imagerie TEP, myéloperoxydase, plaque vulnérable, radiotraceur