Clear Sky Science · ru
p21+TREM2+ сенесцентные макрофаги подпитывают воспалительное старение и метаболически ассоциированное стеатотическое заболевание печени
Почему старение и здоровье печени тесно связаны
По мере того как люди живут дольше и растет распространённость ожирения, всё больше взрослых страдают от болезней печени, связанных с накоплением жира, и от низкоуровневого системного воспаления. В этом исследовании рассматривался, на первый взгляд, простой, но важный вопрос: какие именно клетки в наших органах поддерживают тлеющее воспаление с возрастом и можно ли, выключив их или удалив, обратить повреждения в печени?
Иммунные клетки, которые стареют и остаются на месте
Наш организм патрулируют макрофаги — иммунные клетки, поглощающие мусор, умирающие клетки и микробы. В отличие от многих других клеток, ткане‑резидентные макрофаги могут жить годами в одном и том же органе. Авторы показывают, что эти долгоживущие сторожа могут вступать в глубокое состояние старения, называемое клеточным сенесценцией. В лабораторных экспериментах мышиные и человеческие макрофаги, подвергнутые повреждению ДНК или высокой нагрузке холестерина, прекращали деление, увеличивались в размере и демонстрировали классические признаки сенесценции. Эти «постаревшие» макрофаги образовали отдельный класс, отличающийся от обычных провоспалительных (M1) или регенеративных (M2) типов, и были отмечены высоким уровнем белка p21 и поверхностного рецептора TREM2.
Как стресс превращает макрофаги в фабрики воспаления
Сенесцентные макрофаги делали больше, чем просто переставали делиться — они изменяли свой секрет. С помощью РНК‑секвенирования и профилирования белков команда обнаружила выраженный секреторный профиль, богатый воспалительными молекулами и ферментами ремоделирования тканей, известный как сенесценция‑ассоциированный секреторный фенотип. Ключевым драйвером был сигнальный каскад, запускаемый, когда поврежденные митохондрии протекали и выбрасывали кусочки своей ДНК в цитоплазму. Эта свободная ДНК активировала систему тревоги cGAS‑STING, что в свою очередь усиливало ответы типа I интерферонов, повышая готовность макрофагов чрезмерно реагировать на дополнительные стимулы. При нарушении митохондриального фермента CMPK2 исследователи сократили утечку ДНК и ослабили программы интерферона и воспаления, показывая, что этот путь помогает фиксировать макрофаги в сенесцентном, провоспалительном состоянии.
Холестерин превращает полезные клетки в жирные, вредные «пенные» клетки
Поскольку старение часто сопровождается повышенным уровнем холестерина в крови, авторы проверили, может ли избыток жира толкать макрофаги в сенесценцию. Детальные измерения липидов показали, что сенесцентные макрофаги накапливают эфиры холестерина и другие липиды, напоминая пенистые клетки, встречающиеся в закупоренных артериях. Когда нормальные макрофаги экспериментально насыщали частицами, богатыми холестерином, они образовывали крупные липидные капли, повышали экспрессию p21 и TREM2 и приобретали признаки сенесценции и провоспалительный секреторный профиль. У стареющих мышей резидентные макрофаги печени — клетки Купфера — демонстрировали ту же сигнатуру с высоким уровнем p21 и TREM2 и сенесцентную генную программу, которую авторы называют профилем «MSen». Эта сигнатура также была повышена в моделях MASLD у мышей и в цирротических человеческих печенях, что указывает на появление холестерин‑индуцированных сенесцентных макрофагов при реальной болезни печени.
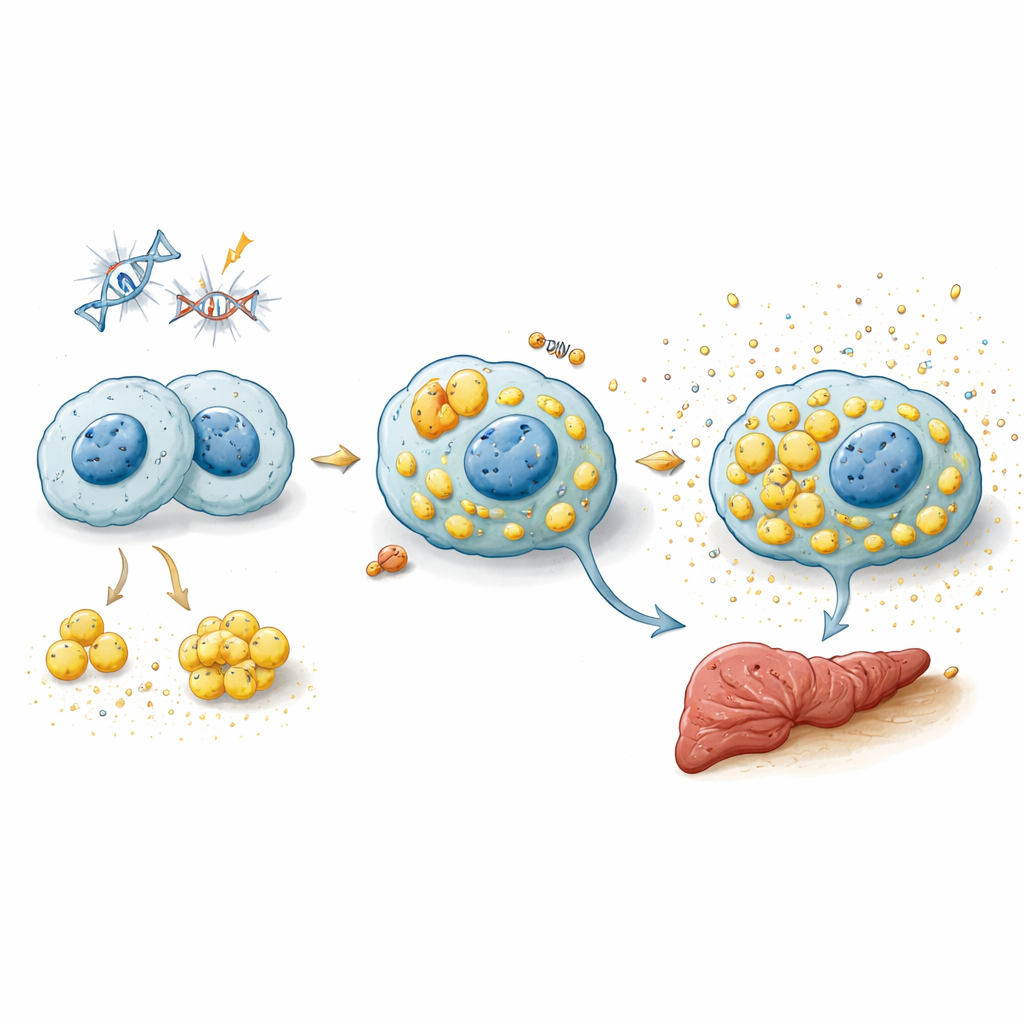
Удаление сенесцентных макрофагов для защиты печени
Если сенесцентные макрофаги приводят к хрониическому воспалению, может ли их селективное устранение улучшить здоровье печени? Команда испытала препарат ABT‑263 (навитоклакс), сенолитическое соединение, заставляющее определённые стрессовые клетки вступать в программируемую гибель путем блокирования антиапоптотических белков. В культуре клеток ABT‑263 убивал сенесцентные макрофаги значительно эффективнее, чем нормальные или просто активированные клетки. У старых мышей прерывистый приём препарата резко снизил долю p21‑позитивных макрофагов в печени, уменьшил экспрессию воспалительных генов и сократил размер жировых капель в тканях печени. В модели MASLD, вызванной холестерином, то же лечение уменьшило размеры печени, улучшило стеатоз, снизило системные маркеры воспаления и частично восстановило уровни NAD⁺ — важной метаболической молекулы, часто истощаемой в стареющих тканях.
Что это значит для старения, жировой болезни печени и будущих лечений
Для неспециалиста главный вывод таков: определённый подкласс долгоживущих иммунных клеток — p21⁺TREM2⁺ сенесцентные макрофаги — действует как постоянный искрящий фактор воспаления в стареющей, перенасыщенной холестерином печени. Эти клетки накапливают жир, перестают обновляться и постоянно выделяют воспалительные сигналы, способствующие стеатозу и метаболическому упадку. Указав их молекулярные отпечатки и показав, что сенолитик может избирательно их удалить, исследование предлагает новый терапевтический подход: вместо того чтобы лишь снижать холестерин или подавлять общее воспаление, врачи однажды смогут нацеливаться на эти сенесцентные макрофаги, чтобы охладить хроническое воспаление, улучшить здоровье печени и, возможно, повлиять на другие возраст‑связанные заболевания, вызванные похожими клетками.
Цитирование: Salladay-Perez, I.A., Avila, I., Estrada, L. et al. p21+TREM2+ senescent macrophages fuel inflammaging and metabolic dysfunction-associated steatotic liver disease. Nat Aging 6, 792–815 (2026). https://doi.org/10.1038/s43587-026-01101-6
Ключевые слова: клеточное старение, макрофаги, стеатоз печени, воспалительное старение, обмен холестерина