Clear Sky Science · fr
Les macrophages sénescents p21+TREM2+ alimentent l'inflammaging et la stéatose hépatique associée à la dysfonction métabolique
Pourquoi le vieillissement et la santé du foie sont étroitement liés
À mesure que la longévité augmente et que l'obésité progresse, de plus en plus d'adultes développent une maladie du foie gras et une inflammation systémique de bas grade. Cette étude pose une question apparemment simple mais aux grandes implications : quelles cellules spécifiques de nos organes maintiennent le système immunitaire en état de combustion lente avec l'âge, et peut‑on éteindre — ou éliminer — ces cellules pour inverser les lésions hépatiques ?
Les cellules immunitaires qui vieillissent et restent en place
Notre organisme est parcouru par des macrophages, des cellules immunitaires qui avalent débris, cellules en train de mourir et microbes. Contrairement à de nombreuses autres cellules, les macrophages résidents tissulaires peuvent vivre des années dans un même organe. Les auteurs montrent que ces sentinelles longévives peuvent entrer dans un état de vieillissement profond appelé sénescence cellulaire. En laboratoire, des macrophages de souris et d'humain exposés à un stress endommageant l'ADN ou à un excès de cholestérol ont cessé de se diviser, ont augmenté de taille et ont affiché des caractéristiques classiques de la sénescence. Ces macrophages « âgés » formaient un groupe distinct, différent des types pro‑inflammatoires (M1) ou réparateurs (M2), et étaient marqués par des niveaux élevés de la protéine p21 et du récepteur de surface TREM2.
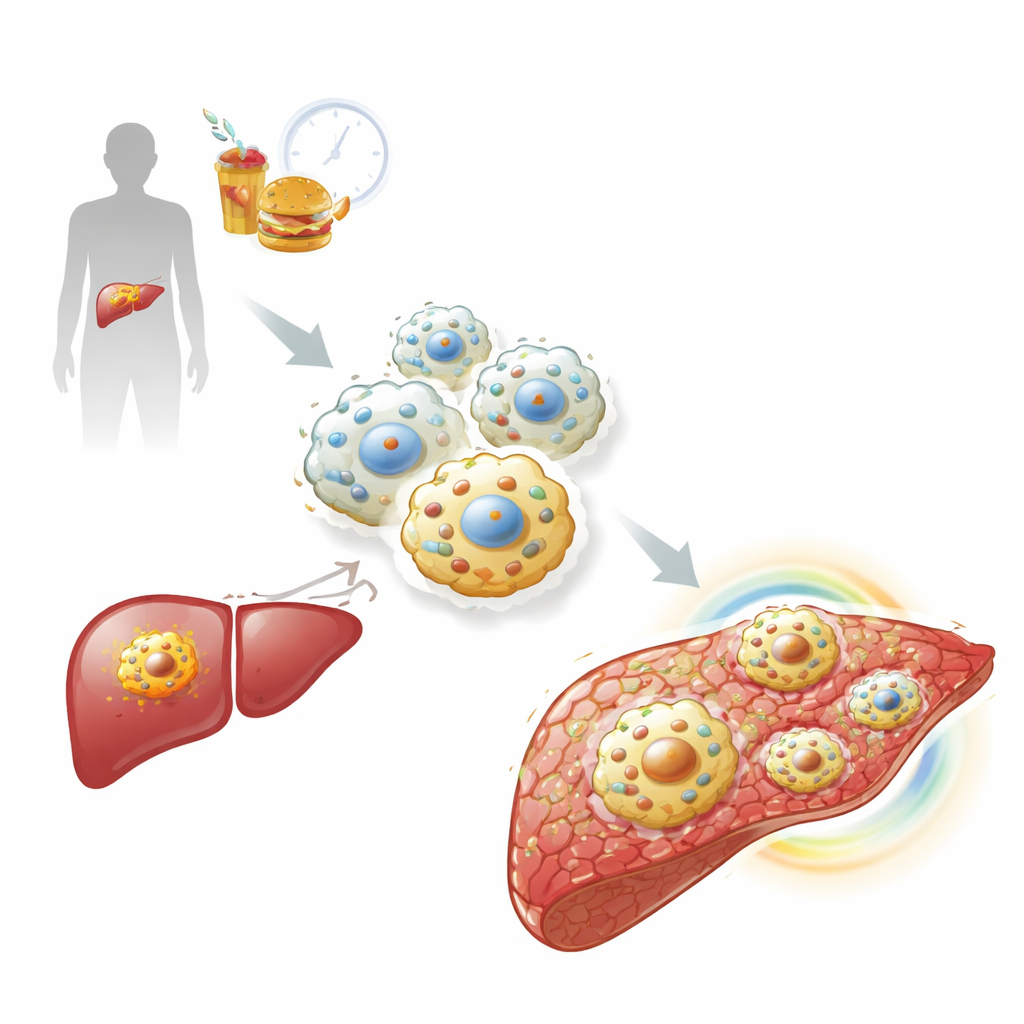
Comment les macrophages stressés se transforment en usines d'inflammation
Les macrophages sénescents n'ont pas seulement arrêté de se diviser : ils ont modifié leur profil sécrétoire. Par séquençage de l'ARN et profilage protéique, l'équipe a identifié un fort motif « sécrétoire » riche en molécules inflammatoires et en enzymes de remodelage tissulaire, connu sous le nom de phénotype sécrétoire associé à la sénescence. Un moteur clé était une cascade de signalisation déclenchée lorsque des mitochondries endommagées fuyaient des fragments d'ADN dans le cytosol. Cet ADN libre activait un système d'alerte appelé cGAS‑STING, qui renforçait à son tour les réponses d'interféron de type I, préparant les macrophages à sur‑réagir à des déclencheurs supplémentaires. Lorsque les chercheurs ont perturbé une enzyme mitochondriale, CMPK2, ils ont réduit cette fuite d'ADN et atténué les programmes d'interféron et inflammatoires, montrant que cette voie contribue à enfermer les macrophages dans leur état sénescent et inflammatoire.
Le cholestérol transforme des cellules utiles en cellules « mousseuses » grasses et nocives
Comme le vieillissement s'accompagne souvent d'un taux de cholestérol élevé, les investigateurs se sont demandé si la surcharge lipidique pouvait pousser les macrophages vers la sénescence. Des mesures lipidiques détaillées ont révélé que les macrophages sénescents accumulaient des esters de cholestérol et d'autres lipides, ressemblant aux cellules « mousseuses » observées dans les artères obstruées. Lorsque des macrophages normaux ont été expérimentalement gavés de particules riches en cholestérol, ils ont développé de grosses gouttelettes lipidiques, sur‑exprimé p21 et TREM2, et acquis des caractéristiques sénescentes ainsi qu'un profil sécrétoire inflammatoire. Chez la souris vieillissante, les macrophages résidents du foie — les cellules de Kupffer — présentaient la même signature riche en p21 et TREM2 et un programme génique sénescent que les auteurs appellent le profil « MSen ». Cette signature était également élevée dans des modèles murins de stéatose hépatique associée à la dysfonction métabolique (MASLD) et dans des foies cirrhotiques humains, indiquant que des macrophages sénescents induits par le cholestérol apparaissent dans la maladie hépatique en conditions réelles.
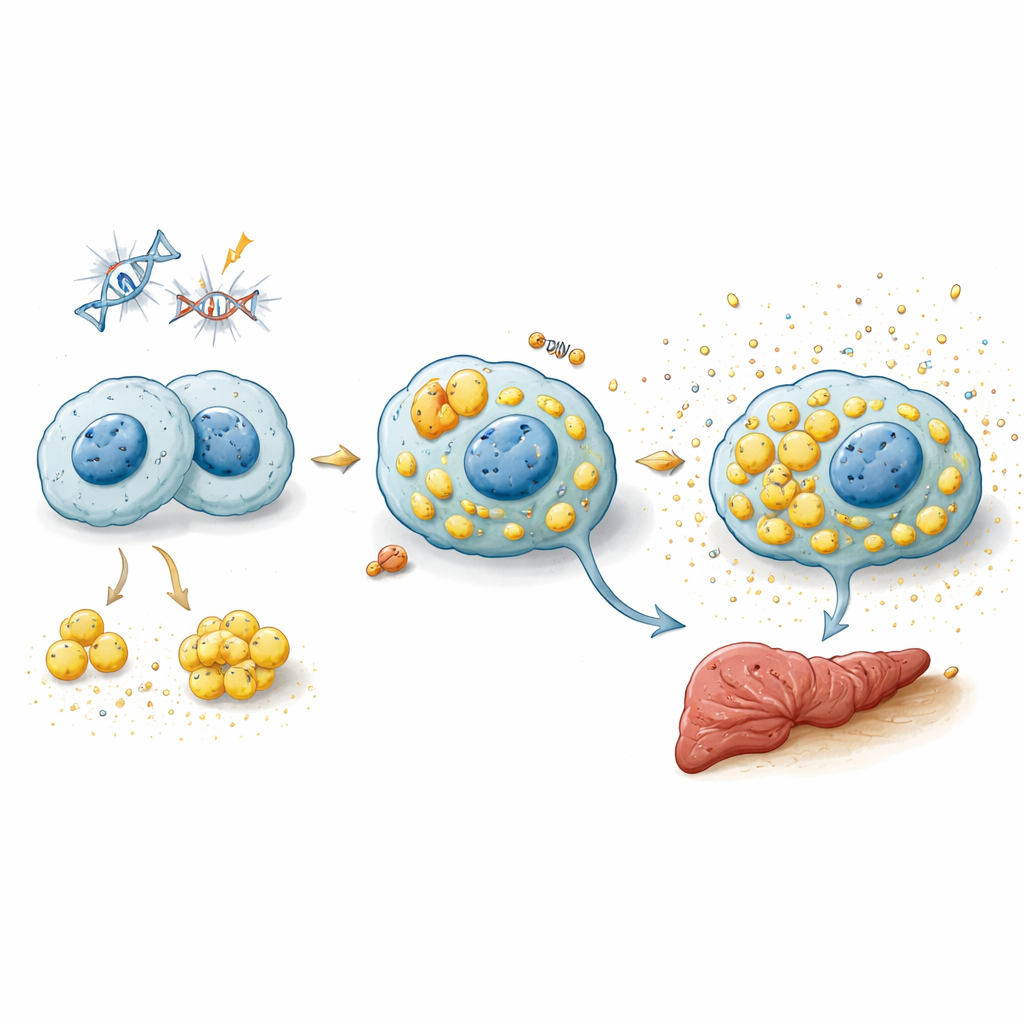
Éliminer les macrophages sénescents pour protéger le foie
Si les macrophages sénescents pilotent l'inflammation chronique, leur élimination sélective pourrait‑elle améliorer la santé hépatique ? L'équipe a testé un médicament appelé ABT‑263 (navitoclax), un composé sénolytique qui force certaines cellules stressées à entrer en mort programmée en bloquant des protéines anti‑apoptotiques. En culture cellulaire, l'ABT‑263 a tué les macrophages sénescents beaucoup plus efficacement que les macrophages normaux ou simplement activés. Chez des souris âgées, des doses intermittentes ont fortement réduit la proportion de macrophages p21‑positifs dans le foie, diminué l'expression de gènes inflammatoires et réduit la taille des gouttelettes lipidiques dans le tissu hépatique. Dans un modèle murin de MASLD induit par le cholestérol, le même traitement a réduit la taille du foie, amélioré les altérations lipidiques, abaissé des marqueurs inflammatoires systémiques et partiellement restauré les niveaux de NAD⁺, une molécule métabolique vitale souvent épuisée dans les tissus âgés.
Ce que cela signifie pour le vieillissement, la stéatose hépatique et les traitements futurs
Pour un public non spécialisé, l'idée principale est qu'une sous‑classe spécifique de cellules immunitaires longévives — les macrophages sénescents p21⁺TREM2⁺ — agit comme une étincelle persistante d'inflammation dans le foie vieillissant et encombré de cholestérol. Ces cellules accumulent des lipides, cessent de se renouveler et libèrent en continu des signaux inflammatoires qui favorisent la stéatose hépatique et le déclin métabolique. En identifiant leurs empreintes moléculaires et en montrant qu'un médicament sénolytique peut les cibler sélectivement, cette étude suggère un nouvel angle thérapeutique : plutôt que de se contenter d'abaisser le cholestérol ou de supprimer l'inflammation de façon large, on pourrait un jour cibler ces macrophages sénescents pour refroidir l'inflammation chronique, améliorer la santé du foie et peut‑être influencer d'autres maladies liées à l'âge conduites par des cellules similaires.
Citation: Salladay-Perez, I.A., Avila, I., Estrada, L. et al. p21+TREM2+ senescent macrophages fuel inflammaging and metabolic dysfunction-associated steatotic liver disease. Nat Aging 6, 792–815 (2026). https://doi.org/10.1038/s43587-026-01101-6
Mots-clés: sénescence cellulaire, macrophages, maladie du foie gras, inflammaging, métabolisme du cholestérol