Clear Sky Science · ru
Транскрипционные и функциональные профили нейронов, экспрессирующих мускариновые рецепторы, в латеральной префронтальной и передней поясной коре приматов
Как нейромедиатор формирует мышление и чувства
Каждую секунду ваш мозг балансирует между мыслями и эмоциями. Два ключевых узла в этой работе — латеральная префронтальная кора, участвующая в планировании и рабочей памяти, и передняя поясная кора, отслеживающая мотивацию, конфликт и боль. В этом исследовании поставлен, казалось бы, простой вопрос: как один и тот же химический сигнал — ацетилхолин — по-разному настраивает эти два региона, чтобы поддерживать обучение, гибкость и эмоциональный контроль? 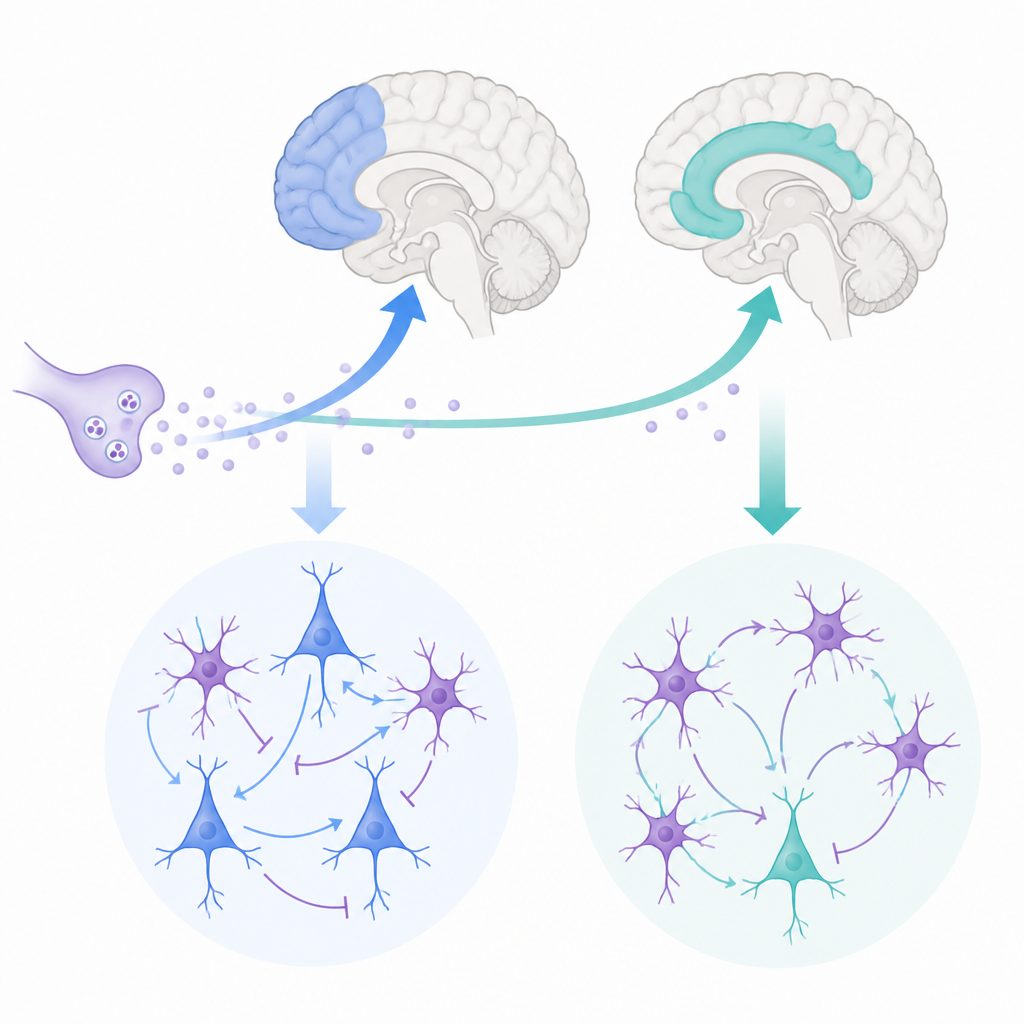
Взгляд поближе на два центра мышления
Исследователи сосредоточились на двух областях лобной доли макак-резусов, которые тесно соответствуют человеческим регионам мозга. Латеральная префронтальная кора помогает удерживать информацию в памяти и принимать решения, тогда как передняя поясная кора связывает действия с вознаграждением, ошибками и эмоциями. Обе области получают вход от ацетилхолина — химического вещества, выделяемого глубокими центрами мозга, известного тем, что влияет на внимание и память. При этом передняя поясная кора получает более плотный ацетилхолиновый вход, чем латеральная префронтальная кора, что указывает на то, что этот медиатор может по-разному формировать их активность.
Чтение генетических отпечатков клеток мозга
Чтобы выяснить, как отдельные клетки реагируют на ацетилхолин, команда использовала секвенирование РНК одиночных ядер, которое позволяет определить, какие гены активны в тысячах клеток одновременно. В фокусе были мускариновые рецепторы — основные чувствительные к ацетилхолину «переключатели» на кортикальных нейронах, кодируемые четырьмя генами CHRM1–CHRM4. Удивительно, но было обнаружено, что ген CHRM3 наиболее широко экспрессируется в обоих регионах — в более чем половине клеток, хотя предыдущие белковые исследования указывали на большую распространённость рецептора m1, кодируемого CHRM1. Большинство возбуждающих и тормозных нейронов несли CHRM3, часто вместе с CHRM1, тогда как CHRM2 показал более селективный рисунок экспрессии, особенно в глубоких слоях возбуждающих клеток и в ключевой популяции быстро спайкинговых тормозных нейронов.
Когда сообщения генов и белки не совпадают
Чтобы разрешить несоответствие между РНК и белком, учёные совместили флуоресцентную маркировку белков-рецепторов с in situ обнаружением их РНК в срезах мозга. Они подтвердили, что белок m1 в целом выражен сильнее, чем белок m3, но обнаружили, что РНК CHRM3 чаще локализуется как в ядре, так и в окружающем цитоплазматическом пространстве, тогда как РНК CHRM1 преимущественно находится в цитоплазме. Это указывает на то, что сообщения CHRM3 могут задерживаться в ядре или переводиться в белок медленнее, что помогает объяснить, почему его РНК выглядит обильной, а белок менее доминирующим. Одновременно клетки, экспрессирующие CHRM1 и CHRM3, имели очень схожие генные подписи, связанные с синаптической передачей и пластичностью, тогда как CHRM2-положительные клетки сформировали явно отличную группу, связанную с путями, ослабляющими высвобождение нейромедиаторов.
Два региона — два стиля синаптической настройки
Далее команда перешла от молекул к функциям, регистрируя небольшие электрические токи отдельных пирамида́льных нейронов слоя 3 в срезах мозга. Ткани купали в карбахоле — препарате, активирующем ацетилхолиновые рецепторы — и измеряли спонтанные возбуждающие и тормозные синаптические события. В передней поясной коре такая стимуляция, как правило, снижала возбуждающий вход и усиливала тормозные токи, сдвигая местный баланс в сторону более сильного торможения. В латеральной префронтальной коре, напротив, холинергическая стимуляция чаще ослабляла тормозные токи и относительно сохраняла возбуждение, подталкивая сеть к более активному, возбудимому состоянию. Эти изменения сопровождались перестройкой формы и плотности дендритных шипиков — мелких выступов, в которых располагаются возбуждающие синапсы: карбахол уменьшал количество крупных стабильных «грибовидных» шипиков и увеличивал долю более тонких, гибких, с несколько различными временными характеристиками в каждом регионе. 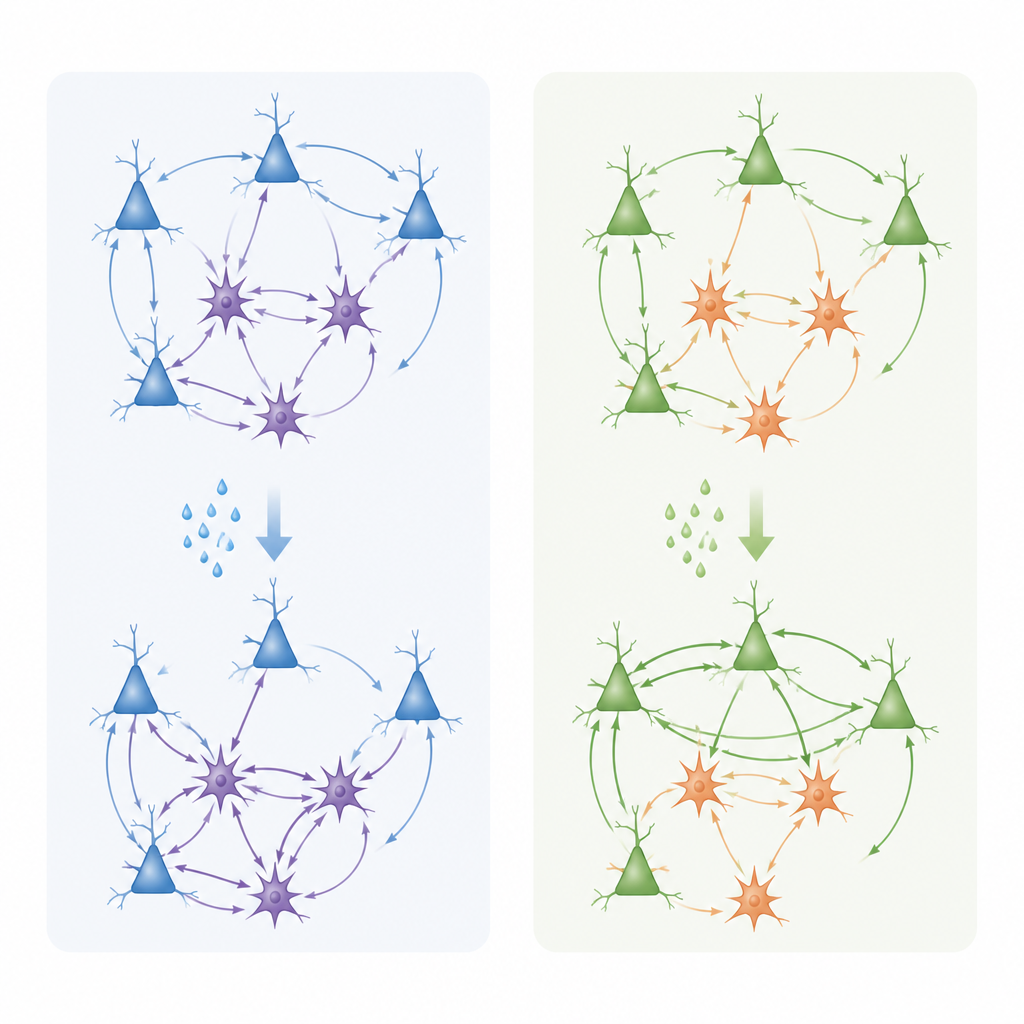
Что это значит для обучения и психического здоровья
В совокупности результаты показывают, что ацетилхолин не действует в лобной коре как простой выключатель «вкл/выкл». Скорее он вовлекает разные сочетания мускариновых рецепторов в определённых типах клеток и слоях, чтобы настраивать соотношение возбуждения и торможения в зависимости от региона. В передней поясной коре ацетилхолин, по-видимому, улучшает отношение сигнал/шум, ослабляя возбуждающий драйв и усиливая торможение, одновременно поддерживая гены, вовлечённые в синаптическое ремоделирование, важное для эмоционального обучения и обработки боли. В латеральной префронтальной коре он склонен сохранять или усиливать возбуждающий тон и способствовать структурной гибкости синапсов, что может помогать поддержанию рабочей памяти и адаптивного принятия решений. Связав детальные карты экспрессии генов с реальным временем изменений синаптической активности, эта работа предлагает механистическую основу для понимания того, как холинергические нарушения могут способствовать когнитивным и аффективным симптомам при нейропсихиатрических расстройствах, и указывает на то, что нацеливание на специфические подтипы мускариновых рецепторов в определённых цепях может позволить создавать более точечные терапии в будущем.
Цитирование: Tsolias, A., Mojica, C.A., Yamani, R. et al. Transcriptional and functional profiles of muscarinic receptor-expressing neurons in primate lateral prefrontal and anterior cingulate cortices. Commun Biol 9, 620 (2026). https://doi.org/10.1038/s42003-026-09866-7
Ключевые слова: ацетилхолин, префронтальная кора, передняя поясная кора, мускариновые рецепторы, синаптическая пластичность