Clear Sky Science · fr
Profils transcriptionnels et fonctionnels des neurones exprimant des récepteurs muscariniques dans les cortex préfrontal latéral et cingulaire antérieur de primates
Comment un messager cérébral façonne la pensée et le ressenti
À chaque instant, votre cerveau met en balance ce que vous pensez et ce que vous ressentez. Deux centres majeurs pour cela sont le cortex préfrontal latéral, impliqué dans la planification et la mémoire de travail, et le cortex cingulaire antérieur, qui suit la motivation, les conflits et la douleur. Cette étude pose une question apparemment simple : comment le même signal chimique, l’acétylcholine, module-t-il ces deux régions de manières différentes pour soutenir l’apprentissage, la flexibilité et le contrôle émotionnel ? 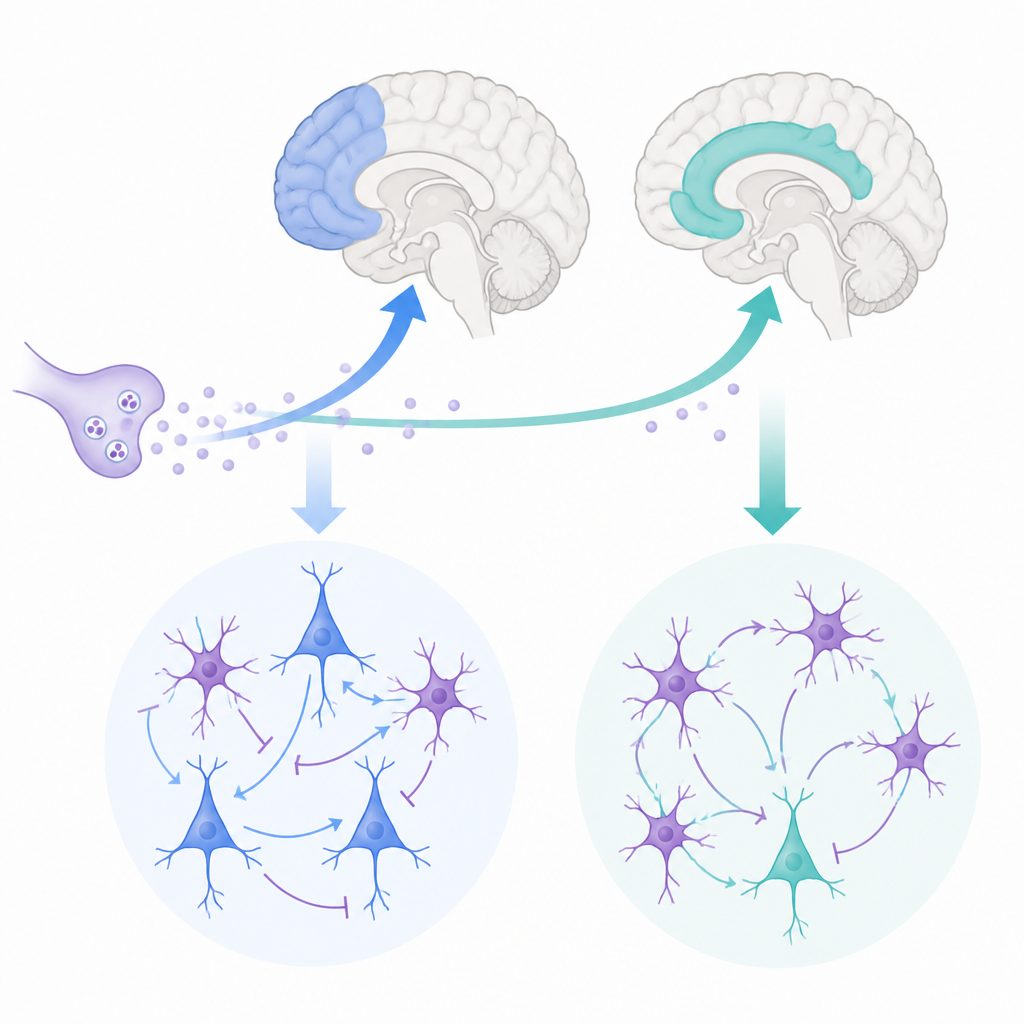
Un examen rapproché de deux centres de la cognition
Les chercheurs se sont concentrés sur deux zones du lobe frontal chez des macaques rhésus qui ressemblent étroitement aux régions humaines. Le cortex préfrontal latéral nous aide à maintenir des informations en mémoire et à prendre des décisions, tandis que le cortex cingulaire antérieur relie les actions aux récompenses, aux erreurs et aux émotions. Les deux régions reçoivent des projections cholinergiques — l’acétylcholine étant libérée par des centres profonds du cerveau et connue pour influencer attention et mémoire. Pourtant, le cingulaire antérieur reçoit une innervation cholinergique plus dense que le préfrontal latéral, ce qui suggère que ce messager pourrait sculpter leur activité de façons distinctes.
Lire les empreintes génétiques des cellules cérébrales
Pour savoir comment chaque cellule répond à l’acétylcholine, l’équipe a utilisé le séquençage ARN de noyaux uniques, qui révèle quels gènes sont actifs dans des milliers de cellules simultanément. Ils se sont intéressés aux récepteurs muscariniques, principaux détecteurs de l’acétylcholine sur les neurones corticaux, codés par quatre gènes nommés CHRM1 à CHRM4. De manière surprenante, ils ont trouvé que le gène CHRM3 était le plus largement exprimé dans les deux régions, présent dans plus de la moitié des cellules, alors que des études protéiques antérieures laissaient penser que le récepteur m1, codé par CHRM1, était plus abondant. La plupart des neurones excitateurs et inhibiteurs portaient CHRM3, souvent conjointement avec CHRM1, tandis que CHRM2 montrait un profil plus sélectif, en particulier dans les cellules excitatrices des couches profondes et un groupe clé de neurones inhibiteurs à décharge rapide.
Quand ARN et protéines ne coïncident pas
Pour résoudre le décalage entre ARN et protéine, les scientifiques ont combiné le marquage fluorescent des protéines réceptrices avec la détection in situ de leurs ARN dans des coupes de cerveau. Ils ont confirmé que la protéine m1 était globalement plus forte que la protéine m3, mais ont découvert que l’ARN CHRM3 avait tendance à se localiser à la fois dans le noyau et dans le cytoplasme environnant, tandis que l’ARN CHRM1 se trouvait surtout dans le cytoplasme. Cela suggère que les messages CHRM3 peuvent être retenus dans le noyau ou traduits en protéine plus lentement, ce qui aide à expliquer pourquoi son ARN apparaît abondant alors que sa protéine est moins dominante. Parallèlement, les cellules exprimant CHRM1 et CHRM3 partageaient des signatures géniques très similaires liées à la signalisation synaptique et à la plasticité, tandis que les cellules CHRM2-positives formaient un groupe clairement distinct associé à des voies qui réduisent la libération des neurotransmetteurs.
Deux régions, deux modalités d’ajustement synaptique
L’équipe est ensuite passée des molécules à la fonction en enregistrant de petits courants électriques dans des neurones pyramidaux de la couche 3 sur des coupes de cerveau. Ils ont baigné le tissu dans la carbachol, un agoniste des récepteurs cholinergiques, et mesuré les événements synaptiques excitateurs et inhibiteurs spontanés. Dans le cingulaire antérieur, cette stimulation réduisait généralement les entrées excitatrices tout en augmentant les courants inhibiteurs, décalant l’équilibre local vers un freinage plus marqué de l’activité. Dans le cortex préfrontal latéral, en revanche, la stimulation cholinergique affaiblissait le plus souvent les courants inhibiteurs en laissant l’excitation relativement plus forte, poussant le réseau vers un état plus actif et excitable. Ces changements s’accompagnaient de modifications de la forme et de la densité des épines dendritiques — les petites saillies qui hébergent les synapses excitatrices : la carbachol réduisait les grosses épines « en champignon » stables et augmentait les épines plus fines et flexibles, avec des dynamiques temporelles légèrement différentes selon la région. 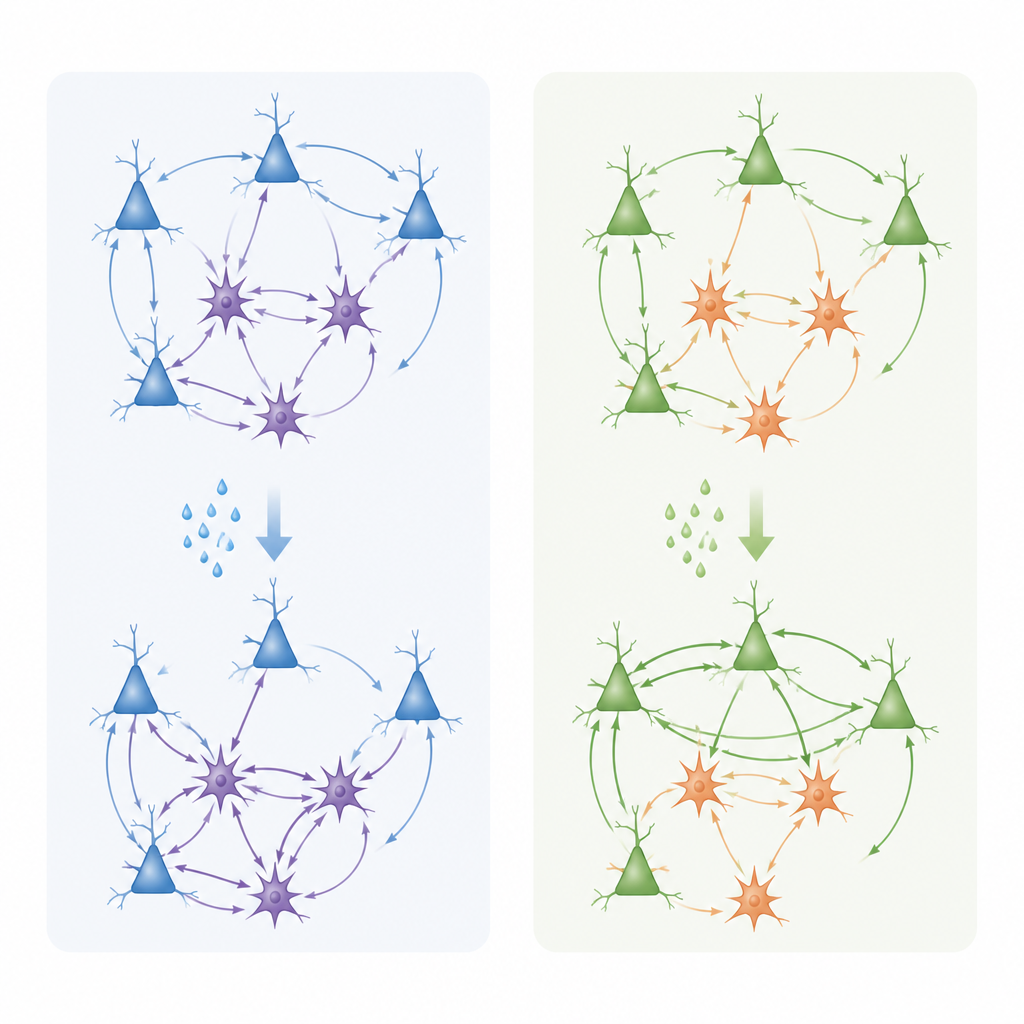
Ce que cela implique pour l’apprentissage et la santé mentale
Pris ensemble, les résultats montrent que l’acétylcholine n’agit pas comme un simple interrupteur marche–arrêt dans le cortex frontal. Au contraire, elle mobilise des combinaisons distinctes de récepteurs muscariniques dans des types cellulaires et des couches spécifiques pour régler l’équilibre entre excitation et inhibition de manière dépendante de la région. Dans le cingulaire antérieur, l’acétylcholine semble affiner le rapport signal/bruit en atténuant la poussée excitatrice et en renforçant l’inhibition, tout en soutenant des gènes impliqués dans le remodelage synaptique important pour l’apprentissage émotionnel et le traitement de la douleur. Dans le cortex préfrontal latéral, elle tend à préserver ou à renforcer le tonus excitateur et à favoriser la flexibilité structurelle des synapses, ce qui pourrait aider à soutenir la mémoire de travail et la prise de décision adaptative. En reliant des cartographies détaillées d’expression génique à des changements en temps réel de l’activité synaptique, ce travail fournit un cadre mécanistique expliquant comment des déséquilibres cholinergiques pourraient contribuer à des symptômes cognitifs et affectifs dans des troubles neuropsychiatriques, et suggère que cibler des sous-types spécifiques de récepteurs muscariniques dans des circuits définis pourrait permettre des thérapies plus précises à l’avenir.
Citation: Tsolias, A., Mojica, C.A., Yamani, R. et al. Transcriptional and functional profiles of muscarinic receptor-expressing neurons in primate lateral prefrontal and anterior cingulate cortices. Commun Biol 9, 620 (2026). https://doi.org/10.1038/s42003-026-09866-7
Mots-clés: acétylcholine, cortex préfrontal, cingulaire antérieur, récepteurs muscariniques, plasticité synaptique