Clear Sky Science · ru
Прояснение и функциональная характеристика биосинтетического пути природного подсластителя филлодулцина в Hydrangea macrophylla
Растение, дающее сверхсладкий лист
Представьте чашку чая из листьев, которые по своей естественной сладости в сотни раз превосходят сахар, но при этом дают почти никаких калорий. Куст Hydrangea macrophylla делает именно это, производя соединение под названием филлодулцин, давно используемое в традиционном японском «сладком чае» и ныне привлекающее внимание как потенциальный натуральный подсластитель и лекарственная составляющая. В этом исследовании задают на первый взгляд простой вопрос: как именно растение синтезирует эту мощную сладкую молекулу в своих листьях?
От общих строительных блоков к особой сладости
Растения производят огромное разнообразие специализированных химических веществ из небольшого набора базовых ингредиентов. В Hydrangea macrophylla филлодулцин принадлежит к семейству соединений, все из которых начинаются с аминокислоты фенилаланина. Исследователи собрали 182 различных сортов гортензии и измерили содержание филлодулцина и тесно связанного с ним соединения гидрангенола в их листьях. Некоторые сорта вырабатывали большое количество этих сладких молекул, другие — очень мало, а родственный вид Hydrangea paniculata не производил их вовсе. Эта природная вариативность предоставила живую лабораторию для прослеживания, какие внутренние химические пути ведут к филлодулцину, а какие — в обход него.
Прослеживание химических троп внутри листа
Далее команда проанализировала 14 ключевых промежуточных соединений более широкой фенилпропаноидной цепочки — центрального химического маршрута у многих растений. У сортов с высоким содержанием филлодулцина обычно наблюдались повышенные уровни фенилаланина, p-кумаровой кислоты, норингенина, ресвератрола, умбелиферона и производного под названием тунбергинол C. Напротив, у растений с низким уровнем филлодулцина накапливались больше кофеиновая и феруловая кислоты и несколько родственных кумаринов, что указывает на то, что в этих растениях поток химических превращений отклоняется в боковые ветви, которые не ведут к подсластителю. Статистические анализы показали сильные положительные корреляции между филлодулцином и «высокой» группой промежуточных соединений и сильные отрицательные корреляции с «низкой» группой, что указывает на предпочтительные и альтернативные ответвления во внутренней химии растения.
Чтение генетического рецепта растения
Один лишь химический профиль не может показать, какие ферменты действительно выполняют каждое звено, поэтому учёные также изучили активность генов в листьях выбранных сортов с высоким и низким содержанием сладких веществ, а также у несладкого вида. С помощью РНК‑секвенирования они сравнили, какие гены включены или выключены, и сопоставили это с известными метаболическими путями. У растений, продуцирующих много филлодулцина или гидрангенола, гены, связанные с синтезом фенилпропаноидов, флавоноидов и стилбенов, были сильно обогащены. Сетевой анализ, группирующий коактивные гены в модули, показал, что определённые кластеры генов тесно коррелируют с уровнями филлодулцина, гидрангенола и ключевых промежуточных соединений, таких как p-кумаровая кислота и ресвератрол, что намекает на общие управляющие цепочки.
Ключевые этапы на пути к сладкой молекуле
Среди множества генов несколько выделялись как правдоподобные драйверы формирования филлодулцина. У сортов с высоким содержанием сладкого соединения сильно экспрессировались гены, кодирующие ферменты, такие как p-кумароилтриацетатсинтаза (CTAS), поликетидсинтазы типа III, кеторедуктазы, поликетидные циклазы и фермент, модифицирующий ресвератрол (ROMT). Эти ферменты могут собирать или перестраивать циклические молекулы, напоминающие известные промежуточные звенья на пути к филлодулцину и гидрангенолу. В растениях с низкой сладостью более активен другой набор генов, направляющий p-кумаровую кислоту в сторону кофеиновой и феруловой кислот, что подкрепляет идею метаболического раздвоения, где одна ветвь ведёт к сладости, а другая — к несвязанным соединениям. У несладкой Hydrangea paniculata критические ферменты, наблюдаемые у сладколистных растений, в основном отсутствовали или использовались в меньшей степени.
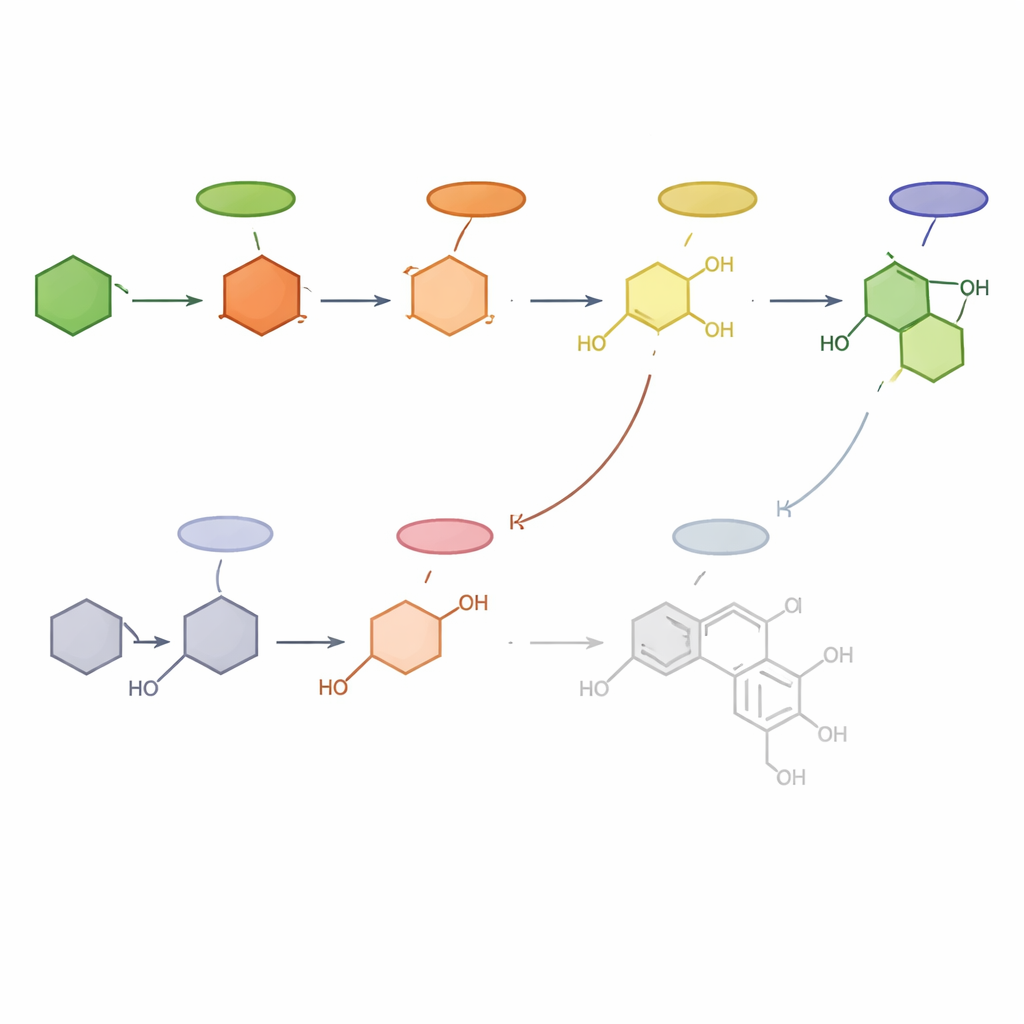
Построение новой карты сладкого пути
Комбинируя химические «отпечатки» с профилями активности генов, исследователи предлагают подробную рабочую модель того, как Hydrangea macrophylla синтезирует филлодулцин. По их мнению, путь начинается с фенилаланина и проходит через p-кумаровую кислоту, затем разветвляется как минимум на три маршрута, включающие гидрангенол, ресвератрол и тунбергинол C, при этом последний вероятно служит непосредственным предшественником. В сортах, где доминируют боковые маршруты, филлодулцина образуется значительно меньше. Хотя некоторые этапы остаются гипотетическими, эта карта превращает некогда таинственный традиционный подсластитель в чётко определённый биохимический продукт. Для неспециалистов вывод ясен: понимание этой природной «фабрики» на молекулярном уровне открывает путь к селекции более сладких сортов гортензии, улучшению устойчивого производства филлодулцина и целенаправленному изучению его обещающих свойств для здоровья.
Цитирование: Padmakumar Sarala, G., Engel, F., Hartmann, A. et al. Elucidation and functional characterization of the biosynthetic pathway of the natural sweetener phyllodulcin in Hydrangea macrophylla. Sci Rep 16, 12044 (2026). https://doi.org/10.1038/s41598-026-47892-x
Ключевые слова: натуральные подсластители, Гортензия, метаболизм растений, филлодулцин, биосинтез