Clear Sky Science · fr
Élucidation et caractérisation fonctionnelle de la voie biosynthétique du édulcorant naturel phyllodulcine dans Hydrangea macrophylla
Une plante qui produit une feuille ultra-sucrée
Imaginez une tasse de thé préparée avec des feuilles naturellement des centaines de fois plus sucrées que le sucre, tout en apportant presque aucune calorie. L’arbuste Hydrangea macrophylla fait exactement cela en produisant un composé appelé phyllodulcine, utilisé depuis longtemps dans le « thé sucré » traditionnel japonais et qui suscite désormais l’intérêt comme édulcorant naturel potentiel et ingrédient médicinal. Cette étude pose une question apparemment simple : comment la plante synthétise‑t‑elle réellement cette molécule très sucrée à l’intérieur de ses feuilles ?
Des éléments de base communs vers une douceur particulière
Les plantes fabriquent une énorme variété de composés spécialisés à partir d’un petit jeu d’ingrédients de base. Chez Hydrangea macrophylla, la phyllodulcine appartient à une famille de composés qui prennent tous leur origine dans l’acide aminé phénylalanine. Les chercheurs ont collecté 182 variétés différentes d’hortensias et ont mesuré les quantités de phyllodulcine et d’un composé étroitement lié, l’hydrangenol, dans leurs feuilles. Certaines variétés produisaient beaucoup de ces molécules sucrées, d’autres très peu, et une espèce apparentée, Hydrangea paniculata, n’en produisait aucune. Cette variation naturelle a fourni un laboratoire vivant pour retracer quelles routes chimiques internes conduisent vers — ou s’éloignent de — la phyllodulcine.
Suivre les traces chimiques à l’intérieur de la feuille
L’équipe a ensuite profilé 14 composés intermédiaires clés issus de la voie générale des phénylpropanoïdes, une route chimique centrale chez de nombreuses plantes. Les variétés riches en phyllodulcine présentaient généralement des niveaux élevés de phénylalanine, d’acide p‑coumarique, de naringénine, de resvératrol, d’umbelliférone et d’un dérivé appelé thunberginol C. En revanche, les plantes avec peu ou pas de phyllodulcine accumulaient davantage d’acides caféique et férulique et plusieurs coumarines apparentées, ce qui suggère que, chez ces plantes, le flux chimique est détourné vers des voies secondaires qui n’aboutissent pas à l’édulcorant. Des analyses statistiques ont montré de fortes corrélations positives entre la phyllodulcine et l’ensemble « élevé » d’intermédiaires, et de fortes corrélations négatives avec l’ensemble « faible », indiquant des embranchements préférentiels et alternatifs au sein de la chimie interne de la plante.
Lire la recette génétique de la plante
Les indices chimiques seuls ne peuvent pas révéler quelles enzymes effectuent chaque étape, aussi les scientifiques ont‑ils aussi examiné l’activité génique dans les feuilles de variétés sélectionnées à forte et faible teneur en sucres, ainsi que dans l’espèce non sucrée. Grâce au séquençage de l’ARN, ils ont comparé les gènes activés ou réprimés et les ont cartographiés sur des voies métaboliques connues. Chez les plantes qui produisaient beaucoup de phyllodulcine ou d’hydrangenol, les gènes associés à la production de phénylpropanoïdes, de flavonoïdes et de stilbènes étaient fortement enrichis. Une analyse de réseau regroupant les gènes co‑actifs en modules a montré que certains groupes de gènes corrélaient étroitement avec les niveaux de phyllodulcine, d’hydrangenol et d’intermédiaires clés comme l’acide p‑coumarique et le resvératrol, suggérant l’existence de circuits de régulation partagés.
Étapes clés sur la route du composé sucré
Parmi les nombreux gènes, plusieurs se sont distingués comme des candidats plausibles à la formation de la phyllodulcine. Les variétés riches en ce composé exprimaient fortement des gènes codant des enzymes telles que la p‑coumaroyltriacétate synthase (CTAS), des synthases de polykétides de type III, des réductases céto, des cyclases de polykétides et une enzyme modifiant le resvératrol (ROMT). Ces enzymes peuvent assembler ou remodeler des structures cycliques ressemblant à des intermédiaires connus sur le chemin menant à la phyllodulcine et à l’hydrangenol. Chez les plantes peu sucrées, un ensemble différent de gènes qui oriente l’acide p‑coumarique vers les acides caféique et férulique était plus actif, renforçant l’idée d’une bifurcation métabolique où une branche mène à la douceur et l’autre à des composés non liés. L’espèce non sucrée Hydrangea paniculata présentait en grande partie une absence ou une sous‑utilisation des enzymes critiques observées chez les plantes à feuilles sucrées.
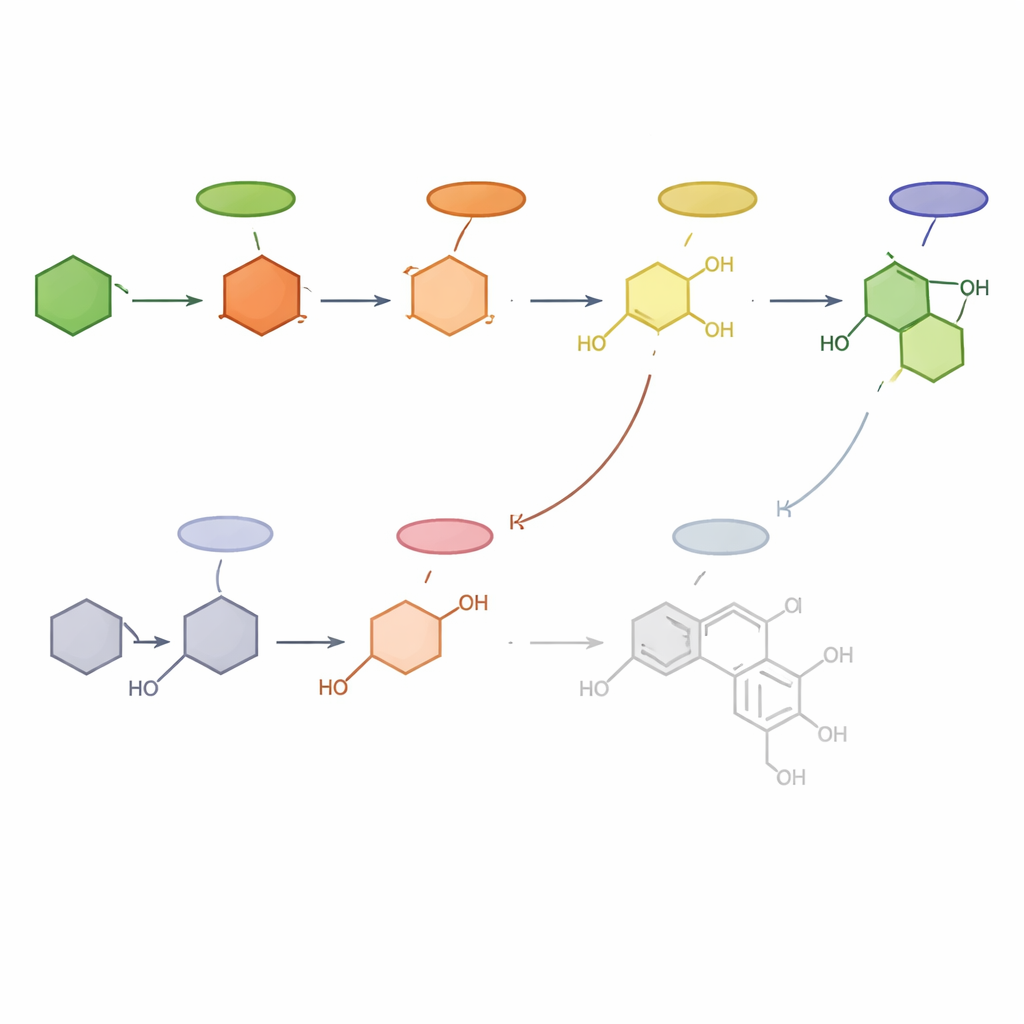
Tracer la nouvelle carte d’une voie sucrée
En combinant les empreintes chimiques et les profils d’activité génique, les chercheurs proposent un modèle de travail détaillé expliquant comment Hydrangea macrophylla fabrique la phyllodulcine. Selon eux, la voie débute avec la phénylalanine et passe par l’acide p‑coumarique, puis se ramifie en au moins trois itinéraires impliquant l’hydrangenol, le resvératrol et le thunberginol C, ce dernier servant probablement de précurseur direct final. Dans les variétés où les voies secondaires dominent, beaucoup moins de phyllodulcine est produite. Bien que certaines étapes restent hypothétiques, cette carte transforme un édulcorant traditionnel autrefois mystérieux en un produit biochimique bien défini. Pour un public non spécialiste, la conclusion est que comprendre cette usine naturelle au niveau moléculaire ouvre la voie à la sélection de variétés d’hortensias plus sucrées, à une production durable améliorée de phyllodulcine et à l’exploration plus ciblée de ses propriétés prometteuses pour la santé.
Citation: Padmakumar Sarala, G., Engel, F., Hartmann, A. et al. Elucidation and functional characterization of the biosynthetic pathway of the natural sweetener phyllodulcin in Hydrangea macrophylla. Sci Rep 16, 12044 (2026). https://doi.org/10.1038/s41598-026-47892-x
Mots-clés: édulcorants naturels, hortensia, métabolisme des plantes, phyllodulcine, voies biosynthétiques