Clear Sky Science · ru
Идентификация биомаркеров, связанных с путем NF-κB, при ишемии‑реперфузионном повреждении миокарда: на основе транскриптомного анализа и валидации RT-qPCR
Почему спасение сердечной мышцы всё ещё может причинять вред
Когда у человека происходит инфаркт, врачи спешат восстановить кровоток в закрытой артерии. Парадоксально, но возвращение крови само по себе может повредить сердце — это явление называется ишемо‑реперфузионным повреждением. В этом исследовании поставлен простой, но важный вопрос: можно ли обнаружить надежные молекулярные «лампочки‑предупреждения» внутри кардиомиоцитов, которые рано сигнализируют об этом повреждении и указывают на новые подходы к лечению? Объединив анализ больших наборов данных по генам с экспериментами на животных, авторы выделили два таких сигнала в рамках ключевого воспалительного пути.
Сердце под стрессом от потери и возвращения крови
Ишемо‑реперфузионное повреждение миокарда возникает, когда истощенная кислородом сердечная мышца внезапно снова получает кровь, например при восстановлении проходимости коронарной артерии или во время операций на сердце. Поступление кислорода может вызвать всплески вредных молекул, нарушить работу митохондрий и разжечь интенсивное воспаление. Лейкоциты устремляются в ткань сердца, мелкие сосуды закупориваются, а кардиомиоциты гибнут через несколько форм программируемой смерти. Эти процессы не только ограничивают восстановление функции сердца после лечения, но и повышают риск развития хронической сердечной недостаточности. Поскольку воспаление находится в центре этой бури, пути, контролирующие воспалительные сигналы, рассматриваются как главные подозреваемые и потенциальные цели терапии.
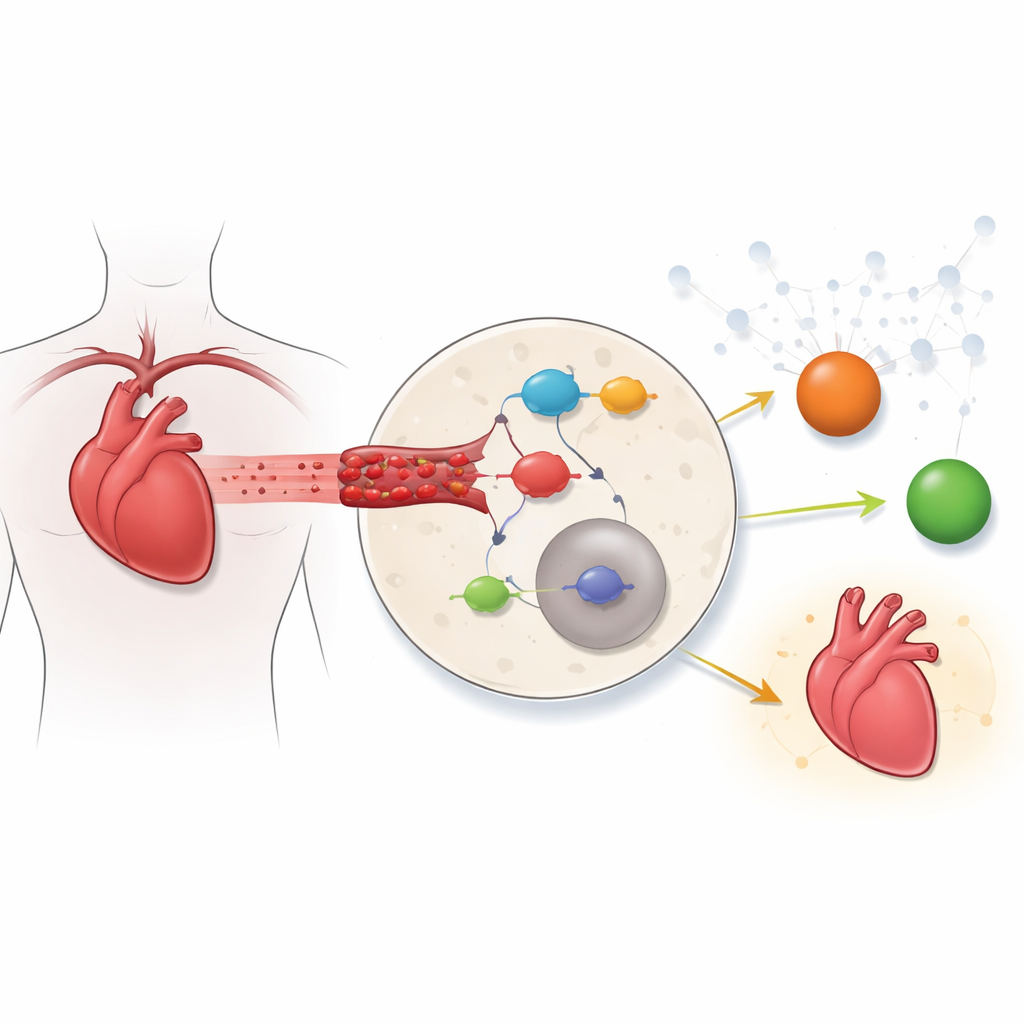
Ключевой переключатель воспаления внутри клеток сердца
Один из главных регуляторов воспаления в организме — путь NF‑κB, каскад белков, запускающий множество иммунных и защитных генов. В спокойных условиях NF‑κB удерживается в цитоплазме ингибиторным белком; при стрессe этот ингибитор удаляется, и NF‑κB перемещается в ядро, где активирует воспалительные программы. Ранее исследования сердца обычно рассматривали один‑два гена или препараты по отдельности. В этой работе авторы применили более глобальный подход: они объединили данные об активности генов из мышиных сердец с каталогом генов, связанных с NF‑κB, чтобы выяснить, какие компоненты этого пути наиболее резко меняются при ишемии‑реперфузии.
Две заметные молекулярные «лампочки‑предупреждения»
Из сотен изменённых генов только девять принадлежали к пути NF‑κB, и сетевой анализ выделил два из них как центральные игроки: Nfkbia и Icam1. Nfkbia кодирует ключевой «тормоз» для NF‑κB, тогда как Icam1 отвечает за клейкий белок на эндотелии сосудов и иммунных клетках, который помогает лейкоцитам прилипать и проникать в ткани. В двух независимых наборах данных у мышей оба гена стабильно проявляли повышенную активность после повреждения сердца по сравнению с контрольными образцами. Дополнительный анализ связал Icam1 с изменениями внеклеточного матрикса, а Nfkbia — с митохондриальной функцией, что указывает на то, что один ген больше отражает внешнюю среду и межклеточное взаимодействие, а другой — внутриклеточный энергетический баланс и стресс.
Скрытые РНК‑сети и возможный кандидат в лекарства
Углубившись в данные, команда построила карты возможной регуляции этих двух маркеров. Они предсказали транскрипционные факторы, включающие эти гены, а также сеть малых регуляторных РНК и более длинных «губчатых» РНК, которые могут тонко настраивать активность Icam1. Одна малая РНК, обозначенная mmu‑miR‑706, выделялась как потенциальный тормоз Icam1, на который сами могут влиять несколько длинных РНК, формируя регуляторную петлю, способную усиливать воспаление. Авторы затем сделали шаг от биологии к терапии: с помощью баз данных лекарств и молекулярного докинга они искали существующие соединения, которые могли бы связываться с NFKBIA и ICAM1. Одна молекула, ингибитор протеаз TLCK, в симуляциях показала плотное сродство к обоим белкам, что наводит на мысль, что она могла бы смягчать активацию пути NF‑κB и снижать «прилипание» лейкоцитов в повреждённом сердце.
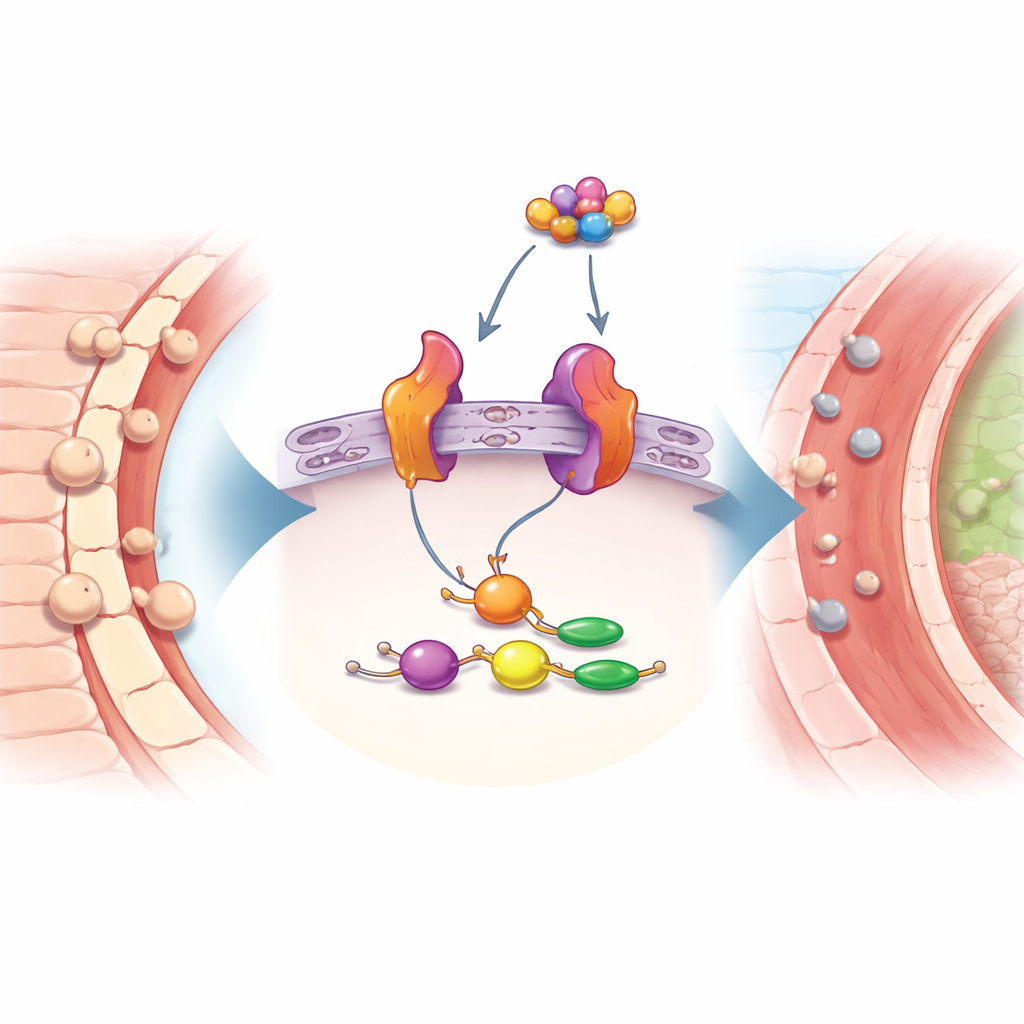
Эксперименты на мышах подтверждают сигнал
Чтобы убедиться, что обнаруженные изменения не являются артефактами вычислительного анализа, команда создала мышиную модель ишемии‑реперфузии, кратковременно пережимая и затем восстанавливая кровоток в коронарной артерии. Они измерили экспрессию генов в тканях сердца и обнаружили, что Nfkbia и Icam1 значительно повышены по сравнению с неповреждёнными контрольными образцами. Это экспериментальное подтверждение укрепляет позицию этих генов как надежных маркеров процесса повреждения, а не случайных флуктуаций экспрессии.
Что это означает для будущей помощи при сердечных заболеваниях
Для широкой аудитории главная мысль такова: исследование выделяет два молекулярных индикатора, которые действуют как приборные лампы при воспалительном повреждении, возникающем после восстановления кровотока в сердце. Nfkbia показывает, насколько интенсивно клетка старается сдерживать мощный воспалительный переключатель, а Icam1 отражает, насколько активно в ткань сердца привлекаются иммунные клетки. Хотя предстоит ещё много работы — особенно чтобы проверить, могут ли таргетирование этих молекул или применение TLCK безопасно защитить сердце человека — это исследование даёт более чёткую карту процесса повреждения и новые отправные точки для разработки препаратов, которые сделают спасительное реперфузионное лечение более безопасным и эффективным.
Цитирование: Ting, W., Helong, X., Xiaoyu, W. et al. Identification of NF-κB pathway-related biomarkers in myocardial ischemia-reperfusion injury: based on transcriptomics analysis and RT-qPCR validation. Sci Rep 16, 11729 (2026). https://doi.org/10.1038/s41598-026-47878-9
Ключевые слова: реперфузионное повреждение сердца, воспаление NF-kappaB, кардиальные биомаркеры, анализ экспрессии генов, ICAM1 и NFKBIA