Clear Sky Science · it
Identificazione di biomarcatori correlati alla via NF-κB nel danno da ischemia‑riperfusione miocardica: basato su analisi trascrittomica e validazione RT-qPCR
Perché salvare il muscolo cardiaco può comunque causare danni
Quando qualcuno subisce un infarto, i medici corrono per riaprire l’arteria bloccata. Ironia della sorte, il ripristino del flusso sanguigno può di per sé danneggiare il cuore, un problema noto come danno da ischemia‑riperfusione. Questo studio pone una domanda semplice ma importante: è possibile individuare segnali molecolari affidabili all’interno delle cellule cardiache che segnalino precocemente questo danno e indichino nuove terapie? Combinando l’analisi di grandi serie di dati genici con esperimenti su animali, i ricercatori hanno individuato due segnali di questo tipo all’interno di una principale via infiammatoria.
Il cuore sotto stress per la perdita e il ritorno del sangue
Il danno da ischemia‑riperfusione miocardica si verifica quando un muscolo cardiaco privato di ossigeno riceve di nuovo sangue, ad esempio durante l’apertura di un’arteria coronaria ostruita o un intervento cardiaco. Il brusco afflusso di ossigeno può innescare ondate di molecole dannose, disturbare i mitocondri che producono energia e scatenare un’infiammazione intensa. I globuli bianchi invadono il tessuto cardiaco, i piccoli vasi si intasano e le cellule miocardiche muoiono attraverso diverse forme di morte cellulare programmata. Questi eventi non solo limitano la quantità di funzione cardiaca recuperabile dopo il trattamento, ma aumentano anche il rischio di insufficienza cardiaca a lungo termine. Poiché l’infiammazione è al centro di questa tempesta, le vie che regolano i segnali infiammatori sono sospettate e considerate bersagli privilegiati.
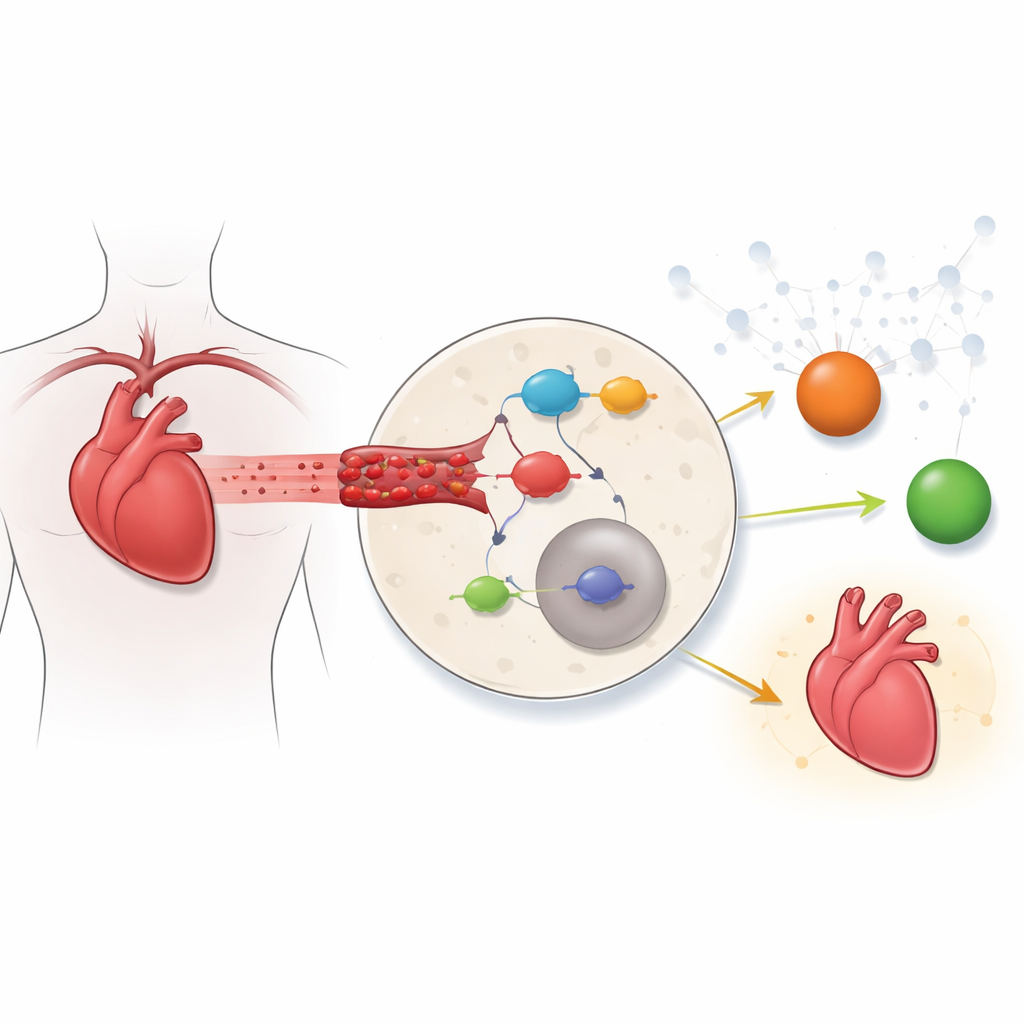
Un interruttore chiave dell’infiammazione nelle cellule cardiache
Una delle centrali dell’infiammazione nell’organismo è la via NF‑κB, una catena di proteine che attiva molti geni immunitari e di sopravvivenza. In condizioni di quiete, NF‑κB è tenuta sotto controllo nel citoplasma da una proteina inibitrice; sotto stress, quell’inibitore viene rimosso e NF‑κB si sposta nel nucleo per attivare programmi infiammatori. Studi cardiaci precedenti hanno spesso esaminato uno o due geni o farmaci alla volta. Qui, gli autori hanno adottato una visione più globale. Hanno fuso i dati di attività genica da cuori di topo con un catalogo di geni correlati a NF‑κB per vedere quali membri di questa via cambiavano in modo più marcato durante l’ischemia‑riperfusione.
Due segnali molecolari che emergono
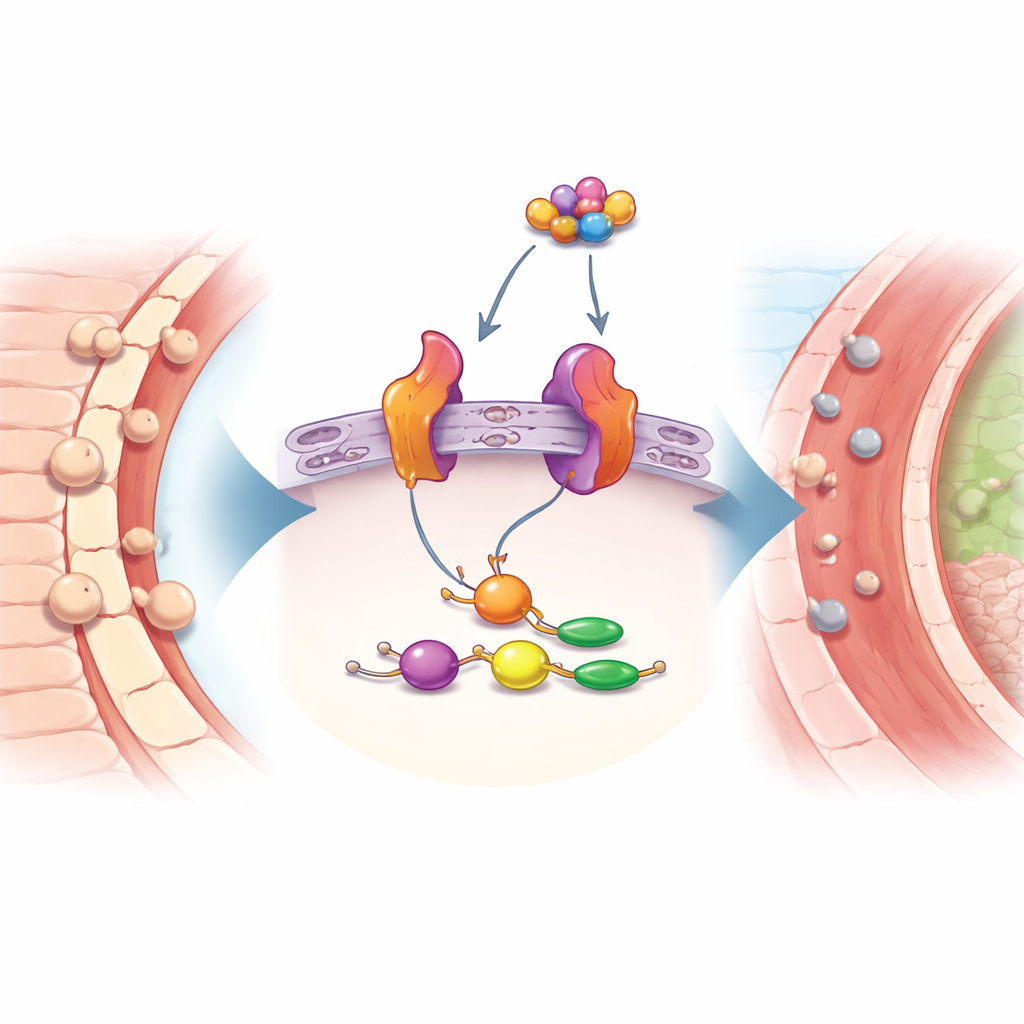
Da centinaia di geni alterati, solo nove appartenevano alla via NF‑κB, e l’analisi di rete ha evidenziato due di essi come protagonisti centrali: Nfkbia e Icam1. Nfkbia codifica per il freno chiave di NF‑κB, mentre Icam1 produce una proteina adesiva sulle cellule dei vasi e sulle cellule immunitarie che facilita l’adesione e l’ingresso dei globuli bianchi nei tessuti. In due dataset indipendenti di topi, entrambi i geni risultavano costantemente più attivi dopo il danno cardiaco rispetto ai cuori di controllo. Un’ulteriore analisi ha collegato Icam1 a cambiamenti nella matrice extracellulare attorno alle cellule, e Nfkbia ai piccoli “impianti” energetici intracellulari, suggerendo che il primo sia più legato all’ambiente esterno e alle interazioni cellula‑cellula, mentre il secondo sia più connesso all’equilibrio energetico e allo stress interno alla cellula.
Circuiti nascosti di RNA e un possibile candidato farmaco
Approfondendo, il gruppo ha mappato come altre molecole potrebbero regolare questi due marker. Hanno previsto fattori di trascrizione che attivano questi geni, oltre a una rete di piccoli RNA regolatori e più lunghi RNA “spugna” che potrebbero modulare finemente l’attività di Icam1. Un piccolo RNA, denominato mmu‑miR‑706, è emerso come possibile freno di Icam1 che a sua volta potrebbe essere bloccato da diversi RNA lunghi, formando un circuito regolatorio in grado di amplificare l’infiammazione. I ricercatori hanno poi compiuto un passo dalla biologia verso la terapia: usando banche dati farmaco‑gene e docking computazionale, hanno cercato composti esistenti in grado di legare sia NFKBIA sia ICAM1. Una molecola, l’inibitore delle proteasi TLCK, sembrava attaccarsi bene a entrambe le proteine nelle simulazioni, suggerendo che potrebbe calmare la via NF‑κB e ridurre l’adesione dei globuli bianchi nel cuore lesionato.
Esperimenti sui topi confermano il segnale
Per assicurarsi che queste variazioni non fossero solo artefatti dell’analisi computazionale, il gruppo ha creato un modello murino di ischemia‑riperfusione, legando brevemente e poi riaprendo un’arteria cardiaca. Hanno misurato l’attività genica nel tessuto cardiaco e hanno riscontrato che Nfkbia e Icam1 risultavano entrambe chiaramente elevate rispetto ai cuori di controllo non lesionati. Questa conferma sperimentale rafforza l’ipotesi che questi geni siano marcatori robusti del processo di danno piuttosto che fluttuazioni casuali nell’espressione genica.
Cosa significa per la cura del cuore in futuro
Per i non specialisti, il messaggio principale è che lo studio identifica due molecole che funzionano come spie sul cruscotto per il danno guidato dall’infiammazione quando il flusso sanguigno ritorna al cuore. Nfkbia riflette quanto la cellula stia lavorando per tenere sotto controllo un potente interruttore infiammatorio, mentre Icam1 riflette quanto vigorosamente le cellule immunitarie vengano richiamate nel tessuto cardiaco. Sebbene rimanga molto lavoro da fare — specialmente per verificare se mirare a queste molecole o a TLCK possa proteggere in modo sicuro i cuori umani — questa ricerca offre una mappa più chiara del processo di danno e nuovi punti di partenza per farmaci che potrebbero rendere le terapie di riperfusione salvavita più sicure ed efficaci.
Citazione: Ting, W., Helong, X., Xiaoyu, W. et al. Identification of NF-κB pathway-related biomarkers in myocardial ischemia-reperfusion injury: based on transcriptomics analysis and RT-qPCR validation. Sci Rep 16, 11729 (2026). https://doi.org/10.1038/s41598-026-47878-9
Parole chiave: danno da riperfusione cardiaca, infiammazione NF-kappaB, biomarcatori cardiaci, analisi dell'espressione genica, ICAM1 e NFKBIA