Clear Sky Science · de
Identifizierung NF-κB-Signalwegs-assoziierter Biomarker bei ischämisch-reperfusionsbedingter Myokardschädigung: basierend auf Transkriptom-Analyse und RT-qPCR-Validierung
Warum das Retten von Herzmuskel dennoch schaden kann
Wenn jemand einen Herzinfarkt erleidet, kämpfen Ärztinnen und Ärzte darum, die verschlossene Arterie wieder zu eröffnen. Ironischerweise kann die Wiederherstellung des Blutflusses selbst das Herz schädigen — ein Problem, das als Ischämie‑Reperfusionsschaden bezeichnet wird. Diese Studie stellt eine einfache, aber wichtige Frage: Lassen sich verlässliche molekulare Warnsignale in Herzmuskelzellen finden, die diesen Schaden früh ankündigen und auf neue Behandlungsansätze hinweisen? Durch die Kombination von groß angelegter Genanalyse und Tierversuchen konzentrierten sich die Forschenden auf zwei solche Signale innerhalb eines zentralen Entzündungswegs.
Herz unter Stress durch Verlust und Rückkehr von Blut
Myokardiale Ischämie‑Reperfusionsschädigung tritt auf, wenn ein unterversorgter Herzmuskel während Eingriffen wie der Öffnung einer verstopften Koronararterie oder einer Herzoperation plötzlich wieder durchblutet wird. Der plötzliche Sauerstoffzufluss kann schädliche Molekülschübe auslösen, die Energie produzierenden Mitochondrien stören und heftige Entzündungsreaktionen entfachen. Weiße Blutkörperchen strömen ins Herzgewebe, kleine Gefäße verstopfen, und Herzmuskelzellen sterben durch verschiedene Formen programmierten Zelltods. Diese Ereignisse begrenzen nicht nur, wie viel Herzfunktion nach der Behandlung wiederhergestellt werden kann, sondern erhöhen auch das Risiko für langfristige Herzinsuffizienz. Da die Entzündung im Zentrum dieses Geschehens steht, sind Signalwege, die Entzündungsreaktionen steuern, besonders verdächtig und zugleich potenzielle Therapieziele.
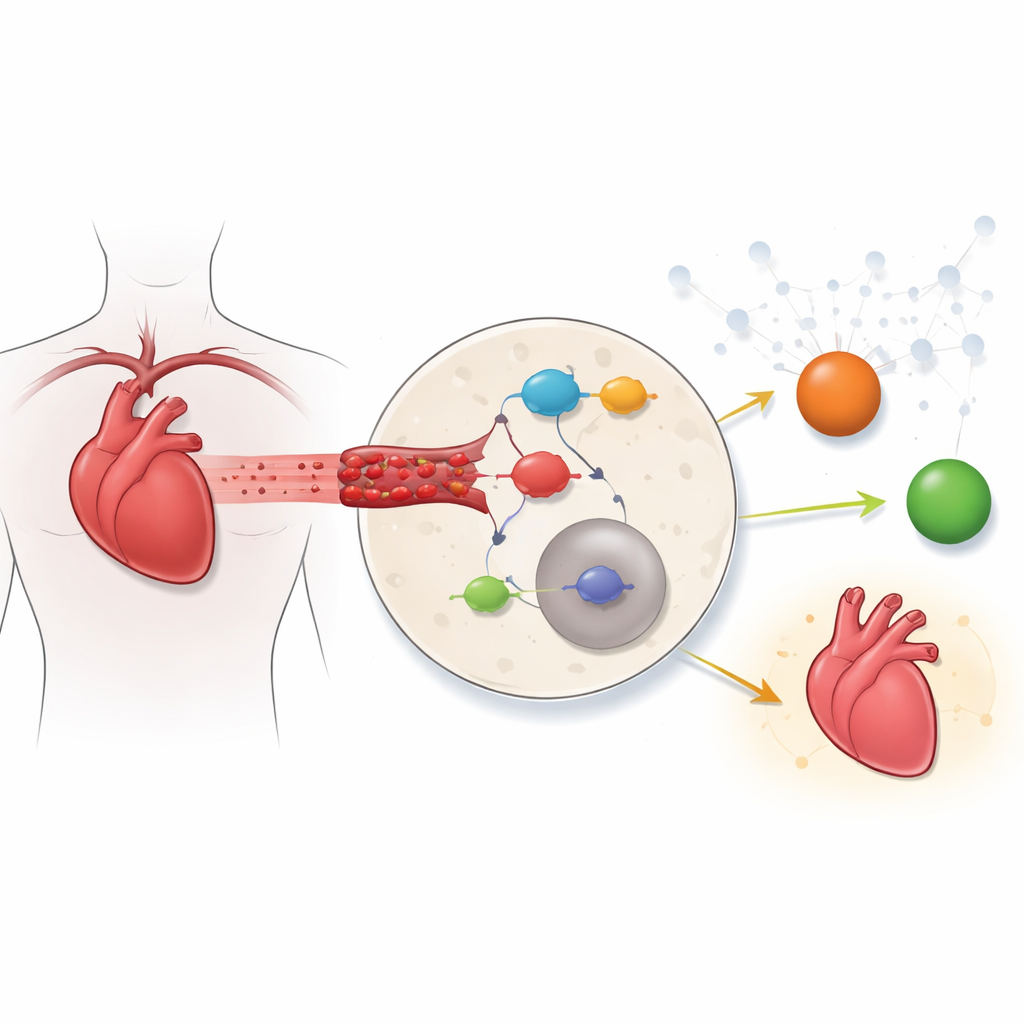
Ein wichtiger Entzündungsschalter in Herzmuskelzellen
Einer der zentralen Schalter für Entzündungen im Körper ist der NF‑κB-Signalweg, eine Kaskade von Proteinen, die zahlreiche Immun‑ und Überlebensgene aktiviert. Unter ruhigen Bedingungen wird NF‑κB im Zellplasma durch ein Inhibitorprotein in Schach gehalten; unter Stress wird dieser Inhibitor entfernt und NF‑κB wandert in den Zellkern, um entzündliche Programme zu starten. Frühere Herzstudien untersuchten meist nur ein oder zwei Gene oder Wirkstoffe gleichzeitig. Hier nahmen die Autorinnen und Autoren eine globalere Perspektive ein. Sie kombinierten Genaktivitätsdaten aus Maus-Herzen mit einem Katalog NF‑κB‑bezogener Gene, um zu sehen, welche Mitglieder dieses Wegs sich während der Ischämie‑Reperfusion am stärksten veränderten.
Zwei herausragende molekulare Warnsignale
Aus Hunderten veränderter Gene gehörten nur neun zum NF‑κB‑Signalweg, und Netzwerk‑Analysen hoben zwei davon als zentrale Akteure hervor: Nfkbia und Icam1. Nfkbia kodiert die Schlüsselbremse für NF‑κB, während Icam1 ein klebriges Protein auf Gefäß- und Immunzellen produziert, das weißen Blutkörperchen das Anhaften und Eindringen ins Gewebe erleichtert. In zwei unabhängigen Mausdatensätzen waren beide Gene nach der Herzverletzung konsistent stärker aktiv als in Kontrollherzen. Weitere Analysen verknüpften Icam1 mit Veränderungen in der extrazellulären Matrix und Nfkbia mit den kleinen Kraftwerken in der Zelle, was darauf hindeutet, dass das eine eher mit der äußeren Umgebung und Zell‑zu‑Zell‑Interaktionen assoziiert ist, das andere mit Energiegleichgewicht und intrazellulärem Stress.
Versteckte RNA‑Schaltkreise und ein möglicher Wirkstoffkandidat
Tiefergehende Untersuchungen kartierten, wie andere Moleküle diese beiden Marker regulieren könnten. Die Forschenden sagten Transkriptionsfaktoren voraus, die diese Gene einschalten, sowie ein Netz aus kleinen regulatorischen RNAs und längeren "Sponge"‑RNAs, die die Icam1‑Aktivität feinabstimmen könnten. Eine kleine RNA, genannt mmu‑miR‑706, fiel als potenzielle Bremse für Icam1 auf, die ihrerseits durch mehrere lange RNAs blockiert werden könnte und so einen Regulationskreis bilden würde, der Entzündungen verstärken kann. Anschließend bewegte sich das Team von der Biologie in Richtung Therapie: Mit Hilfe von Wirkstoff‑Gen-Datenbanken und computergestütztem Docking suchten sie nach vorhandenen Verbindungen, die sowohl an NFKBIA als auch an ICAM1 binden könnten. Ein Molekül, der Proteaseinhibitor TLCK, schien in Simulationen an beide Proteine gut zu binden, was darauf hindeutet, dass es den NF‑κB‑Weg beruhigen und das Anhaften weißer Blutkörperchen im verletzten Herzen reduzieren könnte.
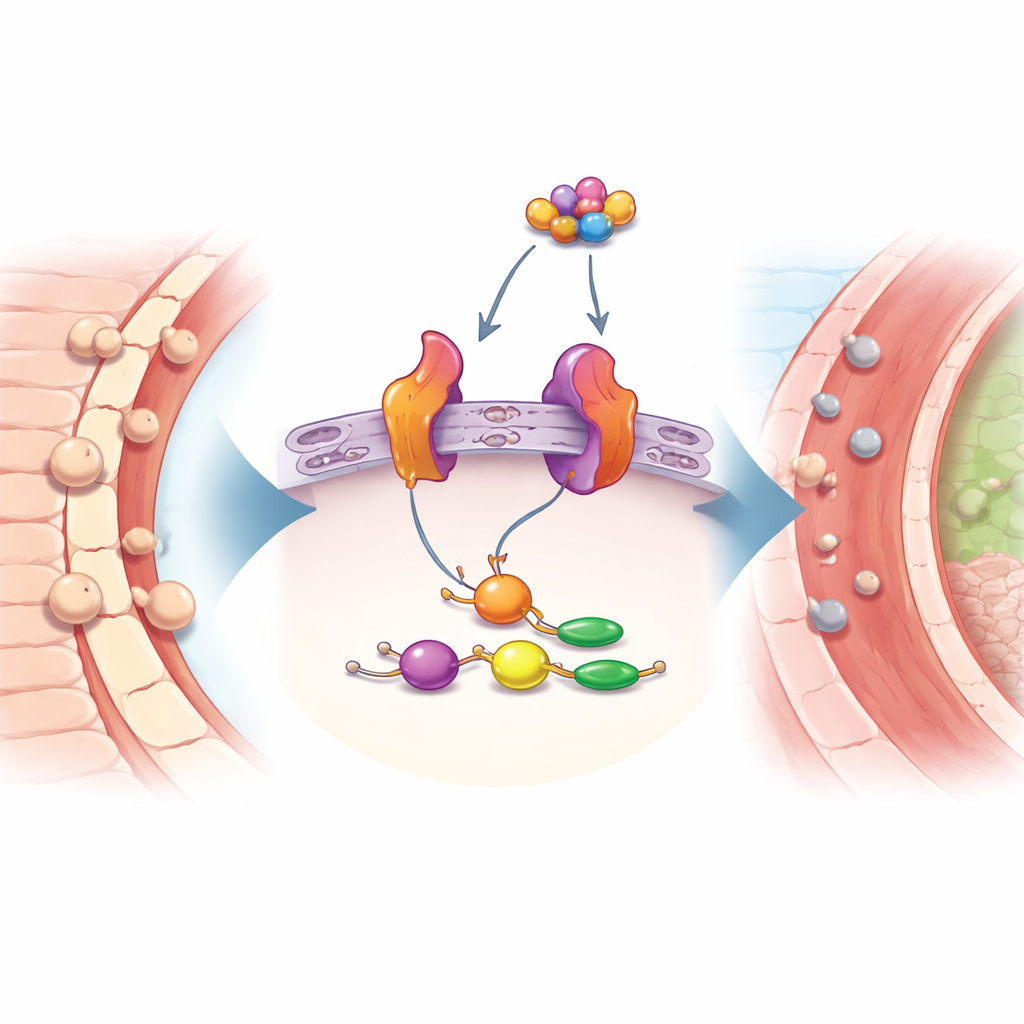
Mausversuche bestätigen das Signal
Um sicherzustellen, dass diese Veränderungen keine bloßen Artefakte der Computeranalyse waren, erzeugte das Team ein Mausmodell der Ischämie‑Reperfusion, bei dem eine Herzarterie kurz abgeklemmt und dann wieder eröffnet wurde. Sie maßen die Genaktivität im Herzgewebe und fanden, dass Nfkbia und Icam1 in den verletzten Herzen deutlich erhöht waren im Vergleich zu unverletzten Kontrollherzen. Diese experimentelle Bestätigung stärkt die Auffassung, dass es sich bei diesen Genen um robuste Marker des Verletzungsprozesses handelt und nicht um zufällige Schwankungen der Genaktivität.
Was das für die künftige Herzversorgung bedeutet
Für Nicht‑Spezialisten lautet die Kernaussage: Die Studie identifiziert zwei Moleküle, die wie Kontrollleuchten auf dem Armaturenbrett für entzündungsgetriebene Schäden wirken, wenn die Durchblutung zum Herzen wiederhergestellt wird. Nfkbia spiegelt wider, wie sehr die Zelle daran arbeitet, einen mächtigen Entzündungsschalter unter Kontrolle zu halten, während Icam1 anzeigt, wie stark Immunzellen ins Herzgewebe rekrutiert werden. Obwohl noch viel Arbeit nötig ist — insbesondere um zu prüfen, ob das Ansteuern dieser Moleküle oder von TLCK menschliche Herzen sicher schützen kann — liefert diese Forschung eine klarere Landkarte des Verletzungsprozesses und neue Ansatzpunkte für Medikamente, die lebensrettende Reperfusionsmaßnahmen sicherer und wirkungsvoller machen könnten.
Zitation: Ting, W., Helong, X., Xiaoyu, W. et al. Identification of NF-κB pathway-related biomarkers in myocardial ischemia-reperfusion injury: based on transcriptomics analysis and RT-qPCR validation. Sci Rep 16, 11729 (2026). https://doi.org/10.1038/s41598-026-47878-9
Schlüsselwörter: Herz-Reperfusionsschaden, NF-kappaB-Entzündung, kardiale Biomarker, Genexpressionsanalyse, ICAM1 und NFKBIA