Clear Sky Science · ru
Опухоле-специфическая терапия цитокинами, опосредованная инженерной Salmonella с синтетической системой доставки белков
Преобразование микробов в борцов с раком
Онкологи давно знают, что некоторые иммуностимулирующие препараты — цитокины — помогают организму атаковать опухоли, но они настолько мощные, что часто повреждают и здоровые ткани. Это исследование рассматривает необычный способ обхода проблемы: использование ослабленной формы бактерии Salmonella в роли крошечного транспортного средства, которое проникает в опухоли и высвобождает сконструированный иммунный сигнал только там, где он нужен, с целью усилить локальную защиту и пощадить остальной организм.
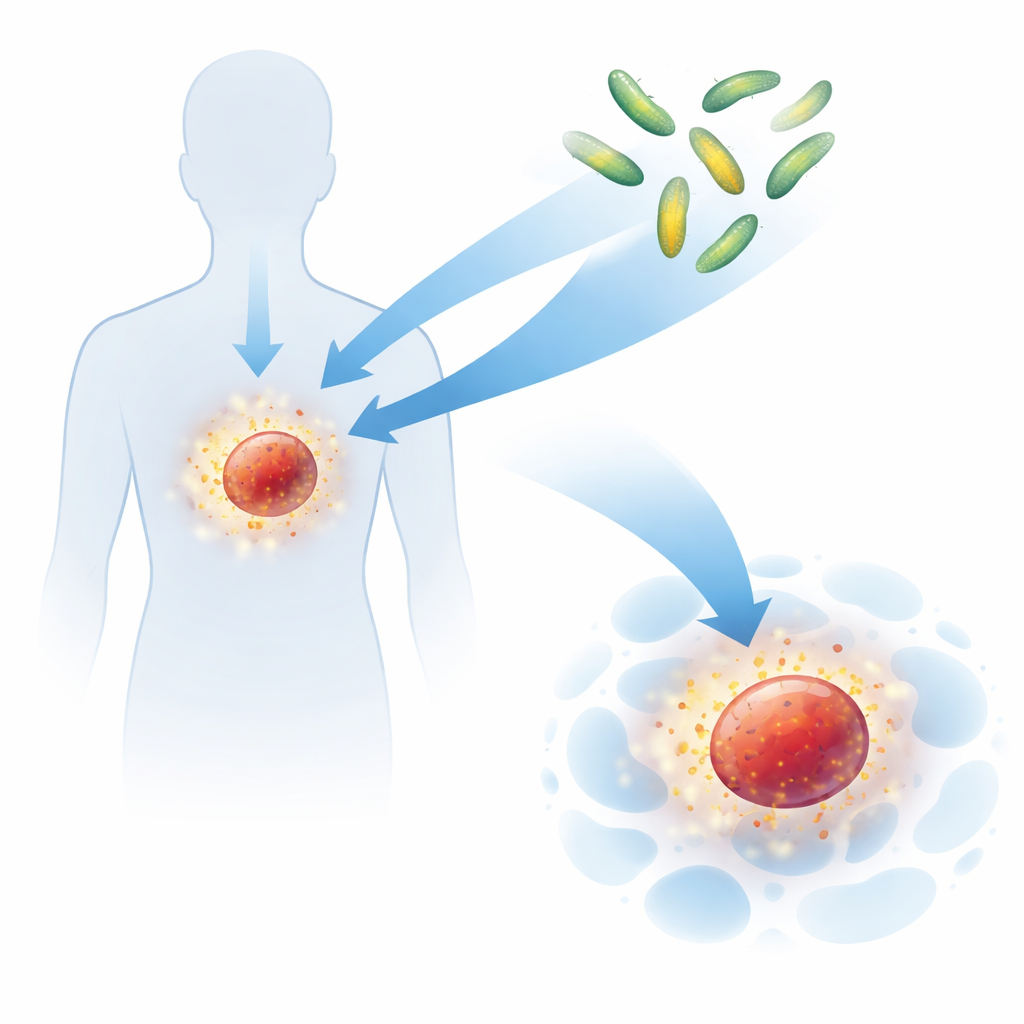
Почему существующие иммунные сигналы трудно использовать
Цитокины действуют как молекулярные текстовые сообщения, сообщая иммунным клеткам, когда отдыхать, а когда сражаться. Препараты на основе природных цитокинов, таких как интерлейкин‑2 и интерлейкин‑15, могут сильно активировать Т‑клетки и натуральные киллеры, убивающие рак, но у них есть серьёзные недостатки: они распространяются по всему телу, вызывают опасные побочные эффекты и быстро разрушаются в крови. Новый, созданный с помощью вычислений цитокин Neoleukin‑2/15 разработан так, чтобы сохранять полезный эффект — пробуждение клеток, борющихся с раком — и при этом избегать путей, включающих подавляющие иммунные клетки. В экспериментах на мышах этот дизайнерский белок работал хорошо, но в клинических испытаниях на людях он всё ещё вызывал побочные эффекты вне целевой зоны, что говорит о том, что проблема заключается не только в самой молекуле, но и в месте и способе её доставки.
Привлечение бактерий, которые естественно направляются в опухоли
Некоторые бактерии естественно предпочитают суровую, бедную кислородом среду внутри опухолей и склонны размножаться там, тогда как из здоровых органов они выводятся. Исследователи воспользовались этим поведением, работая с Salmonella — бактерией, которую можно генетически укротить, чтобы она больше не вторгалась и не повреждала нормальные ткани. Они удалили два ключевых участка генома, которые обычно позволяют Salmonella внедряться в клетки хозяина, создав сильно ослабленную штамм, который тем не менее мигрирует в опухоли. В этот штамм ввели тщательно сконструированную систему экспорта белков и отдельный набор генов, кодирующих дизайнерский цитокин Neo‑2/15, превратив каждую бактерию в управляемую фабрику по производству и высвобождению иммуностимулирующего белка непосредственно в ткани опухоли.
Создание переключаемой машины для доставки белков
Чтобы переместить Neo‑2/15 из бактериальной клетки во внеклеточное пространство опухоли, команда перенастроила молекулярный шприц, который Salmonella обычно использует при инфицировании, известный как система секреции типа 3. Они уместили десятки генов на одну плазмиду — кольцевой фрагмент ДНК — так, чтобы всю машину секреции можно было включить при помощи распространённого антибиотика доксициклина. Короткая «метка» белка из природного белка Salmonella была слита с Neo‑2/15, так что при индукции система выталкивала этот меченый цитокин во внеклеточную жидкость. В лабораторных испытаниях добавление доксициклина вызывало стабильную секрецию белкового фьюжна без гибели бактерий, а стандартные биохимические анализы подтвердили наличие выделенного продукта в измеримых количествах и сохранение ожидаемого размера и структуры.
Доказательство того, что дизайнерский сигнал по‑прежнему работает
Высвобождение цитокина имеет смысл только в том случае, если он всё ещё «говорит» с иммунными клетками на нужном языке. Команда проверила это, подвергнув культуру Т‑клеточной линии мыши, которая обычно зависит от цитокинов для выживания и размножения, воздействию бактериальной жидкости, содержащей секретированный фьюжн Neo‑2/15. После концентрирования этой жидкости до биологически релевантных доз исследователи обнаружили, что Т‑клетки росли почти так же хорошо, как в присутствии стандартного интерлейкина‑2 или очищенного Neo‑2/15, произведённого более традиционным способом. Даже когда точное количество цитокина в жидкости было невелико, сочетание дизайнерского сигнала и других бактериальных компонентов всё равно повышало число Т‑клеток, показывая, что фьюжн‑белок оставался функциональным после секреции.
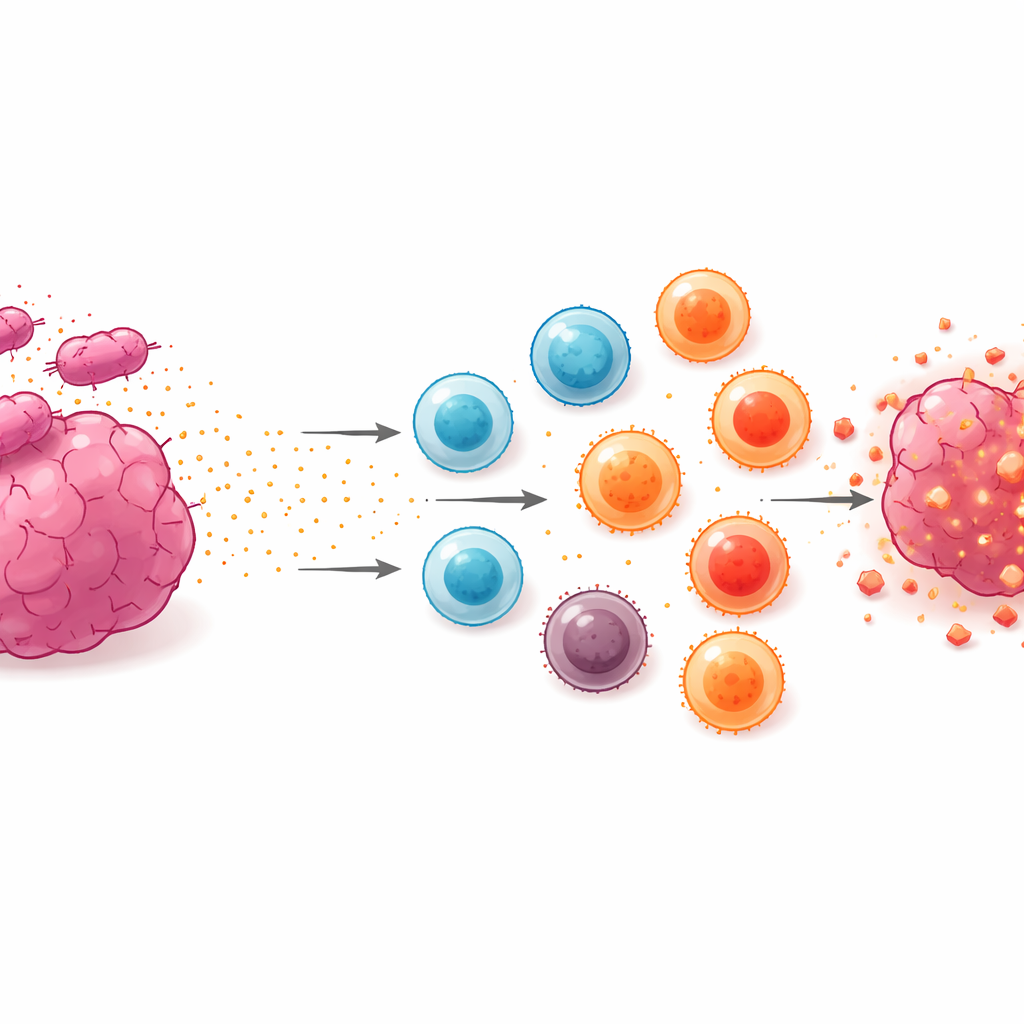
Замедление роста опухолей и увеличение выживаемости у мышей
Ключевой проверкой было то, поможет ли эта бактериальная стратегия доставки животным бороться с раком. Мышам имплантировали клетки колоректального рака и, после формирования опухолей, вводили ослабленную Salmonella, несущую систему секреции и груз Neo‑2/15. Когда переключатель доксициклина оставался выключенным, опухоли продолжали расти, хотя мыши жили немного дольше, чем нетронутые контрольные животные — вероятно, потому что часть цитокина просочилась наружу по мере гибели бактерий внутри опухоли. Когда переключатель включали и секреция полностью активировалась, рост опухолей замедлялся заметно, а лечёные мыши выживали примерно вдвое дольше по сравнению с нелечеными животными, при этом в анализах крови не наблюдалось очевидных повреждений печени или почек. Преимущество не привело к полному излечению, отчасти потому, что одна из плазмид, несущих машину секреции, со временем терялась внутри организма, что ограничивало длительность высокого уровня выделения цитокина.
Что это может значить для будущего онкологической помощи
Работа показывает, что живые ослабленные бактерии могут быть перепрограммированы в программируемых курьеров, которые доставляют мощные иммуностимулирующие белки прямо в опухоли, активируя локальную защиту и ограничивая воздействие на весь организм. Хотя лечёные мыши не были полностью излечены, подход замедлил рост опухолей и продлил жизнь без значительной токсичности, что указывает на то, что дальнейшие усовершенствования — например, повышение стабильности системы доставки или сочетание с другими методами лечения — могут сделать его более эффективным. Для неспециалистов основной вывод таков: микробы, ранее известные лишь как враги, вскоре могут быть использованы как точные инструменты, направляя собственную иммунную систему организма против рака более целенаправленным способом.
Цитирование: Ha, J., Song, M. Tumor-specific cytokine therapy mediated by engineered Salmonella with a synthetic protein delivery system. Sci Rep 16, 14240 (2026). https://doi.org/10.1038/s41598-026-44265-2
Ключевые слова: бактериальная терапия рака, нацеленная доставка цитокинов в опухоль, инженерная Salmonella, иммунотерапия рака, синтетическая секреция белков