Clear Sky Science · de
Tumorspezifische Zytokintherapie vermittelt durch gentechnisch veränderte Salmonellen mit einem synthetischen Protein‑Auslieferungssystem
Aus Krankheitserregern werden Krebsbekämpfer
Krebsärzte wissen seit langem, dass bestimmte immunstärkende Wirkstoffe, sogenannte Zytokine, dem Körper helfen können, Tumore anzugreifen. Sie sind jedoch so wirkstark, dass sie häufig auch gesundes Gewebe schädigen. Diese Studie untersucht einen ungewöhnlichen Lösungsansatz: eine abgeschwächte Form des lebensmittelbedingten Krankheitserregers Salmonella als winziges Transportmittel zu nutzen, das in Tumore eindringt und dort ein designtes Immunsignal freisetzt — genau dort, wo es gebraucht wird — mit dem Ziel, die lokale Abwehr zu stärken und den Rest des Körpers zu schonen.
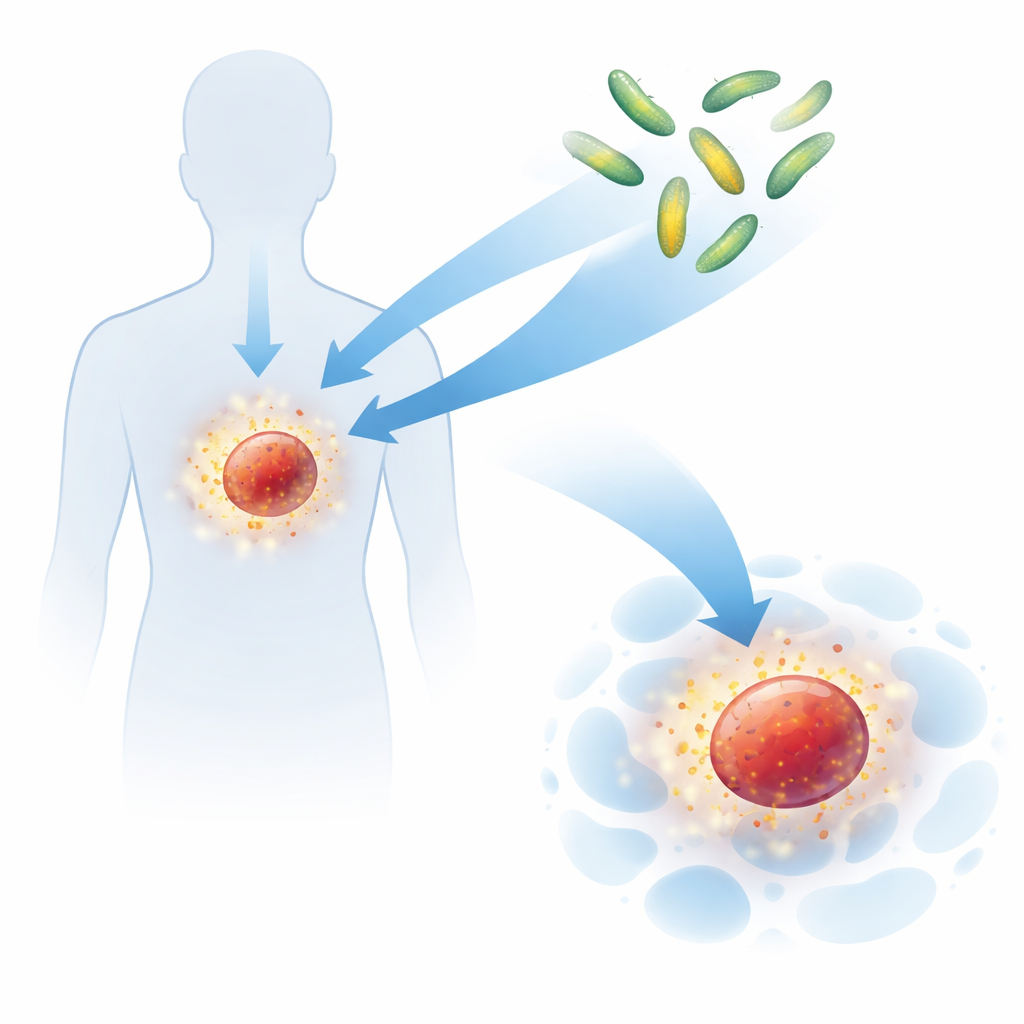
Warum bestehende Immunsignale schwer nutzbar sind
Zytokine funktionieren wie molekulare Textnachrichten, die Immunzellen sagen, wann sie ruhen und wann sie kämpfen sollen. Wirkstoffe, die auf natürlichen Zytokinen wie Interleukin‑2 und Interleukin‑15 basieren, können T‑Zellen und natürliche Killerzellen stark aktivieren, haben aber schwere Nachteile: Sie zirkulieren im gesamten Körper, verursachen gefährliche Nebenwirkungen und bauen sich im Blut schnell ab. Ein neuer, rechnerisch entworfenes Zytokin namens Neoleukin‑2/15 wurde entwickelt, um die guten Effekte — das Aufwecken krebsbekämpfender Zellen — zu erhalten und zugleich Wege zu vermeiden, die unterdrückende Immunzellen aktivieren. Im Mausmodell funktionierte dieses Designer‑Protein gut, in klinischen Studien mit Menschen traten jedoch weiterhin unerwünschte Effekte auf. Das deutet darauf hin, dass das eigentliche Problem nicht nur das Molekül selbst ist, sondern auch, wo und wie es verabreicht wird.
Gewinnen von Bakterien, die natürlicherweise Tumoren ansteuern
Bestimmte Bakterien bevorzugen natürlicherweise die rauen, sauerstoffarmen Bedingungen innerhalb von Tumoren und vermehren sich dort, während sie aus gesunden Organen eliminiert werden. Die Forscher nutzten dieses Verhalten, indem sie mit Salmonella arbeiteten — einem Bakterium, das genetisch so gezähmt werden kann, dass es nicht mehr in normales Gewebe eindringt oder es schädigt. Sie entfernten zwei wichtige genetische Regionen, die Salmonella normalerweise das Eindringen in Wirtszellen ermöglichen, und schufen so einen stark abgeschwächten Stamm, der trotzdem zu Tumoren migriert. In diesen Stamm brachten sie ein sorgfältig konstruiertes Protein‑Export‑System und zusätzlich ein Genpaket für das Designer‑Zytokin Neo‑2/15 ein, wodurch jedes Bakterium zu einer kontrollierbaren Fabrik wurde, die das immunstimulierende Protein direkt im Tumorgewebe produziert und freisetzt.
Aufbau einer schaltbaren Proteinauslieferungsmaschine
Um Neo‑2/15 aus der Bakterienzelle in die Tumorumgebung zu transportieren, programmierte das Team eine molekulare Spritze um, die Salmonella normalerweise während einer Infektion verwendet, bekannt als Typ‑3‑Sekretionssystem. Sie kompaktierten Dutzende von Genen auf ein einzelnes Plasmid — ein ringförmiges DNA‑Stück — sodass die gesamte Sekretionsmaschine durch ein übliches Antibiotikum, Doxycyclin, ein‑ und ausgeschaltet werden konnte. Ein kurzes Protein‑“Tag” aus einem natürlichen Salmonella‑Protein wurde an Neo‑2/15 gekoppelt, sodass bei Induktion die Bakterien dieses getaggte Zytokin in die umgebende Flüssigkeit pumpten. In Labortests löste die Zugabe von Doxycyclin eine kontinuierliche Sekretion des Fusionsproteins aus, ohne die Bakterien abzutöten, und Standard‑biochemische Tests bestätigten, dass das freigesetzte Produkt in messbaren Mengen vorlag und die erwartete Größe sowie Struktur beibehielt.
Nachweis, dass das Designer‑Signal weiterhin wirkt
Die Freisetzung eines Zytokins ist nur dann nützlich, wenn es Immunzellen noch in der richtigen Sprache anspricht. Das Team prüfte dies, indem es eine Maus‑T‑Zelllinie, die normalerweise auf Zytokine zum Überleben und zur Proliferation angewiesen ist, der bakteriellen Kulturflüssigkeit mit dem sezernierten Neo‑2/15‑Fusionsprotein aussetzte. Nach Konzentrierung dieser Flüssigkeit auf biologisch relevante Dosen wuchsen die T‑Zellen nahezu genauso gut wie in Gegenwart von Standard‑Interleukin‑2 oder gereinigtem, auf konventionellem Wege hergestelltem Neo‑2/15. Selbst wenn die exakte Zytokinmenge in der Flüssigkeit gering war, erhöhte die Kombination aus dem Designer‑Signal und anderen bakteriellen Komponenten noch die T‑Zellzahlen, was zeigt, dass das Fusionsprotein nach der Sekretion funktional blieb.
Verlangsamung von Tumoren und verlängertes Überleben bei Mäusen
Die entscheidende Prüfung war, ob diese bakterielle Lieferstrategie Tieren helfen konnte, Krebs zu bekämpfen. Mäusen wurden Kolonkrebsgeschwulste eingesetzt und, nachdem Tumore entstanden waren, mit den abgeschwächten Salmonellen injiziert, die das Sekretionssystem und die Neo‑2/15‑Fracht trugen. War der Doxycyclin‑Schalter ausgeschaltet, wuchsen die Tumore weiter, wobei die Tiere jedoch geringfügig länger lebten als unbehandete Kontrollen — vermutlich weil beim Absterben einiger Bakterien im Tumor etwas Zytokin freigesetzt wurde. Wurde der Schalter aktiviert und die Sekretion vollständig eingeschaltet, verlangsamte sich das Tumorwachstum deutlich und die behandelten Mäuse überlebten etwa doppelt so lang wie unbehandelte Tiere, ohne dass Bluttests offensichtliche Leber‑ oder Nierenschäden zeigten. Der Nutzen war keine vollständige Heilung, zum Teil weil eines der Plasmide, das die Sekretionsmaschinerie trug, im Körper im Laufe der Zeit allmählich verloren ging, was die Dauer einer hochgradigen Zytokinfreisetzung begrenzte.
Was das für die zukünftige Krebsversorgung bedeuten könnte
Diese Arbeit zeigt, dass lebende, abgeschwächte Bakterien so umprogrammiert werden können, dass sie als steuerbare Kuriere fungieren, die potente immunstärkende Proteine direkt in Tumore bringen, lokale Abwehrkräfte aktivieren und gleichzeitig die Ganzkörper‑Exposition begrenzen. Auch wenn die behandelten Mäuse nicht vollständig geheilt wurden, verlangsamte der Ansatz das Tumorwachstum und verlängerte das Leben ohne größere Toxizität. Das deutet darauf hin, dass weitere Verbesserungen — etwa die Stabilisierung des Auslieferungssystems oder die Kombination mit anderen Therapien — die Wirksamkeit steigern könnten. Für Nicht‑Fachleute lautet die Hauptbotschaft: Mikroben, die einst nur als Feinde galten, könnten bald als präzise Werkzeuge genutzt werden, um das körpereigene Immunsystem gezielter gegen Krebs einzusetzen.
Zitation: Ha, J., Song, M. Tumor-specific cytokine therapy mediated by engineered Salmonella with a synthetic protein delivery system. Sci Rep 16, 14240 (2026). https://doi.org/10.1038/s41598-026-44265-2
Schlüsselwörter: bakterienbasierte Krebstherapie, tumorgerichtete Zytokinabgabe, gentechnisch veränderte Salmonella, Krebsimmuntherapie, synthetische Proteinsekretion