Clear Sky Science · ja
合成タンパク質輸送システムを用いた改変サルモネラによる腫瘍特異的サイトカイン療法
細菌をがんと戦う味方に変える
がん治療の現場では、サイトカインと呼ばれる免疫を活性化する薬剤が腫瘍への攻撃を助けることが知られていますが、強力すぎるため健康な組織にも損害を与えがちです。本研究は一風変わった回避策を探ります:食中毒を引き起こすことで知られるサルモネラを弱毒化し、腫瘍にこっそり入り込んで必要な場所だけで設計された免疫信号を放出する小さな輸送体として用いることで、局所的な防御を強化しつつ全身への影響を抑えようとするものです。
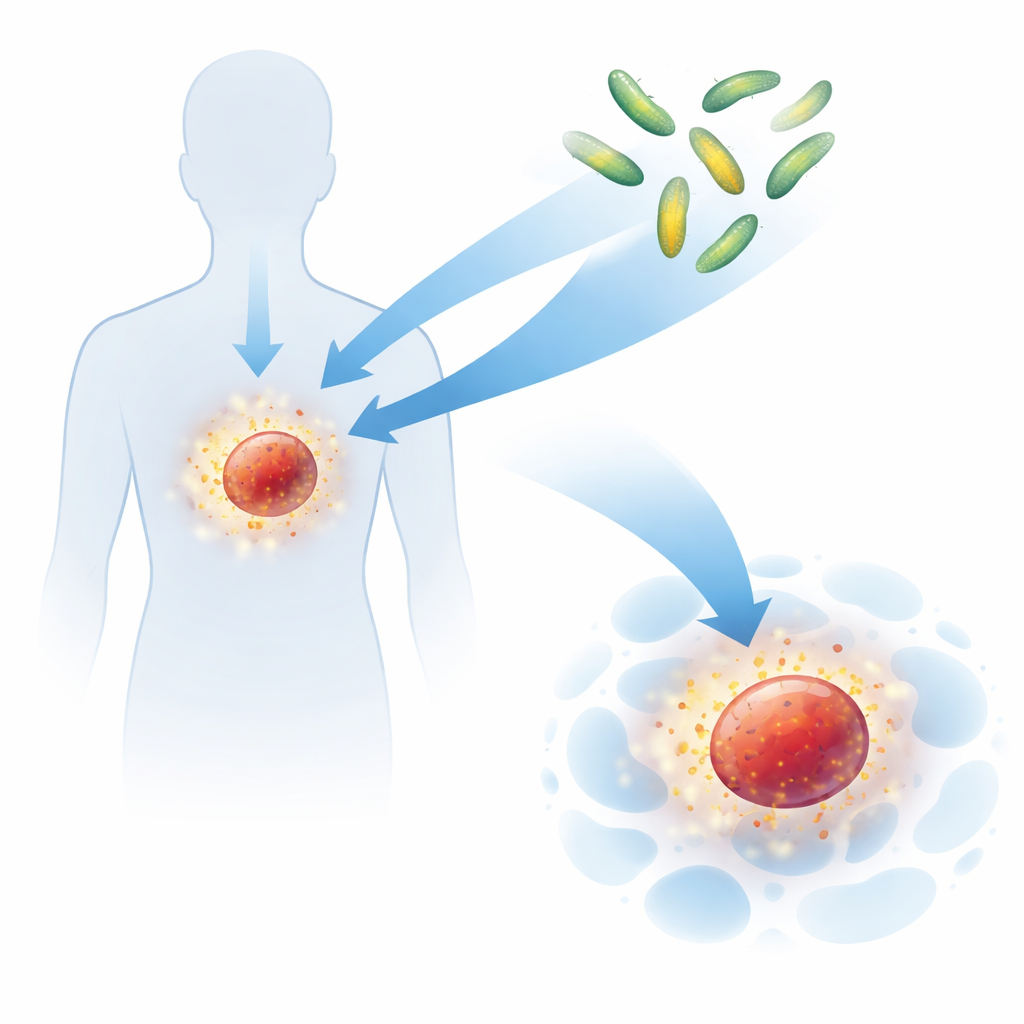
既存の免疫シグナルが使いにくい理由
サイトカインは免疫細胞に休むべきか戦うべきかを伝える分子メッセージのように働きます。インターロイキン‑2やインターロイキン‑15のような天然サイトカインに基づく薬は、がんを攻撃するT細胞やナチュラルキラー細胞を強力に活性化できますが、全身を循環して危険な副作用を引き起こし、血中で速やかに分解されるという重大な欠点があります。より新しい計算設計されたサイトカインであるNeoleukin‑2/15は、がんと戦う細胞を目覚めさせる良い効果を保ちながら、免疫抑制を招く経路を避けるように作られました。マウスではその設計タンパク質はよく働きましたが、ヒト試験では依然としてオフターゲットの問題が生じ、問題の核心は分子そのものだけではなく、どこでどう送達されるかにあることを示唆しました。
腫瘍に自然に集まる細菌を利用する
ある種の細菌は腫瘍内に見られる酸素が乏しい過酷な環境を好み、健康な臓器からは排除される一方で腫瘍内で増殖する傾向があります。研究者たちはこの挙動を利用し、正常組織を侵入・損傷しないよう遺伝的に制御したサルモネラを扱いました。彼らは宿主細胞への侵入を通常可能にする2つの主要な遺伝領域を削除し、腫瘍へ移動する能力を残しながら高度に弱毒化された株を作製しました。この株に、精巧に設計されたタンパク質輸出システムと、設計サイトカインNeo‑2/15をコードする別の遺伝子群を導入し、各細菌を腫瘍組織の内部で免疫刺激性タンパク質を制御して作り出し放出する工場に変えました。
スイッチ可能なタンパク質輸送装置の構築
Neo‑2/15を細菌細胞外へ、腫瘍微小環境へと移送するために、チームはサルモネラが感染時に通常用いる分子注射器であるタイプIII分泌系を再配線しました。多数の遺伝子を一つのプラスミド—環状DNA片—にまとめ、全分泌装置を一般的な抗生物質ドキシサイクリンによってオンにできるようにしました。天然のサルモネラタンパク質由来の短いタンパク質“タグ”をNeo‑2/15に融合し、系が誘導されると菌はこのタグ付きサイトカインを周囲の液体に送り出しました。試験管内の実験では、ドキシサイクリンの添加で融合タンパク質の安定した分泌が誘導され、菌を殺すことなく分泌が続き、標準的な生化学的アッセイで放出物が測定可能なレベルで存在し、期待されるサイズと構造を保持していることが確認されました。
設計されたシグナルが依然として機能することの証明
サイトカインを放出するだけでは、免疫細胞に正しい“言葉”を伝えられなければ意味がありません。チームはこれを、通常サイトカインに依存して生存・増殖するマウス由来のT細胞株を、分泌されたNeo‑2/15融合タンパク質を含む細菌培養上清にさらすことで試験しました。この上清を生物学的に関連する用量に濃縮すると、T細胞は標準的なインターロイキン‑2や従来法で精製したNeo‑2/15がある場合とほぼ同様に増殖しました。上清中のサイトカイン量が厳密には少なくても、設計されたシグナルと他の細菌成分の組み合わせがT細胞数を増加させ、分泌後も融合タンパク質が機能を保持していることを示しました。
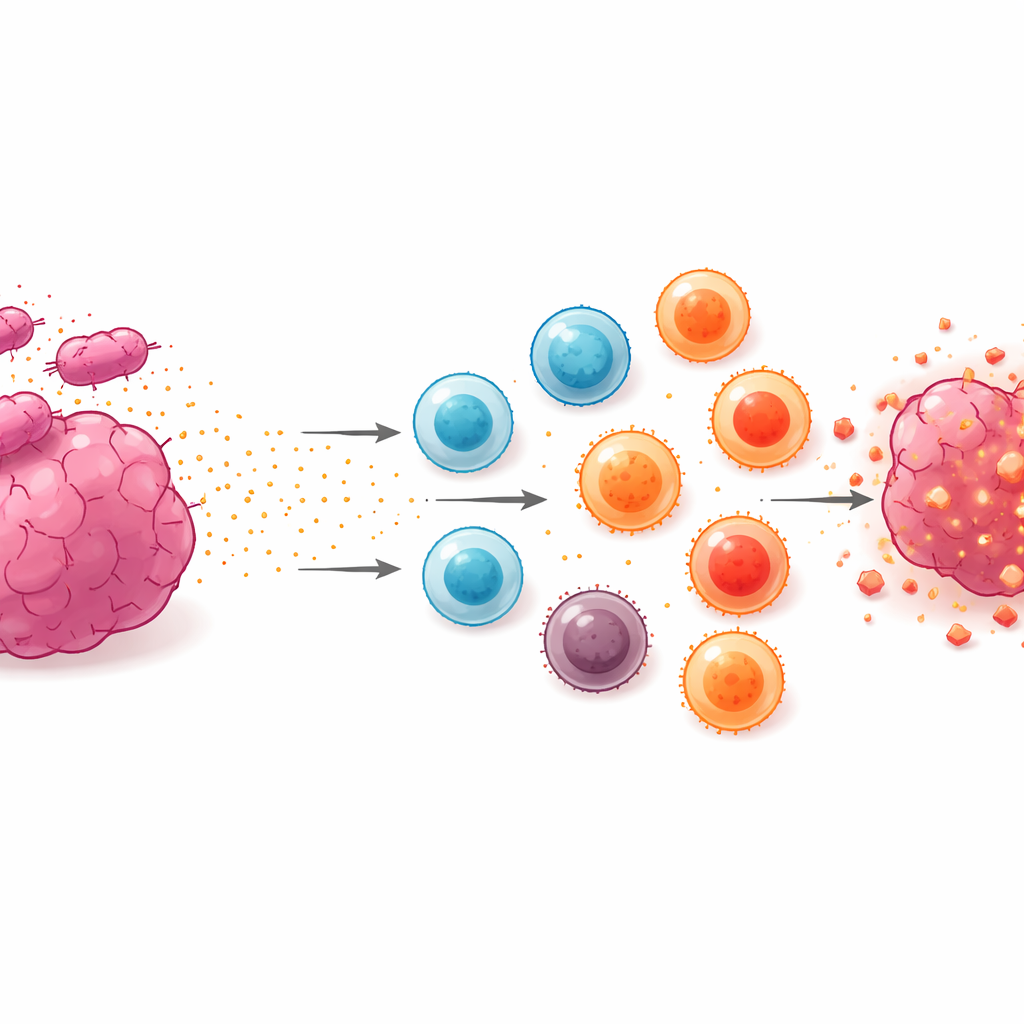
マウスで腫瘍を遅らせ生存を延ばす
最終的な試験は、この細菌による送達戦略が動物のがんと戦う手助けになるかどうかでした。マウスに大腸がん細胞を移植し、腫瘍が形成された後に弱毒化サルモネラを分泌系とNeo‑2/15の貨物とともに注入しました。ドキシサイクリンのスイッチをオフにしておくと腫瘍は増大を続けましたが、未治療の対照よりわずかに長生きしたマウスもおり、これは腫瘍内で細菌が死ぬ際に一部のサイトカインが漏出したためと考えられます。スイッチを入れて分泌が完全に活性化されると、腫瘍成長は著しく遅くなり、処置を受けたマウスは未処置群に比べおおむね2倍長く生存しました。血液検査で肝臓や腎臓の明らかな損傷は認められませんでした。効果が完全な治癒に至らなかった一因は、分泌機構を担うプラスミドの一つが体内で徐々に失われ、高レベルのサイトカイン放出を持続できる期間が制限されたことにあります。
将来のがん治療にとっての意味
本研究は、生きた弱毒化細菌をプログラム可能な運び屋として再設計し、強力な免疫増強タンパク質を腫瘍内部へ直接運んで局所の防御を活性化しつつ全身曝露を抑えられることを示しています。処置を受けたマウスが完全に治癒したわけではないものの、腫瘍増殖を遅らせ生存を延長し重大な毒性を伴わなかったことは、送達系の安定化や他の治療との併用といった改良が行われればより効果的になり得ることを示唆します。専門外の読者に向けた主なメッセージは、かつては敵と見なされていた微生物が、より標的化された形で体の免疫系をがんに向ける精密な道具として利用され得るようになるかもしれない、ということです。
引用: Ha, J., Song, M. Tumor-specific cytokine therapy mediated by engineered Salmonella with a synthetic protein delivery system. Sci Rep 16, 14240 (2026). https://doi.org/10.1038/s41598-026-44265-2
キーワード: 細菌ベースのがん治療, 腫瘍標的サイトカイン送達, 改変サルモネラ, がん免疫療法, 合成タンパク質分泌