Clear Sky Science · ru
От длины цепи до гибели клетки: механистическая основа апоптоза, опосредованного ОРВ, вызываемого насыщенными жирными кислотами
Почему жирные кислоты могут помочь прицельно воздействовать на раковые клетки
Жиры часто изображают как диетических злодеев, но некоторые молекулы, похожие на жиры, могут выступать точными инструментами в нашем организме. В этом исследовании рассматривается семейство таких молекул — этаноламиды жирных кислот — и поставлен, на первый взгляд, простой вопрос с большими последствиями: определяет ли длина их углеродной цепи, насколько эффективно они убивают раковые клетки, щадя при этом здоровые? Тщательно варьируя длину цепи, авторы показывают, как эти липиды можно сконструировать так, чтобы запускать контролируемую гибель клеток в клетках рака простаты, намекая на новые подходы к разработке более разумных противораковых лекарств и носителей препаратов.
Создание дизайнерских молекул жира
Команда синтезировала серию близкородственных молекул, присоединяя «головку» этаноламина к насыщенным «хвостам» из жирных кислот разной длины — от коротких (8 атомов углерода) до длинных (18 углеродов). Получился градуированный ряд этаноламидов жирных кислот с постепенно меняющимися свойствами. Затем провели широкий физико‑химический анализ, измеряя, насколько легко каждое соединение растворяется в воде, насколько оно маслянистое или гидрофобное, как ведёт себя на поверхностях и как течёт в виде жидкости. Эти тесты показали, что короткие цепи более гидрофильны и легче растворяются, тогда как с увеличением длины хвоста молекулы становились более маслянистыми, образовывали более уплотнённые структуры и давали более вязкие растворы. Иными словами, простое добавление углеродов к хвосту систематически изменяло поведение каждой молекулы в смешанных водно‑жировых средах.
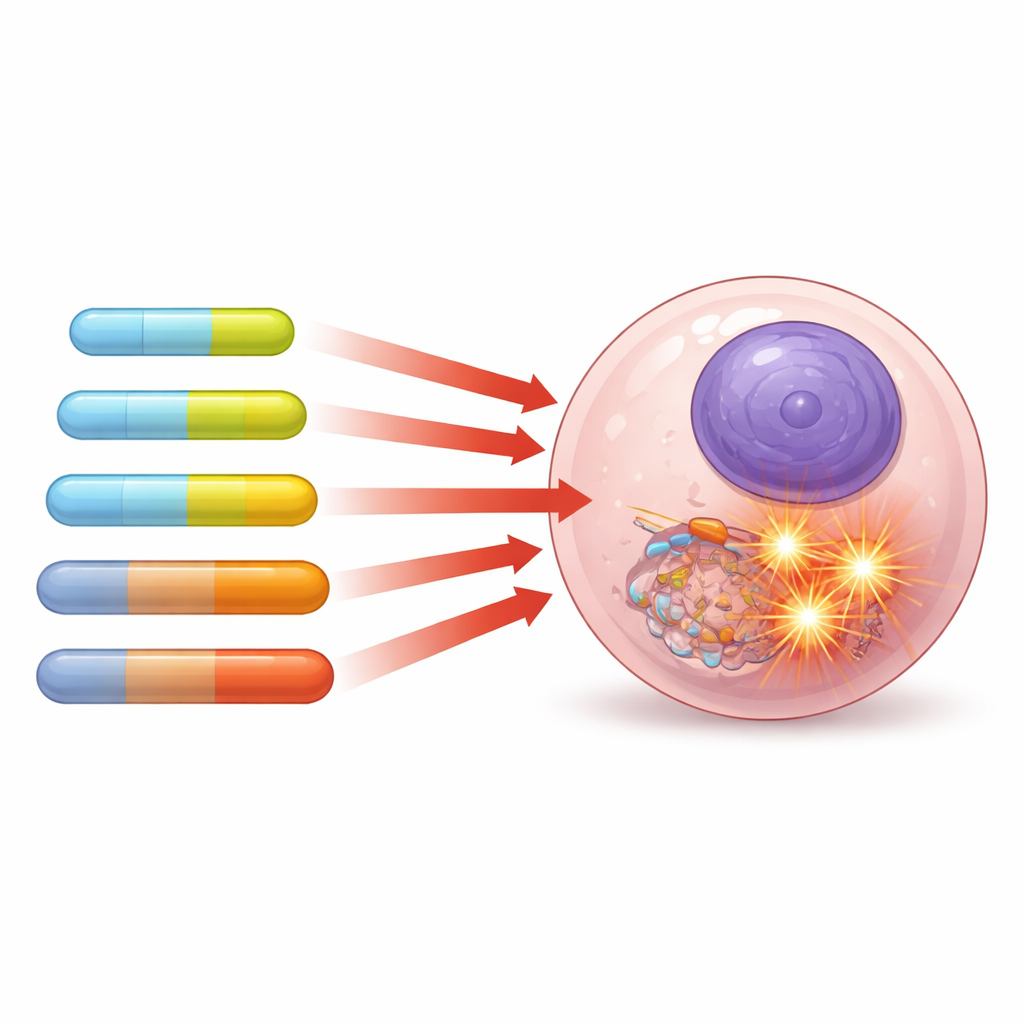
Как длина цепи формирует гибель клетки
Далее исследователи проверяли, как эти настроенные липиды влияют на три линии человеческих раковых клеток, сосредоточившись на клетках рака простаты (PC‑3), которые оказались наиболее чувствительными. Короткоцепочечные соединения практически не вредили клеткам, но по мере удлинения хвостов токсичность для PC‑3 возрастала. Молекула средней длины на основе 12‑углеродной жирной кислоты показала характерный профиль: она значительно повышала уровень реактивных форм кислорода — высокореактивных побочных продуктов клеточного метаболизма — нарушала электрохимический баланс через мембрану митохондрий (энергетических центров клетки) и вызывала выраженный апоптоз, форму запрограммированной клеточной смерти. Ещё более длинные цепи (14–18 углеродов) были более гидрофобными и также индуцировали сильный апоптоз, иногда через кислородозависимое повреждение, иногда через более прямое воздействие на клеточные мембраны и митохондрии. Важно, что те же соединения вызывали очень мало разрушений эритроцитов, что говорит о том, что они могут быть мощными против опухолевых клеток и при этом щадящими для нормальных клеток крови.
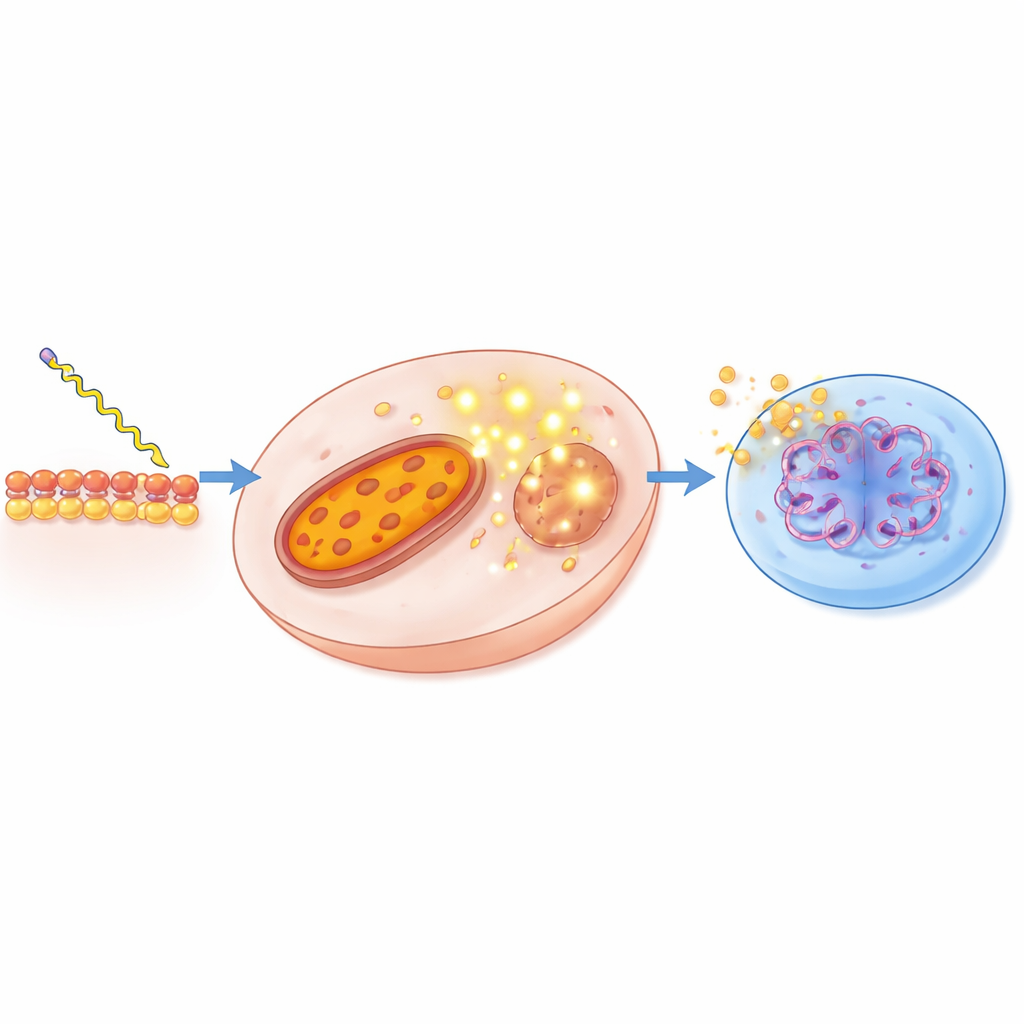
Внутри клетки: стресс, энергетический сбой и распад ДНК
Чтобы понять происходящее внутри раковых клеток, команда использовала флуоресцентные красители и проточную цитометрию для отслеживания ключевых этапов процесса гибели. Они наблюдали, что соединения средней и большой длины вызывали коллапс мембранного потенциала митохондрий — признак сбоя энергетической машины клетки. Одновременно резко возрастал уровень реактивных форм кислорода, особенно для молекул с 12‑ и 18‑углеродными цепями. В микроскопе обработанные клетки PC‑3 демонстрировали уплотнение и фрагментацию ядерного материала, а гель‑тесты ДНК выявляли характерный «лестничный» рисунок апоптоза. Проточные анализы далее подтвердили, что большинство умирающих клеток следуют маршруту запрограммированной смерти, а не разрываются неконтролируемым некрозом. Все вместе эти данные складываются в последовательную картину: настроенные этаноламиды жирных кислот проникают в раковые клетки, нарушают работу митохондрий, усиливают окислительный стресс и завершают процесс чистой, программируемой самоуничтожения.
Взаимодействие с рецепторами клеток
Исследование также изучало, как эти липиды могут взаимодействовать с известными сигнальными центрами. С помощью компьютерного молекулярного докинга авторы смоделировали, как каждое соединение помещается в карманы связывания каннабиноидных рецепторов CB1 и CB2 — белков, которые уже известны как реагирующие на жироподобные сигнальные молекулы. Молекулы средней и большой длины связывались плотнее, чем короткие, образуя стабилизирующие контакты внутри рецептора. Хотя эти моделирования не доказывают причинно‑следственную связь, они поддерживают идею, что те структурные особенности, которые способствуют нарушению митохондрий и окислительному стрессу, также могут повышать способность молекул взаимодействовать с этими рецепторами, добавляя рецептор‑опосредованный уровень к их антираковому действию.
Превращение длины цепи в механизм проектирования
Чтобы объединить многочисленные измерения, команда использовала статистический метод, выявляющий закономерности в наборах данных. Этот анализ показал, что один фактор — длина жирового хвоста — объяснял большую часть вариации растворимости, поведения на поверхности, окислительного стресса и гибели клеток. Короткие цепи способствовали растворимости и мягкому поведению, средние цепи, как 12‑углеродное соединение, находили баланс, максимально направляя действие на митохондрии и апоптоз при контролируемом стрессе, а длинные цепи сдвигали картину в сторону сильной, многосторонней цитотоксичности. С практической точки зрения это означает, что длину цепи можно рассматривать как ручку настройки при кастомизации этих липидов в качестве прозергов и функциональных компонентов в системах доставки лекарств.
Что это значит для будущих терапий
Проще говоря, это исследование показывает, что небольшие структурные изменения в жироподобных молекулах могут существенно повлиять на то, будут ли они тихо сосуществовать с клетками или подтолкнут раковые клетки к самоуничтожению. Выделяющееся 12‑углеродное этаноламидное соединение действует как контролируемый триггер, создавая достаточно внутреннего стресса, чтобы убить клетки рака простаты, при этом обладая благоприятными физическими свойствами и ограниченным побочным воздействием. Более длинные цепи могут выступать ещё более мощными «убийцами», возможно, служа в роли прозергов, активируемых внутри опухолей. Хотя работа пока проведена на культурах клеток, она закладывает механистическую основу для проектирования следующего поколения липидных лекарств, в которых длина жирового хвоста помогает определить, куда попадает соединение, как оно ведёт себя и насколько эффективно может выводить из строя опасные клетки.
Цитирование: Salehi, F., Jamali, T. & Kavoosi, G. From chain length to cell death: mechanistic basis for ROS-mediated apoptosis induced by saturated fatty acids. Sci Rep 16, 13748 (2026). https://doi.org/10.1038/s41598-026-42822-3
Ключевые слова: этаноламиды жирных кислот, рак предстательной железы, окислительный стресс, митохондрии, апоптоз