Clear Sky Science · pl
Od długości łańcucha do śmierci komórki: mechanistyczne podstawy apoptozy indukowanej przez ROS przez nasycone kwasy tłuszczowe
Dlaczego kwasy tłuszczowe mogą pomagać w celowaniu w komórki nowotworowe
Tłuszcze są często przedstawiane jako wrogowie diety, ale niektóre molekuły przypominające tłuszcze mogą pełnić w organizmie rolę precyzyjnych narzędzi. W badaniu tym przeanalizowano rodzinę takich związków — etanoloamidów kwasów tłuszczowych — i postawiono pozornie proste pytanie o dalekosiężnych konsekwencjach: czy długość ich łańcucha węglowego decyduje o tym, jak skutecznie zabijają komórki nowotworowe, oszczędzając przy tym zdrowe? Poprzez staranne dostrajanie długości łańcucha autorzy pokazują, że te lipidy można zaprojektować tak, by wywoływały kontrolowaną śmierć komórek w liniach raka prostaty, co wskazuje na nowe możliwości projektowania inteligentniejszych terapii i nośników leków.
Tworzenie zaprojektowanych cząsteczek tłuszczu
Zespół zsyntezował serię blisko spokrewnionych związków, łącząc grupę etanolaminową jako „głowę” z nasyconymi „ogonami” kwasów tłuszczowych o różnej długości — od krótkich (8 atomów węgla) do długich (18 atomów). Powstał stopniowy zestaw etanoloamidów kwasów tłuszczowych o stopniowo zmieniających się właściwościach. Przeprowadzono szeroką charakterystykę fizyczno-chemiczną, mierząc rozpuszczalność w wodzie, stopień oleistości czy hydrofobowość, zachowanie na powierzchniach i lepkość płynów. Testy wykazały, że krótsze łańcuchy były bardziej hydrofilowe i łatwiejsze do rozpuszczenia, podczas gdy dłuższe stawały się bardziej oleiste, formowały ścisłe struktury i prowadziły do bardziej lepkościowych roztworów. Innymi słowy, samo dodanie atomów węgla do „ogona” systematycznie zmieniało zachowanie każdej molekuły w środowiskach mieszanych woda–tłuszcz.
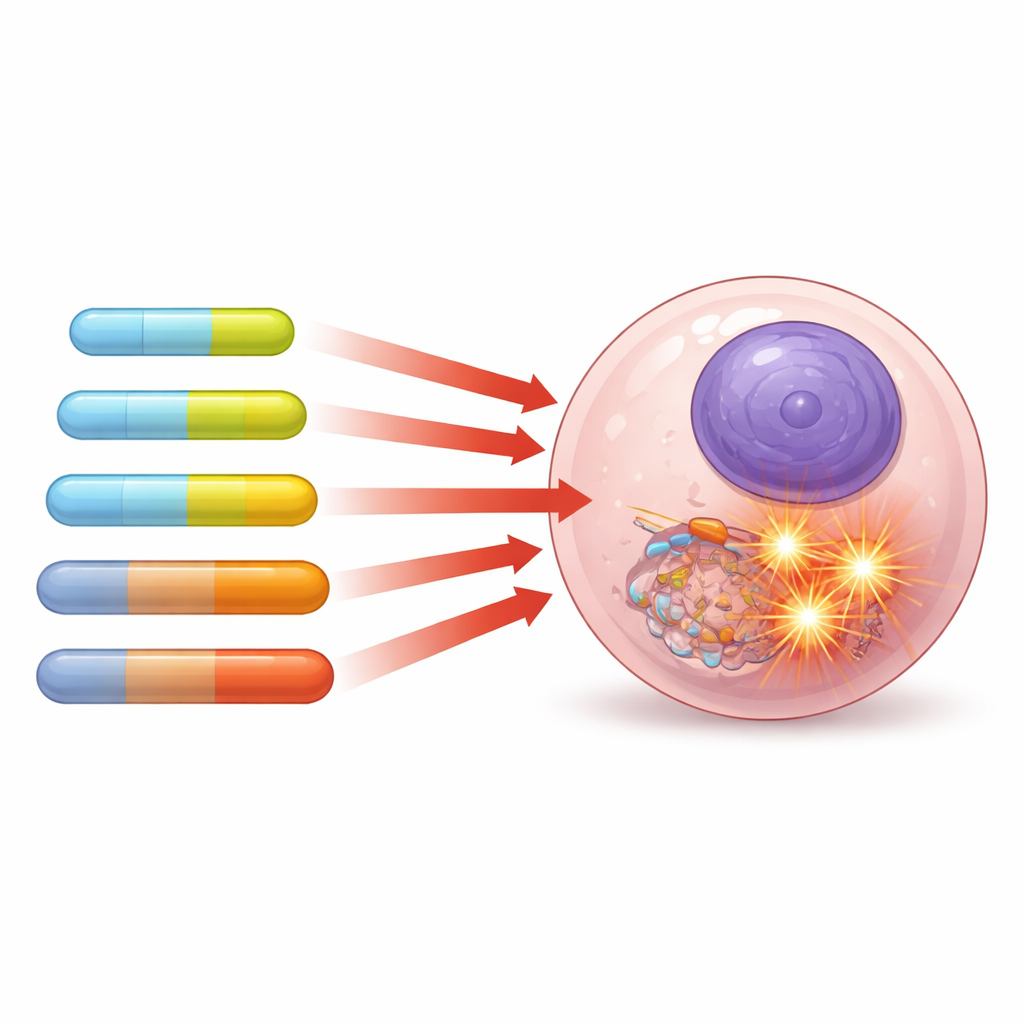
Jak długość łańcucha kształtuje śmierć komórki
Następnie badacze sprawdzili, jak te dostrojone lipidy wpływają na trzy ludzkie linie komórek nowotworowych, koncentrując się na komórkach raka prostaty (PC-3), które okazały się najbardziej wrażliwe. Krótkie łańcuchy niemal nie szkodziły komórkom, natomiast w miarę wydłużania „ogonów” związki stawały się coraz bardziej toksyczne dla komórek PC-3. Cząsteczka o średniej długości oparta na 12-węglowym kwasie tłuszczowym wykazała charakterystyczny wzorzec: silnie zwiększała poziom reaktywnych form tlenu — wysoce reaktywnych produktów ubocznych metabolizmu komórkowego — zaburzała potencjał elektryczny mitochondriów (elektrownia komórki) i wywoływała wyraźną apoptozę, czyli programowaną śmierć komórki. Jeszcze dłuższe łańcuchy (14–18 atomów węgla) były bardziej hydrofobowe i również indukowały silną apoptozę, czasem poprzez uszkodzenia zależne od tlenu, a czasem przez bezpośrednie oddziaływanie z błonami komórkowymi i mitochondriami. Co ważne, te same związki powodowały bardzo niewielkie pękanie krwinek czerwonych, co sugeruje, że mogą być silne wobec komórek nowotworowych, a jednocześnie względnie łagodne wobec normalnych krwinek.
Wewnątrz komórki: stres, awaria energetyczna i rozpad DNA
Aby zrozumieć, co działo się wewnątrz komórek nowotworowych, zespół użył barwników fluorescencyjnych i cytometrii przepływowej do śledzenia kluczowych etapów procesu śmierci. Zaobserwowano, że związki o średnich i długich łańcuchach powodowały zapadanie się potencjału błony mitochondrialnej, co świadczy o upadku maszyny energetycznej komórki. Równocześnie nasilały się reaktywne formy tlenu, szczególnie dla cząsteczek 12- i 18-węglowych. Pod mikroskopem traktowane komórki PC-3 wykazywały skondensowany i pofragmentowany materiał jądrowy, a testy żelowe DNA ujawniały charakterystyczny „drabinkowy” wzór apoptozy. Analizy przepływowe potwierdziły również, że większość umierających komórek przeszła drogę programowanej śmierci, a nie niekontrolowaną nekrozę. Razem te obserwacje tworzą spójną opowieść: dostrojone etanoloamidy kwasów tłuszczowych wnikają do komórek nowotworowych, zaburzają mitochondria, wywołują stres oksydacyjny i prowadzą do „czystego”, zaprogramowanego samozniszczenia.
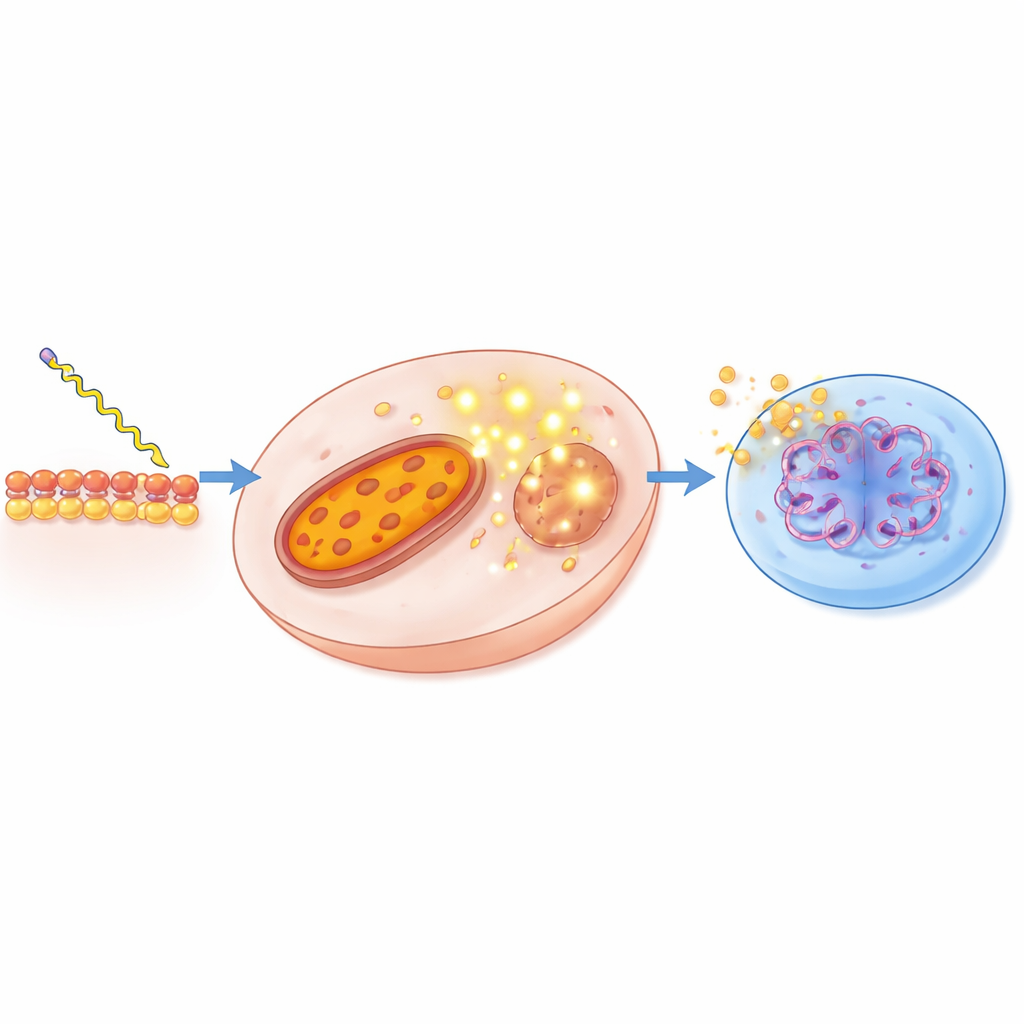
Komunikacja z receptorami komórkowymi
Praca badała też, jak te lipidy mogą komunikować się z poznanymi węzłami sygnałowymi. Przy użyciu komputerowego dokowania molekularnego badacze symulowali, jak każdy związek mieści się w kieszonkach wiążących receptorów kannabinoidowych CB1 i CB2 — białek już znanych z reagowania na lipidowe sygnały. Etanoloamidy o średnich i długich łańcuchach wiązały się silniej niż krótkie, tworząc stabilizujące kontakty wewnątrz receptora. Choć symulacje te nie dowodzą związku przyczynowo-skutkowego, wspierają ideę, że te same cechy strukturalne, które sprzyjają zaburzeniu mitochondriów i stresowi oksydacyjnemu, mogą także ułatwiać oddziaływanie z receptorami, dodając receptorowo pośredniczony wymiar do ich działania przeciwnowotworowego.
Przekształcenie długości łańcucha w pokrętło projektowe
Aby zintegrować liczne pomiary, zespół zastosował metodę statystyczną identyfikującą wzorce w danych. Analiza wykazała, że pojedynczy czynnik — długość tłuszczowego „ogona” — wyjaśnia większość zmienności w rozpuszczalności, zachowaniu na powierzchni, stresie oksydacyjnym i śmierci komórek. Krótsze łańcuchy sprzyjały rozpuszczalności i łagodniejszemu zachowaniu, łańcuchy średnie, takie jak związek 12-węglowy, osiągały kompromis maksymalizujący celowanie w mitochondria i apoptozę przy kontrolowanym stresie, a długie łańcuchy przesuwały równowagę w stronę silnej, wielotorowej cytotoksyczności. Z praktycznego punktu widzenia oznacza to, że długość łańcucha można traktować jak pokrętło projektowe do dostosowywania tych lipidów jako proleków i funkcjonalnych składników systemów dostarczania leków.
Co to oznacza dla przyszłych terapii
Mówiąc najprościej, badanie pokazuje, że drobne zmiany strukturalne w molekułach podobnych do tłuszczów mogą silnie wpływać na to, czy współistnieją one z komórkami w spokoju, czy też pchają komórki nowotworowe ku samobójstwu. Wyróżniający się etanoloamid o 12 atomach węgla działa jak kontrolowany wyzwalacz, generując wystarczający wewnętrzny stres, by zabić komórki raka prostaty, przy zachowaniu korzystnych właściwości fizycznych i ograniczonym działaniu poza celem. Dłuższe łańcuchy mogą pełnić rolę jeszcze silniejszych zabójców, potencjalnie jako proleki aktywowane wewnątrz guza. Choć prace te pozostają na etapie hodowli komórek, tworzą mechanistyczną podstawę do projektowania następnej generacji leków opartych na lipidach, w których długość tłuszczowego „ogona” pomaga określić, dokąd związek trafia, jak się zachowuje i jak skutecznie wyłącza niebezpieczne komórki.
Cytowanie: Salehi, F., Jamali, T. & Kavoosi, G. From chain length to cell death: mechanistic basis for ROS-mediated apoptosis induced by saturated fatty acids. Sci Rep 16, 13748 (2026). https://doi.org/10.1038/s41598-026-42822-3
Słowa kluczowe: etanoloamidy kwasów tłuszczowych, rak prostaty, stres oksydacyjny, mitochondria, apoptoza