Clear Sky Science · he
מאורך השרשרת למותו של התא: הבסיס המנגנוני של אפופטוזיס בתיווך ROS המושרה על ידי חומצות שומן רווחות
מדוע חומצות שומן יכולות לסייע במיקוד תאי סרטן
שומנים נתפסים לעתים כהרשעים התזונתיים, אבל מולקולות דמויות שומן מסוימות יכולות לשמש כלים מדויקים בגופנו. המחקר הזה בוחן משפחה של מולקולות כאלה, הקרויות אתנולאמידים של חומצות שומן, ושואל שאלה פשוטה אך עם השלכות גדולות: האם אורך שרשרת הפחמנים שלהן קובע עד כמה הן מסוגלות להרוג תאי סרטן תוך שמירה על תאים בריאים? על ידי כוונון מדוקדק של אורך השרשרת, החוקרים מראים כיצד ניתן לעצב את הליפידים האלה כדי להפעיל מוות תאי מבוקר בתאי סרטן הערמונית, ומרמזים על דרכים חדשות לעיצוב טיפולים חכמים ונושאי תרופות.
בניית מולקולות שומן מהונדסות
הצוות סינתז סדרת מולקולות קרובות זו לזו באמצעות חיבור "ראש" אתנולאמיני לזנבות של חומצות שומן רווחות באורכים שונים, מקצרים (8 פחמנים) ועד ארוכים (18 פחמנים). כך נוצר סט מדורג של אתנולאמידים של חומצות שומן עם תכונות משתנות בהדרגה. הם ביצעו ת characterization פיזיקלית וכימית מקיפה, מדדו עד כמה כל תרכובת מתמוססת במים, עד כמה היא שומנית או הידרופובית, כיצד היא מתנהגת במשטחים וכיצד היא זורמת כנוזל. הבדיקות חשפו ששרשרות קצרות היו יותר אוהדות מים וקלויות יותר להמיס, בעוד ששרשרות ארוכות הפכו לשומניות יותר, יצרו מבנים צפופים יותר והובילו לתמיסות עבות ויסקוזיות יותר. במילים אחרות, הוספת אטומי פחמן לזנב שינתה באופן שיטתי את התנהגות כל מולקולה בסביבות מעורבות מים–שומן.
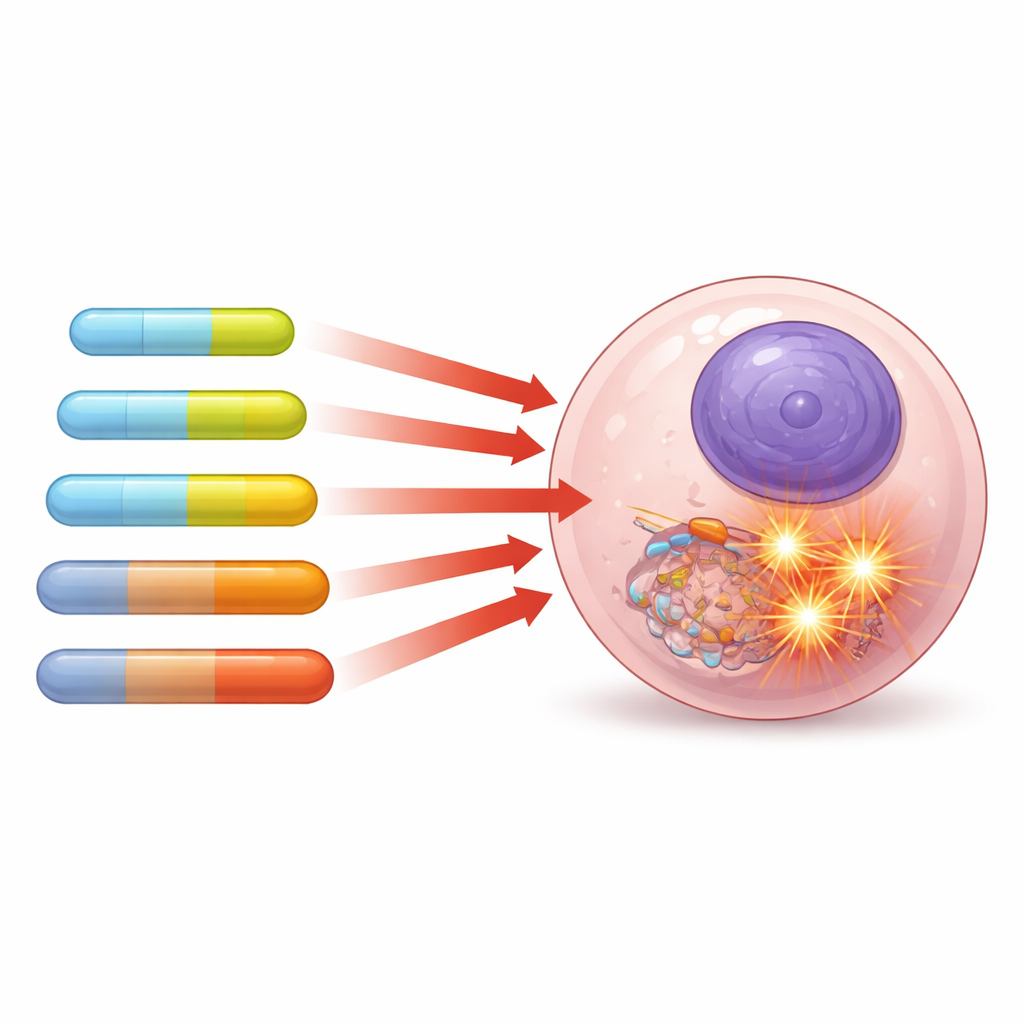
כיצד אורך השרשרת מעצב את מוות התא
בהמשך, החוקרים בדקו כיצד הליפידים המתואמים האלה השפיעו על שלוש שורות של תאים סרטניים אנושיים, עם דגש על תאי סרטן הערמונית (PC-3), שנמצאו הרגישים ביותר. חברי השרשרת הקצרה כמעט ולא פגעו בתאים, אך ככל שהזנבות התרבו באורך, התרכובות הפכו רעילות יותר לתאי PC-3. מולקולה באורך בינוני המבוססת על חומצה שומנית בת 12 פחמנים הציגה דפוס מובהק: היא הגרימה עלייה חזקה ברדיקלים חופשיים של חמצן—תוצרי לוואי רעילים מאוד של המטבוליזם התאי—שיבשה את מאזן המתח החשמלי במיטוכונדריה (תחנת הכוח של התא) והפעילה אפופטוזיס משמעותי, צורת מוות תאי מתוכנתת. שרשרות ארוכות אף יותר (14–18 פחמנים) היו הידרופוביות יותר והפעילו גם הן אפופטוזיס חזק, לעיתים באמצעות נזק התלוי בחמצן ולעיתים באמצעות השפעות ישירות יותר על ממברנות התא והמיטוכונדריה. חשוב לציין, אותן תרכובות גרמו לנזק מועט מאוד לפירוק תאי דם אדומים, מה שמרמז שהן חזקות נגד תאים סרטניים אך עדינות כלפי תאי דם נורמליים.
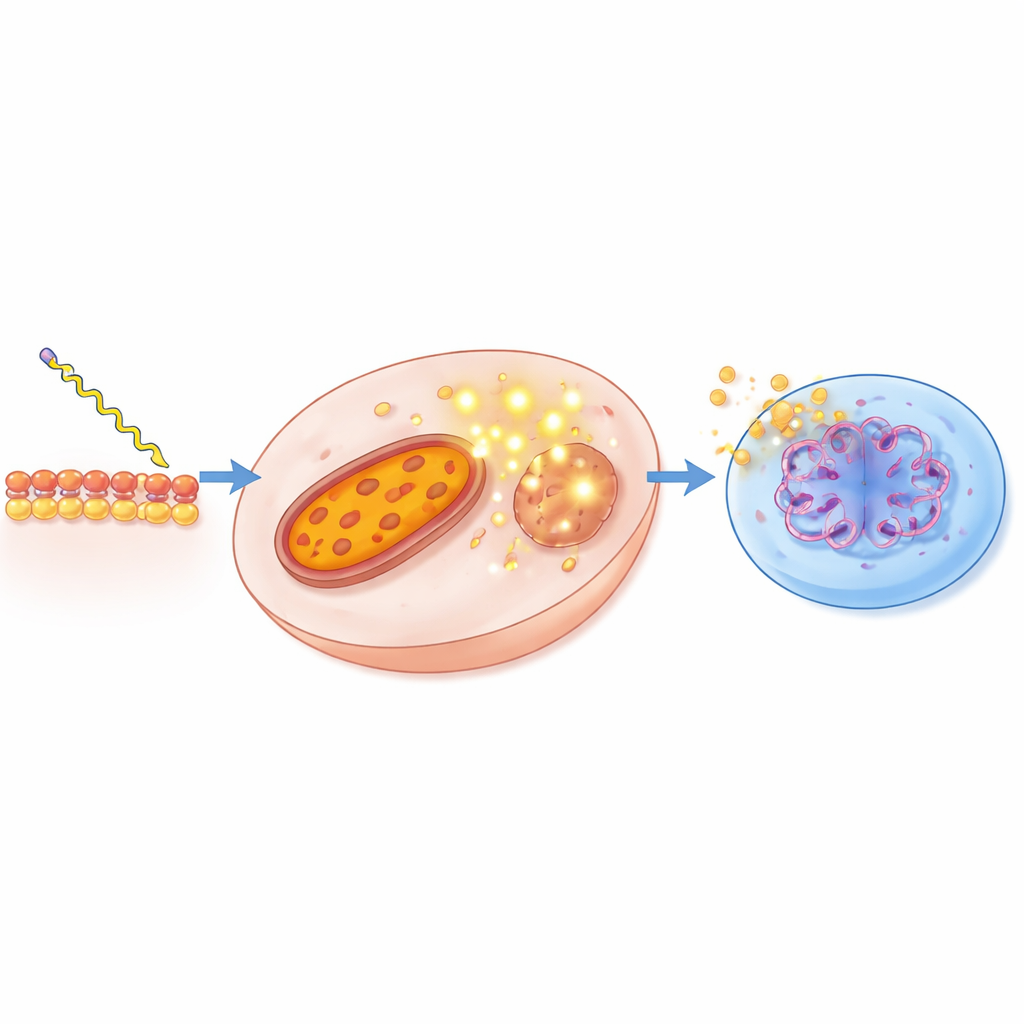
בתוך התא: לחץ, כשל אנרגיה ושבר בדנ"א
כדי להבין מה מתרחש בתוך תאי הסרטן, הצוות השתמש בצבעים פלואורסצנטיים ובסיטומטריה בזרימה כדי לעקוב אחר שלבים מרכזיים בתהליך המוות. הם צפו שמולקולות באורך בינוני וארוך גרמו לקריסה של פוטנציאל ממברנת המיטוכונדריה, סימן לכך שמכונת האנרגיה של התא נכשלת. בו בזמן, רמות המולקולות הריאקטיביות של החמצן זינקו, בעיקר עבור מולקולות ב-12 וב-18 פחמנים. תחת המיקרוסקופ, תאי PC-3 המטופלים הראו חומר גרעיני דחוס ומפורק, ובמבחני ג'ל לדנ"א נצפה דפוס "סולם" האופייני לאפופטוזיס. בדיקות מבוססות זרימה איששו שחלק גדול מהתאים המתים עברו את מסלול המוות המתוכנת ולא פיצוץ בלתי נשלט של נקרוזה. יחד, הממצאים בונים סיפור עקבי: אתנולאמידים של חומצות שומן בכוונון נכנסו לתאים סרטניים, הפריעו למיטוכונדריה, גרמו ללחץ חמצוני והובילו להשמדה עצמית מתוכננת ומסודרת.
תקשורת עם קולטני התא
המחקר בדק גם כיצד הליפידים האלה עלולים לתקשר עם צירי איתות ידועים. באמצעות דוקינג מולקולרי ממוחשב, סימלו החוקרים כיצד כל תרכובת מתאימה לכיסי הקישור של קולטני הקנאבינואיד CB1 ו-CB2, חלבונים הידועים כבר כמגיבים למולקולות אות שומניות. אתנולאמידים באורך בינוני וארוך קושרו בחוזקה רבה יותר מאשר קצרים, תוך יצירת מגעים מייצבים בפנים הקולטן. אמנם סימולציות אלה אינן מוכיחות סיבה ותוצאה, אך הן תומכות ברעיון שהתכונות המבניות שמקדמות הפרעה מיטוכונדריאלית ולחץ חמצוני עשויות גם להפוך את המולקולות ליותר מתאימות לתקשר עם קולטנים אלה, מה שמוסיף שכבת מנגנון מתווכת-קולטנים לפעילות האנטי־סרטנית שלהן.
הפיכת אורך השרשרת לכפתור עיצוב
כדי לשלב את המדידות הרבות, הצוות השתמש בשיטה סטטיסטית שמזהה דפוסים בין מערכי נתונים. הניתוח הראה שגורם יחיד—אורך זנב השומן—הסביר את רוב השונות בפתרון במים, בהתנהגות פני השטח, בלחץ החמצוני ובמות התא. שרשרות קצרות הטו לטובת מסיסות והתנהגות עדינה, שרשראות בינוניות כמו המולקולה בת 12 פחמנים מצאו איזון שממקסם מיקוד מיטוכונדריאלי ואפופטוזיס עם לחץ מבוקר, ושרשראות ארוכות יותר דחפו לכיוון רעילות חזקה ורב־מערכתית. מבחינה מעשית, הדבר אומר שניתן להתייחס לאורך השרשרת ככפתור עיצוב להתאמת הליפידים הללו כפרודראגים ורכיבים פונקציונליים במערכות נשא של תרופות.
מה משמעות הדבר לטיפולים עתידיים
במונחים פשוטים, המחקר מראה ששינויים מבניים עדינים במולקולות דמויות שומן יכולים להשפיע רבות על האם הן יתקיימו בשקט עם התאים או ידחפו תאי סרטן להתאבדות. אתנולאמיד בולט באורך 12 הפחמנים פועל כזרז מבוקר: הוא יוצר מספיק מתח פנימי כדי להרוג תאי סרטן הערמונית תוך שמירה על תכונות פיזיקליות נוחות ונזק צדדי מוגבל. שרשראות ארוכות יותר יכולות לפעול כ"מכשירים הרג" עוצמתיים אף יותר, שעשויים לשמש כפרודראגים שמופעלים בתוך הגידול. אמנם העבודה עדיין בשלב תרבית תאים, היא מניחה בסיס מנגנוני לעיצוב תרופות מבוססות ליפידים בדור הבא, שבו אורך זנב השומן מסייע לקבוע לאן התרכובת מגיעה, כיצד היא מתנהגת ועד כמה בחוזקה היא מסוגלת לנטרל תאים מסוכנים.
ציטוט: Salehi, F., Jamali, T. & Kavoosi, G. From chain length to cell death: mechanistic basis for ROS-mediated apoptosis induced by saturated fatty acids. Sci Rep 16, 13748 (2026). https://doi.org/10.1038/s41598-026-42822-3
מילות מפתח: אתנולאמידים של חומצות שומן, סרטן הערמונית, לחץ חמצוני, מיטוכונדריה, אפופטוזיס