Clear Sky Science · ru
Эффективность и сигналы безопасности из ранних фаз исследований ингибирования KRAS при раке поджелудочной железы
Почему это важно для пациентов и их семей
Рак поджелудочной железы — одно из самых смертоносных онкологических заболеваний: у большинства пациентов после постановки диагноза, когда болезнь уже распространилась, продолжительность жизни измеряется месяцами. Долгое время врачи в основном полагались на жесткую химиотерапию, дающую ограниченную пользу. Эта статья рассматривает новый класс препаратов, которые напрямую нацелены на ключевой дефектный белок KRAS, ответственный за большинство случаев рака поджелудочной железы. Обобщая результаты ранних клинических испытаний, исследователи задают простой, но срочный вопрос: достаточно ли эти новые лекарства эффективны и безопасны, чтобы изменить прогноз для пациентов с этой болезнью?
Сложная опухоль и давняя преграда
Аденокарцинома протоков поджелудочной железы, наиболее распространенная форма рака поджелудочной, агрессивна и часто диагностируется на поздних стадиях, когда операция уже не представляется возможной. Стандартные схемы лечения объединяют несколько препаратов химиотерапии. Хотя они могут незначительно продлевать выживаемость, часто возникают сильные побочные эффекты, вынуждающие снижать дозы или преждевременно прекращать лечение. Почти в 90 процентах этих опухолей обнаруживаются мутации в KRAS — молекулярном выключателе, контролирующем сигналы роста в клетках. В течение многих лет KRAS считали «нелекарственным», поскольку его поверхность предлагала мало мест для надежного связывания лекарств. В результате попытки блокировать KRAS косвенно, воздействуя на другие звенья его сигнального каскада, в основном не приводили к улучшению исходов.
Новый класс препаратов нацелен на KRAS
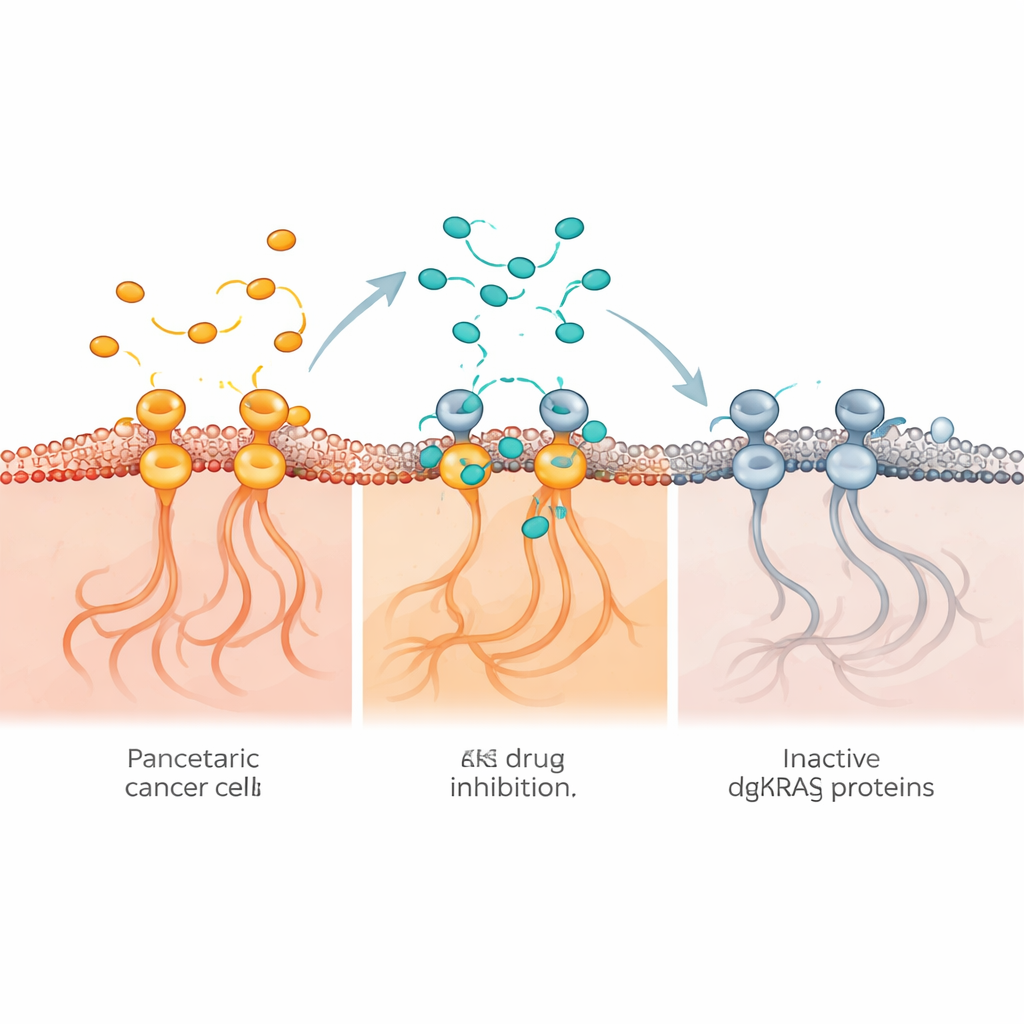
Ситуация изменилась с появлением малых молекул, способных непосредственно связываться с мутировавшим KRAS и нарушать его активность. KRAS обычно переключается между неактивной и активной формой; онкогенные мутации фиксируют его в положении «включено», постоянно посылая клеткам сигнал к росту. Различные экспериментальные препараты, сейчас находящиеся в испытаниях, могут запирать KRAS в выключенном состоянии, атаковать его в активной форме или образовывать более сложные трехкомпонентные структуры, блокирующие его функцию. Поскольку эти лекарства распознают разные конформации одного и того же белка, у них могут быть разные сильные и слабые стороны, а также отличаться механизмы развития резистентности. Авторы утверждают, что их эффекты нельзя считать идентичными и их следует оценивать для каждого препарата отдельно. 
Что показывают ранние исследования
Чтобы понять, чего пока удалось добиться новым препаратам, исследователи провели систематический обзор и мета-анализ семи исследований ранних фаз, в которых участвовали 463 пациента с прогрессирующим или метастатическим раком поджелудочной железы. Все пациенты ранее получали по крайней мере одну линию терапии, что делало их болезни особенно трудно контролируемыми. Только 293 пациента могли быть оценены на предмет уменьшения опухоли, поскольку у многих не было полных сканов или они выбыли по разным причинам. При объединении доступных данных примерно у 29 процентов оцениваемых пациентов наблюдалось значимое уменьшение опухоли. Результаты были удивительно согласованы между исследованиями, что указывает на то, что в будущих испытаниях с похожими препаратами у схожих пациентов вероятно будут сопоставимые показатели ответа. Для рака поджелудочной железы — где исторически значимое уменьшение опухолей было редкостью — такой уровень активности рассматривается как обнадеживающий, хотя по-прежнему далек от излечения.
Побочные эффекты и оговорки исследований
Эффективность — лишь часть картины; безопасность не менее важна. В ходе испытаний проблемы с желудком и кишечником были одними из наиболее частых побочных эффектов. Примерно у четырех из десяти пациентов возникали диарея или тошнота. Когда авторы сосредоточились только на пациентах с раком поджелудочной железы в исследованиях, в которых приводились данные о безопасности именно для этого заболевания, показатели были схожими или немного выше. Конкретный профиль побочных эффектов различался для разных препаратов, а некоторые более крупные исследования, смешивавшие разные типы опухолей, не приводили раздельных данных по раку поджелудочной железы, что затрудняло выявление четких тенденций. Авторы также отметили, что общий риск смещения в включенных исследованиях был от умеренного до высокого. Это были небольшие исследования ранних фаз с одной ветвью и без контрольных групп, поэтому невозможно с уверенностью сказать, стало ли состояние пациентов лучше по сравнению с тем, что было бы при стандартной терапии.
Куда двигаться дальше
Несмотря на эти предостережения, совокупность данных поддерживает ключевой вывод: теперь действительно возможно нацелиться на KRAS при раке поджелудочной железы, и это может приводить к реальному, пусть и умеренному, уменьшению опухоли у сильно предварительно пролеченных пациентов. Авторы рассматривают это как важный перелом после десятилетий разочарований. В то же время у большинства пациентов ответы пока не являются стойкими, а побочные эффекты остаются проблемой. В статье призывают к более крупным, более строгим и унифицированным испытаниям, которые будут сопоставлять конкретные мутации KRAS с определёнными препаратами, разумно сочетать эти агенты с иммунотерапией и другими таргетными методами, а также внедрять современные биомаркеры, такие как мониторинг опухолевой ДНК в крови. Для пациентов и их семей послание осторожное, но обнадеживающее: ингибиторы KRAS открывают важную новую дверь в лечении рака поджелудочной железы, но предстоит еще много работы, чтобы превратить ранние сигналы в долговременную пользу.
Цитирование: Tiede, K.O.M., Teixeira, M.F., Moura, M. et al. Efficacy and safety signals from early-phase studies of KRAS inhibition in pancreatic cancer. Sci Rep 16, 13189 (2026). https://doi.org/10.1038/s41598-026-40757-3
Ключевые слова: рак поджелудочной железы, ингибиторы KRAS, таргетная терапия, клинические испытания, безопасность лекарств