Clear Sky Science · nl
Werkzaamheid en veiligheids-signalen uit vroegfaseonderzoeken naar KRAS-remming bij alvleesklierkanker
Waarom dit belangrijk is voor patiënten en families
Alvleesklierkanker behoort tot de dodelijkste vormen van kanker: de meeste patiënten leven slechts enkele maanden na de diagnose zodra de ziekte is uitgezaaid. Decennialang waren artsen vrijwel uitsluitend aangewezen op agressieve chemotherapie met beperkte meerwaarde. Dit artikel bespreekt een nieuw soort geneesmiddel dat rechtstreeks een cruciaal fout eiwit, KRAS genaamd, aanpakt; KRAS drijft de meeste alvleesklierkankers. Door resultaten van vroegfase klinische onderzoeken samen te brengen, stellen de onderzoekers een eenvoudige maar dringende vraag: werken deze nieuwe middelen goed genoeg, en zijn ze veilig genoeg, om het vooruitzicht voor mensen met deze ziekte te veranderen?
Een hardnekkige kanker en een langdurige blokkade
Pancreasductaal adenocarcinoom, de meest voorkomende vorm van alvleesklierkanker, is agressief en wordt vaak laat vastgesteld, wanneer chirurgie geen optie meer is. De standaardbehandelingen combineren meerdere chemotherapieën. Hoewel deze de levensduur licht kunnen verlengen, veroorzaken ze vaak ernstige bijwerkingen die dosisverlagingen of voortijdige stopzetting noodzakelijk maken. Bij bijna 90 procent van deze tumoren zijn mutaties in KRAS aanwezig, een moleculaire aan/uit-schakelaar die groeisignalen in cellen reguleert. Jarenlang werd KRAS als ‘onwerkbaar’ bestempeld omdat het oppervlak weinig plekken bood waar een geneesmiddel kon binden. Pogingen om KRAS indirect te blokkeren door andere delen van het signaalnetwerk aan te vallen, mislukten grotendeels in het verbeteren van uitkomsten.
Een nieuwe klasse geneesmiddelen richt zich op KRAS
Het beeld veranderde met de ontwikkeling van kleine moleculen die rechtstreeks aan gemuteerd KRAS kunnen binden en diens activiteit verstoren. KRAS schakelt normaal tussen een inactieve en een actieve vorm; kankerveroorzakende mutaties bevriezen het in de “aan”-stand, waardoor cellen voortdurend groeisignalen ontvangen. Verschillende experimentele middelen die nu worden getest, kunnen KRAS in de uit-stand vergrendelen, het aanvallen terwijl het aanstaat, of complexere driedelige structuren vormen die de functie uitschakelen. Omdat deze middelen verschillende vormen van hetzelfde eiwit herkennen, kunnen ze uiteenlopende sterktes, zwaktes en resistentiepatronen hebben. De auteurs betogen dat hun effecten niet als identiek mogen worden verondersteld en per middel beoordeeld moeten worden. 
Wat de vroegste onderzoeken laten zien
Om te begrijpen wat deze nieuwe geneesmiddelen tot nu toe bereiken, voerden de onderzoekers een systematische review en meta-analyse uit van zeven vroegfaseonderzoeken met in totaal 463 patiënten met gevorderde of gemetastaseerde alvleesklierkanker. Alle patiënten hadden minimaal één eerdere behandellijn gehad, waardoor hun ziekte bijzonder moeilijk te beheersen was. Slechts 293 patiënten konden worden geëvalueerd op tumorkrimp omdat velen geen volledige scans hadden of om uiteenlopende redenen waren uitgevallen. Gepoold over de beschikbare data zag ongeveer 29 procent van de evalueerbare patiënten hun tumor met een betekenisvolle mate krimpen. De resultaten waren opvallend consistent tussen de onderzoeken, wat suggereert dat toekomstige onderzoeken met soortgelijke middelen bij vergelijkbare patiënten waarschijnlijk vergelijkbare responspercentages zullen laten zien. Voor alvleesklierkanker — waar betekenisvolle krimp historisch zeldzaam is geweest — wordt dit activiteitsniveau als bemoedigend beschouwd, al blijft het ver verwijderd van een genezing.
Bijwerkingen en kanttekeningen bij de studies
Effectiviteit is slechts een deel van het verhaal; veiligheid telt even zwaar. Over de onderzoeken heen waren maag-darmklachten een van de meest voorkomende bijwerkingen. Ongeveer vier op de tien patiënten ervaarden diarree of misselijkheid. Toen de auteurs zich beperkten tot patiënten met alvleesklierkanker in studies die ziektespecifieke veiligheidsgegevens rapporteerden, waren de percentages vergelijkbaar of iets hoger. Het precieze patroon van bijwerkingen verschilde per middel, en sommige bredere onderzoeken die verschillende tumortypen door elkaar analyseerden, maakten geen aparte uitsplitsing voor alvleesklierkanker, wat het moeilijker maakt om duidelijke trends te zien. De auteurs vonden ook dat het algehele risico op bias in de opgenomen onderzoeken matig tot hoog was. Het ging om kleine, vroegfase, enkelarmige onderzoeken zonder controlegroepen, wat het onmogelijk maakt om met zekerheid te zeggen hoeveel beter patiënten het deden vergeleken met standaardzorg alleen. 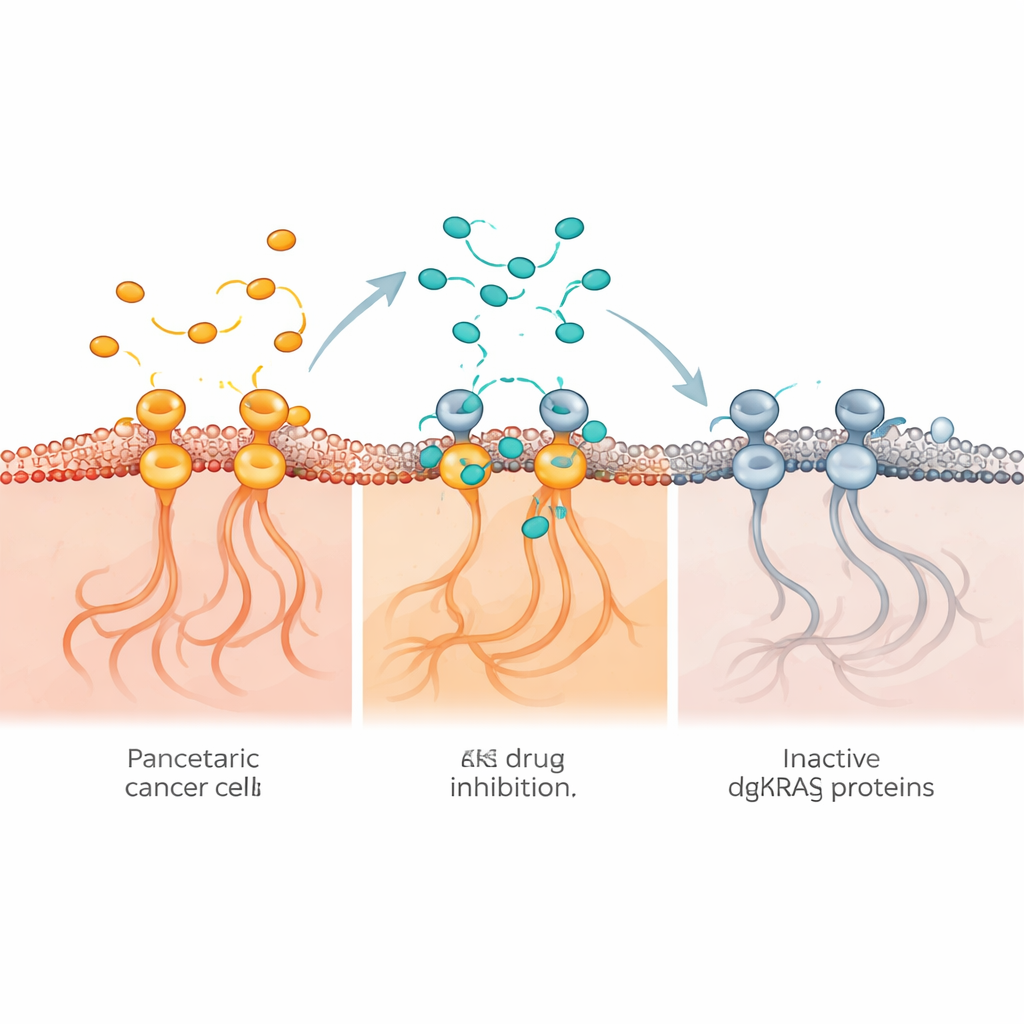
Waar het veld naartoe moet
Ondanks deze voorzichtigheden ondersteunt het gecombineerde bewijs een belangrijke conclusie: het is nu echt mogelijk om KRAS bij alvleesklierkanker medicamenteus aan te pakken, en dat kan bij sterk voorbehandelde patiënten echte, zij het bescheiden, tumorkrimp opleveren. De auteurs zien dit als een mijlpaal na decennia van frustratie. Tegelijkertijd zijn responsen voor de meeste patiënten nog niet duurzaam en blijven bijwerkingen een probleem. Het artikel pleit voor grotere, strengere en meer uniforme onderzoeken die specifieke KRAS-mutaties koppelen aan specifieke middelen, deze middelen verstandig combineren met immunotherapieën en andere gerichte behandelingen, en moderne biomarkers zoals bloedgebaseerde tumordna-tracking integreren. Voor patiënten en families is de boodschap voorzichtig maar hoopvol: KRAS-remmers openen een belangrijke nieuwe deur in de zorg voor alvleesklierkanker, maar er is nog veel werk nodig om vroege signalen om te zetten in blijvend voordeel.
Bronvermelding: Tiede, K.O.M., Teixeira, M.F., Moura, M. et al. Efficacy and safety signals from early-phase studies of KRAS inhibition in pancreatic cancer. Sci Rep 16, 13189 (2026). https://doi.org/10.1038/s41598-026-40757-3
Trefwoorden: alvleesklierkanker, KRAS-remmers, gerichte therapie, klinische onderzoeken, medicijnveiligheid