Clear Sky Science · pl
Wskaźniki skuteczności i sygnały bezpieczeństwa z badań wczesnych faz nad inhibicją KRAS w raku trzustki
Dlaczego ma to znaczenie dla pacjentów i ich rodzin
Rak trzustki należy do najgroźniejszych nowotworów — większość pacjentów żyje zaledwie kilka miesięcy po rozpoznaniu, gdy choroba się rozprzestrzeni. Przez dekady lekarze musieli opierać się niemal wyłącznie na toksycznej chemioterapii, która przynosi ograniczone korzyści. Ten artykuł przygląda się nowemu typowi leków, które bezpośrednio celują w kluczowe, wadliwe białko zwane KRAS, napędzające większość raków trzustki. Zbierając wyniki z badań klinicznych we wczesnych fazach, autorzy stawiają proste, lecz pilne pytanie: czy te nowe leki działają na tyle dobrze i są na tyle bezpieczne, aby zmienić rokowania osób dotkniętych tą chorobą?
Trudny nowotwór i długoletnia przeszkoda
Pancreatic ductal adenocarcinoma (gruczolakorak przewodowy trzustki), najczęstszy typ raka trzustki, jest agresywny i często rozpoznawany późno, gdy operacja nie wchodzi już w grę. Standardowe leczenie farmakologiczne łączy kilka chemioterapii. Choć mogą one nieco wydłużyć przeżycie, często powodują silne działania niepożądane, które zmuszają do zmniejszania dawek lub przerwania terapii. Niemal 90 procent tych guzów nosi mutacje w genie KRAS — molekularnym przełączniku on–off kontrolującym sygnały wzrostu w komórkach. Przez lata KRAS uznawano za „niedający się zahamować” (undruggable), ponieważ jego powierzchnia oferowała niewiele miejsc, do których lek mógłby się przyczepić. W rezultacie próby pośredniego blokowania KRAS, uderzając w inne elementy jego sieci sygnałowej, w dużej mierze nie poprawiały wyników.
Nowa klasa leków celuje w KRAS
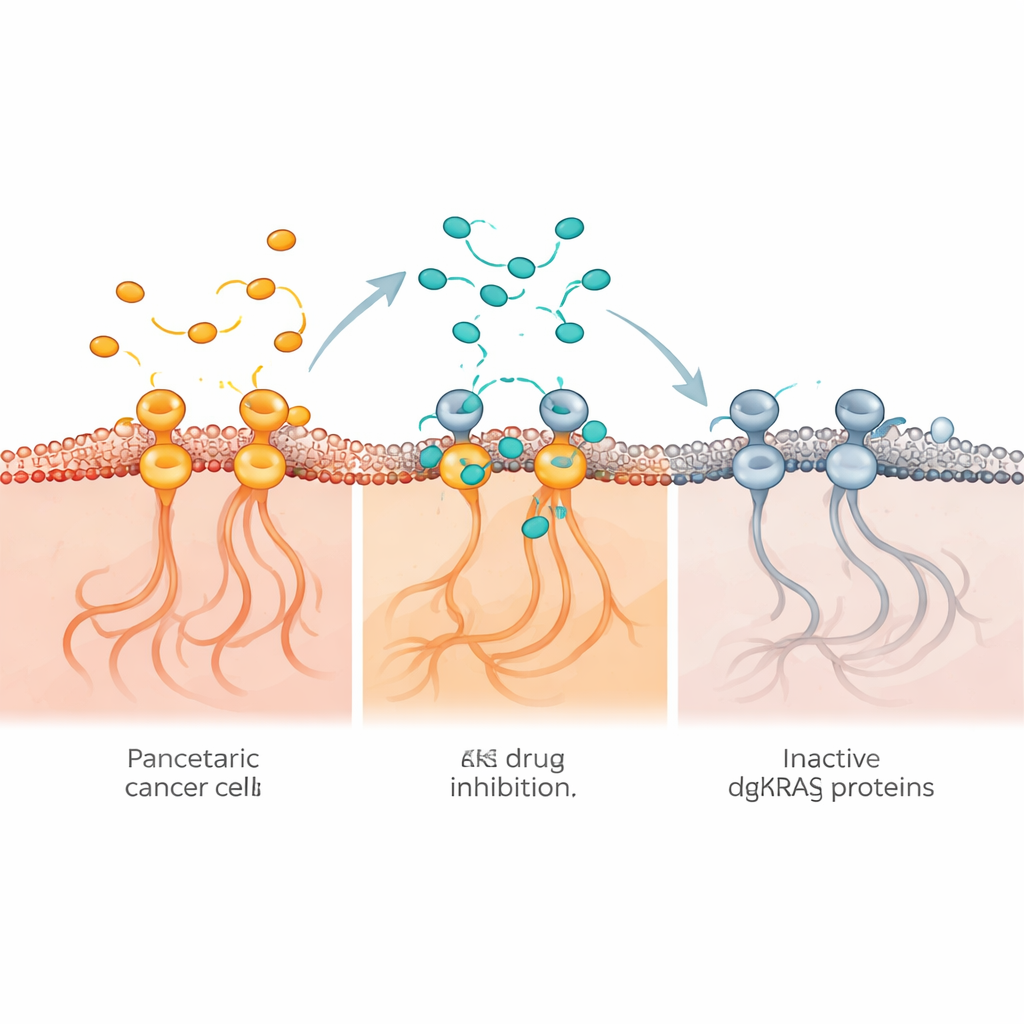
Obraz ten zmienił się wraz z wynalezieniem małych cząsteczek, które mogą wiązać się bezpośrednio z zmutowanym KRAS i zakłócać jego aktywność. KRAS normalnie przełącza się między formą nieaktywną a aktywną; mutacje powodujące raka „zamrażają” go w pozycji „włączonej”, stale nakazując komórkom wzrost. Różne badane obecnie eksperymentalne leki potrafią zablokować KRAS w stanie wyłączonym, atakować go, gdy jest w stanie włączonym, albo tworzyć bardziej złożone trójczłonowe struktury, które unieszkodliwiają jego funkcję. Ponieważ leki te rozpoznają różne kształty tego samego białka, mogą mieć odmienne mocne i słabe strony oraz różne wzory oporności. Autorzy argumentują, że ich efektów nie można zakładać jako identycznych i należy je oceniać dla każdego leku osobno. 
Co wykazują wczesne badania
Aby zrozumieć, co te nowe leki osiągają dotychczas, badacze przeprowadzili przegląd systematyczny i metaanalizę siedmiu badań we wczesnych fazach, obejmujących 463 pacjentów z zaawansowanym lub przerzutowym rakiem trzustki. Wszyscy pacjenci otrzymali co najmniej jedną wcześniejszą linię leczenia, co sprawia, że ich choroba była szczególnie trudna do opanowania. Tylko 293 pacjentów mogło zostać ocenionych pod kątem zmniejszenia guza, ponieważ wielu brakowało pełnych badań obrazowych albo zrezygnowali z udziału z różnych powodów. Łącząc dostępne dane, około 29 procent ocenianych pacjentów doświadczyło istotnego zmniejszenia guza. Wyniki były zadziwiająco spójne między badaniami, co sugeruje, że przyszłe próby z podobnymi lekami u podobnych pacjentów prawdopodobnie pokażą zbliżone wskaźniki odpowiedzi. Dla raka trzustki — gdzie znaczące zmniejszenie guza historycznie było rzadkie — ten poziom aktywności jest uznawany za zachęcający, choć wciąż daleki od wyleczenia.
Działania niepożądane i zastrzeżenia do badań
Skuteczność to tylko część historii; bezpieczeństwo jest równie ważne. W badaniach najczęściej występowały dolegliwości żołądkowo-jelitowe. Około czterech na dziesięciu pacjentów doświadczyło biegunki lub nudności. Gdy autorzy skupili się wyłącznie na pacjentach z rakiem trzustki w badaniach raportujących dane bezpieczeństwa specyficzne dla tego nowotworu, wskaźniki były podobne lub nieco wyższe. Dokładny wzór działań niepożądanych różnił się między lekami, a niektóre szersze badania mieszające różne typy nowotworów nie przedstawiały oddzielnie danych dla raka trzustki, co utrudnia wykrycie jasnych trendów. Autorzy zauważyli również, że ogólne ryzyko biasu w włączonych badaniach było umiarkowane do wysokiego. Były to małe, wczesnofazowe próby jednokierunkowe bez grup porównawczych, co uniemożliwia stwierdzenie z pewnością, o ile lepiej pacjenci radzili sobie niż przy standardowej opiece.
Dokąd zmierza dziedzina
Mimo tych zastrzeżeń zebrane dowody wspierają kluczowy wniosek: teraz naprawdę możliwe jest farmakologiczne zahamowanie KRAS w raku trzustki, a takie podejście może przynieść realne, choć umiarkowane, zmniejszenie guza u pacjentów silnie wcześniej leczonych. Autorzy postrzegają to jako przełom po dekadach frustracji. Jednocześnie odpowiedzi nie są jeszcze trwałe u większości pacjentów, a działania niepożądane wciąż stanowią problem. Artykuł wzywa do większych, bardziej rygorystycznych i bardziej jednorodnych badań, które dopasują konkretne mutacje KRAS do konkretnych leków, rozsądnie połączą te środki z immunoterapiami i innymi terapiami celowanymi oraz włączą nowoczesne markery, takie jak śledzenie nowotworowego DNA we krwi. Dla pacjentów i rodzin przekaz jest ostrożny, ale pełen nadziei: inhibitory KRAS otwierają ważne nowe drzwi w opiece nad rakiem trzustki, ale wciąż trzeba wykonać dużo pracy, aby przemienić wczesne sygnały w trwałe korzyści.
Cytowanie: Tiede, K.O.M., Teixeira, M.F., Moura, M. et al. Efficacy and safety signals from early-phase studies of KRAS inhibition in pancreatic cancer. Sci Rep 16, 13189 (2026). https://doi.org/10.1038/s41598-026-40757-3
Słowa kluczowe: rak trzustki, inhibitory KRAS, terapia celowana, badania kliniczne, bezpieczeństwo leków