Clear Sky Science · ru
Визуализация и генетически подтверждённая ассоциация функции глимфатической системы и многорегиональных характеристик мозга с болезнью Паркинсона
Почему это исследование очистки мозга важно
Болезнь Паркинсона наиболее известна тремором и скованностью, но задолго до появления этих симптомов в глубине мозга уже разворачиваются тонкие изменения. Это исследование изучает скрытую «службу уборки» мозга, которая помогает удалять отходы, и показывает, как её нарушение — вместе с микроскопическими изменениями ткани мозга — может сигнализировать о болезни Паркинсона за годы до того, как это обнаружат существующие тесты. Понимание и неинвазивное измерение этих изменений могут открыть путь к более ранней диагностике и более прицельному лечению.
Ночная бригада уборщиков мозга
Наш мозг постоянно производит продукты распада, которые нужно удалять, включая белки вроде альфа-синуклеина, способные слипаться и повреждать нейроны при болезни Паркинсона. Недавно описанная сеть, называемая глимфатической системой, циркулирует жидкость вдоль сосудов, чтобы смывать эти отходы. Авторы использовали показатель на основе диффузионной МРТ, известный как ALPS-индекс, чтобы оценить, насколько хорошо работает эта система очистки. Они также применили другую МРТ-метрику — свободную воду (free water), которая отражает долю свободно подвижной жидкости в разных областях мозга — признак микроскопического повреждения, отёка или воспаления. Сочетая эти два взгляда на мозг, исследователи задали вопрос: можно ли лучше обнаружить раннюю болезнь Паркинсона, и подскажут ли генетические данные, какие именно области мозга действительно вносят вклад в риск?
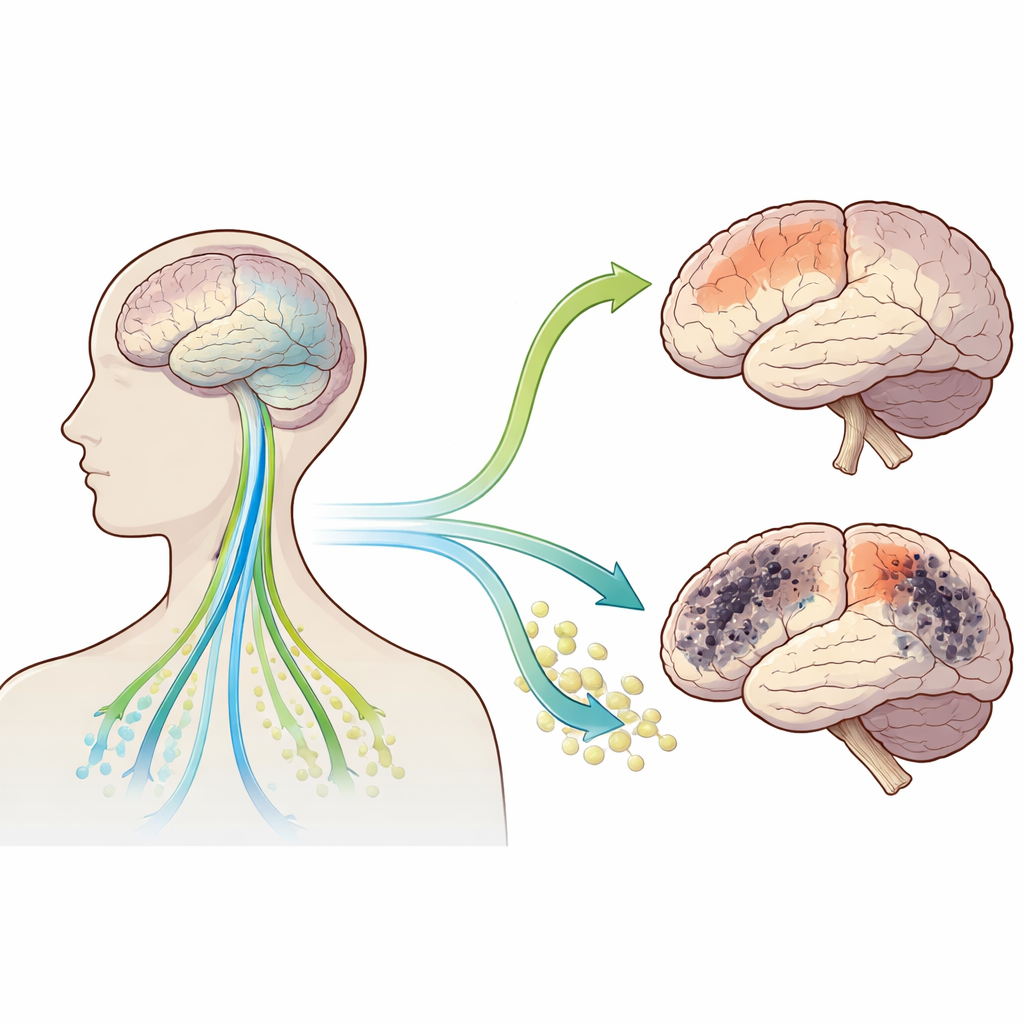
Что показали сканы мозга
Исследователи проанализировали данные 118 человек с ранней болезнью Паркинсона и 58 здоровых добровольцев в крупном международном исследовании. У пациентов с Паркинсоном наблюдался более низкий ALPS-индекс, то есть худшая видимая функция глимфатической системы, и повышенное значение свободной воды в нескольких областях мозга. Наиболее выраженные изменения свободной воды отмечались в височной доле, значительные повышения также зафиксированы во лобной, теменной, затылочной долях и мозжечке, тогда как более глубокие структуры, такие как хвостатое ядро и таламус, особо не отличались. Более низкий ALPS-индекс связывался с худшими двигательными показателями, что указывает на то, что снижение «уборки» мозга коррелирует с более тяжёлыми моторными проблемами даже на ранней стадии.
Построение лучшей модели раннего предупреждения
Далее команда проверила, насколько эти МРТ-показатели умеют различать пациентов с Паркинсоном и здоровых контрольных участников. По отдельности и ALPS-индекс, и свободная вода в височной доле демонстрировали умеренную прогностическую силу. При добавлении к базовым данным — возрасту, полу и образованию — каждый из показателей улучшал точность простой клинической модели. Но реальный прирост далось при комбинировании ALPS-индекса и свободной воды височной доли: вместе они обеспечили наибольшую точность оценки риска, превосходя каждый показатель по отдельности. С помощью этой пары маркеров авторы создали визуальный инструмент оценки, называемый номограммой, который переводит значения скана человека в индивидуальную вероятность наличия болезни Паркинсона и показывает хорошую внутреннюю согласованность при статистической проверке.
Что генетика говорит о уязвимых областях мозга
Чтобы выйти за рамки простой ассоциации, исследователи обратились к генетической стратегии, называемой менделевской рандомизацией, которая использует естественно встречающиеся генетические различия как своего рода «встроенный эксперимент». Используя крупные геномные наборы данных, они проверяли, действительно ли наследуемые признаки, связанные с конкретными структурами мозга, способствуют возникновению болезни Паркинсона. Они обнаружили, что несколько структурных характеристик, особенно во лобной и височной долях, показали положительную причинную связь с риском Паркинсона. Другими словами, генетические варианты, которые сдвигают структуру этих областей в определённом направлении, также были связаны с более высокой вероятностью развития болезни. Удивительно, но сам ALPS-индекс не продемонстрировал ясного генетического причинного эффекта на начало Паркинсона, что позволяет предположить, что снижение глимфатической функции может быть важнее для скорости прогрессирования болезни, чем для её триггера.
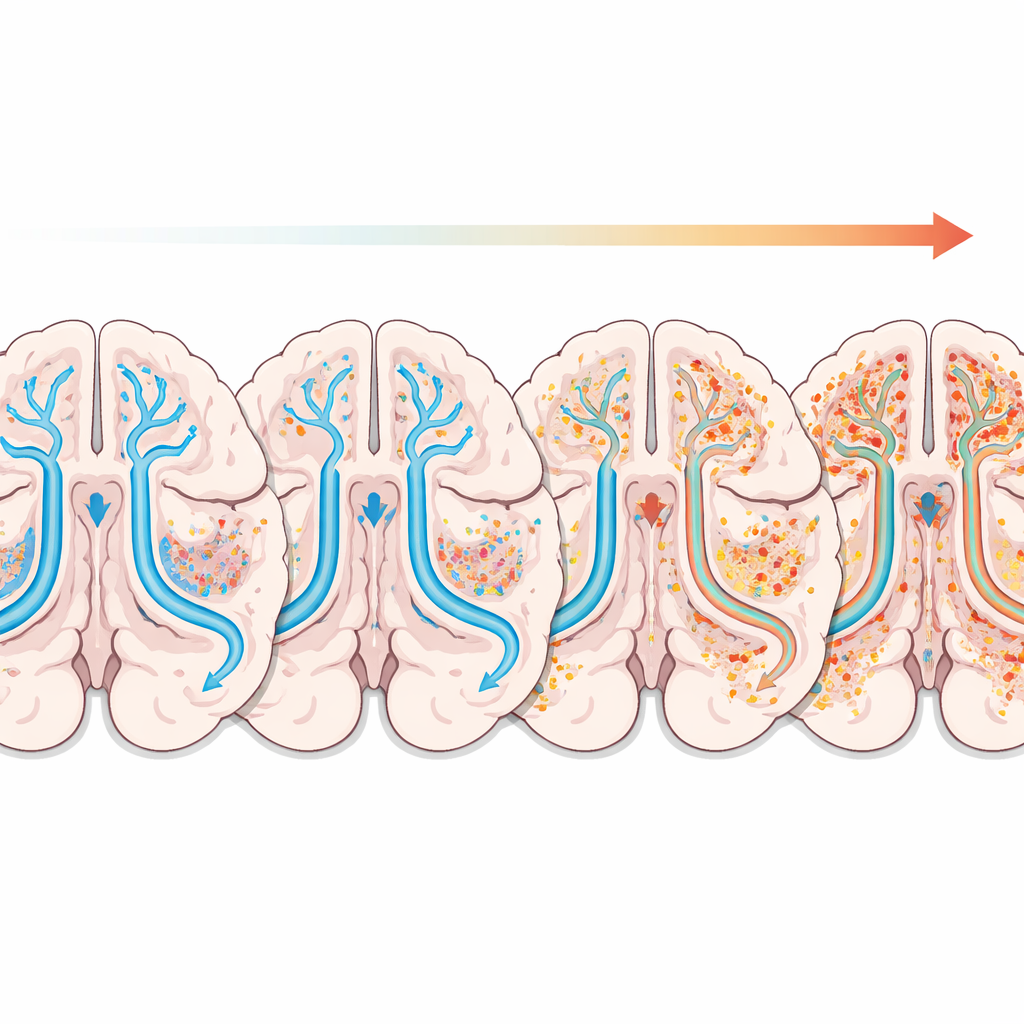
Что это значит для будущей помощи пациентам
В совокупности результаты рисуют картину, в которой ослабление системы очистки мозга и ранние микроструктурные изменения — особенно во фронто-височных областях — идут в ногу с болезнью Паркинсона. Хотя комбинированная модель визуализации пока недостаточно точна, чтобы служить самостоятельным диагностическим тестом, она может стать ценным дополнением, когда симптомы неясны и врачам нужно дополнительное подтверждение. Работа также выделяет фронтотемпоральные области как перспективные мишени для будущих терапий, направленных на замедление когнитивных и эмоциональных нарушений при болезни Паркинсона. При проведении более крупных и длительных исследований, стандартизации методов сканирования и совершенствовании инструментов визуализации, этот взгляд на очистку мозга может способствовать смещению ухода при Паркинсоне в сторону более раннего выявления и персонализированных вмешательств.
Цитирование: Ye, Z., Lin, Y., Lu, Y. et al. Imaging and genome-supported association of glymphatic system function and multiregional brain characteristics with Parkinson’s disease. npj Parkinsons Dis. 12, 103 (2026). https://doi.org/10.1038/s41531-026-01314-x
Ключевые слова: Болезнь Паркинсона, мозговая визуализация, глимфатическая система, височная доля, ранняя диагностика