Clear Sky Science · pl
Obrazowanie i powiązania genetyczne funkcji układu glimfatycznego oraz wielomiejscowych cech mózgu z chorobą Parkinsona
Dlaczego to badanie oczyszczania mózgu ma znaczenie
Choroba Parkinsona jest najbardziej znana z drżeń i sztywności, ale na długo przed pojawieniem się tych objawów w głębi mózgu zachodzą już subtelne zmiany. Badanie to przygląda się ukrytej „usłudze sprzątającej” w mózgu, która pomaga usuwać odpady, i pokazuje, jak jej upadek — wraz z drobnymi zmianami w tkance mózgowej — może sygnalizować chorobę Parkinsona na wiele lat przed wykrywalnością przez obecne testy. Niemalinwazyjne rozumienie i mierzenie tych zmian mogłoby otworzyć drogę do wcześniejszej diagnozy i dokładniej ukierunkowanego leczenia.
Nocna załoga sprzątająca mózg
Nasz mózg nieustannie wytwarza produkty odpadowe, które trzeba usuwać, w tym białka takie jak alfa-synukleina, mogące się agregować i uszkadzać komórki nerwowe w chorobie Parkinsona. Niedawno opisana sieć, zwana układem glimfatycznym, cyrkuluje płyn wzdłuż naczyń krwionośnych, by wypłukiwać te odpady. Autorzy wykorzystali miarę z dyfuzyjnego badania MRI znaną jako wskaźnik ALPS, aby oszacować sprawność tego systemu oczyszczania. Użyli też innej miary MRI, zwanej wolną wodą, która obrazuje ilość swobodnie poruszającego się płynu w różnych regionach mózgu — sygnał mikroskopowych uszkodzeń, obrzęku lub zapalenia. Łącząc te dwa spojrzenia na mózg, zespół zapytał: czy można lepiej wykrywać wczesną chorobę Parkinsona i czy genetyka wskaże, które obszary mózgu rzeczywiście przyczyniają się do ryzyka?
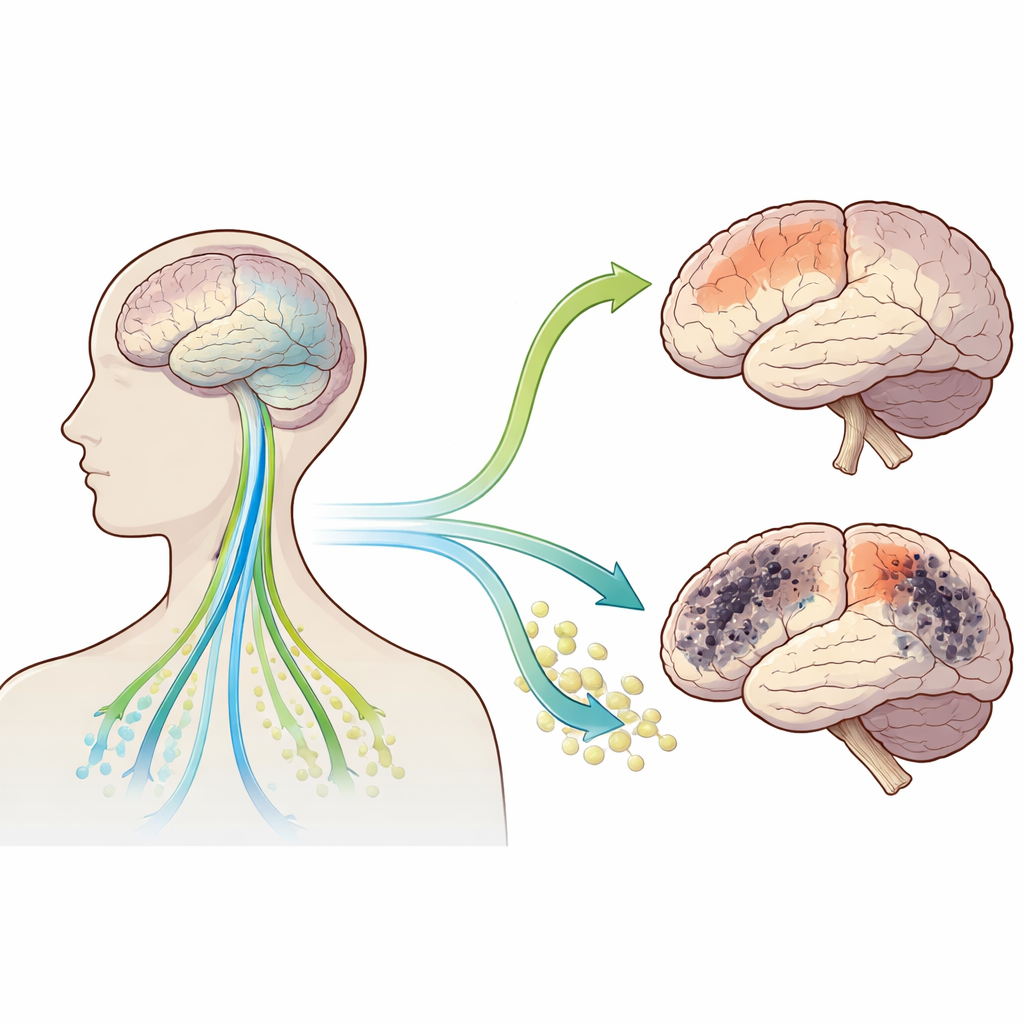
Co ujawniły skany mózgu
Naukowcy przeanalizowali dane od 118 osób z wczesną chorobą Parkinsona oraz 58 zdrowych ochotników w dużym międzynarodowym badaniu. Osoby z Parkinsonem miały niższy wskaźnik ALPS, co oznacza gorszą pozorną funkcję glimfatyczną, oraz wyższy poziom wolnej wody w kilku regionach mózgu. Najsilniejsze zmiany wolnej wody pojawiły się w płacie skroniowym, z zauważalnymi wzrostami także w płatach czołowym, ciemieniowym, potylicznym oraz w móżdżku, podczas gdy głębsze struktury, takie jak jądro ogoniaste i wzgórze, nie różniły się znacznie. Niższy wskaźnik ALPS wiązał się z gorszymi wynikami w ocenie ruchowej, sugerując, że zmniejszone oczyszczanie mózgu idzie w parze z poważniejszymi zaburzeniami motorycznymi, nawet we wczesnym stadium.
Budowanie lepszego modelu wczesnego ostrzegania
Następnie zespół sprawdził, jak dobrze te miary MRI potrafią odróżnić pacjentów z Parkinsonem od zdrowych kontrol. Samodzielnie zarówno wskaźnik ALPS, jak i wolna woda w płacie skroniowym wykazały umiarkowaną moc predykcyjną. Po dodaniu do podstawowych informacji, takich jak wiek, płeć i wykształcenie, każda z miar poprawiła dokładność prostego modelu klinicznego. Prawdziwy zysk uzyskano jednak łącząc wskaźnik ALPS z wolną wodą w płacie skroniowym: razem dały najdokładniejszą ocenę ryzyka, przewyższając każdą z miar osobno. Wykorzystując tę parę markerów obrazowych, autorzy zbudowali wizualne narzędzie punktacyjne, zwane nomogramem, które zamienia wartości ze skanu danej osoby na indywidualne prawdopodobieństwo występowania choroby Parkinsona, z dobrą wewnętrzną spójnością w testach statystycznych.
Co genetyka mówi o wrażliwych regionach mózgu
Aby wyjść poza prostą asocjację, badacze zwrócili się ku strategii genetycznej zwanej randomizacją Mendla, która wykorzystuje występujące naturalnie różnice genetyczne jako rodzaj „wbudowanego eksperymentu”. Korzystając z dużych zestawów danych z całego genomu, sprawdzili, czy dziedziczne cechy związane z określonymi strukturami mózgu faktycznie przyczyniają się do choroby Parkinsona. Stwierdzili, że kilka cech strukturalnych, zwłaszcza w płatach czołowym i skroniowym, wykazywało pozytywny związek przyczynowy z ryzykiem Parkinsona. Innymi słowy, warianty genetyczne, które przesuwają strukturę tych obszarów w określonych kierunkach, były również powiązane z wyższym prawdopodobieństwem rozwoju choroby. Zaskakująco, sam wskaźnik ALPS nie wykazał wyraźnego genetycznego efektu przyczynowego na wystąpienie Parkinsona, co sugeruje, że zmniejszona funkcja glimfatyczna może mieć większe znaczenie dla tempa postępu choroby niż dla jej wywołania.
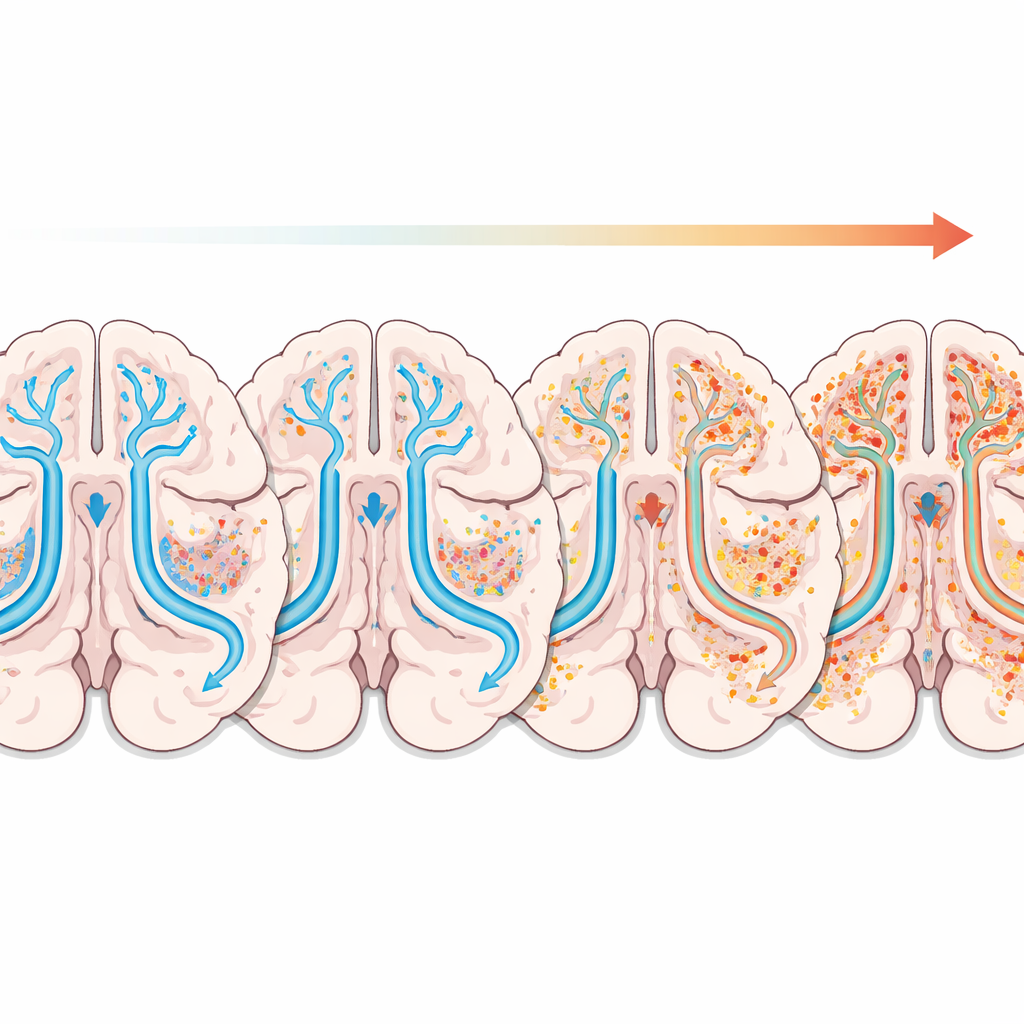
Co to oznacza dla przyszłej opieki
Podsumowując, wyniki malują obraz, w którym słabnący system oczyszczania mózgu i wczesne mikrostrukturalne zmiany — zwłaszcza w płatach czołowym i skroniowym — towarzyszą chorobie Parkinsona. Chociaż łączony model obrazowy nie jest wystarczająco dokładny, by służyć jako samodzielny test diagnostyczny, może stać się wartościowym uzupełnieniem, gdy objawy są niejasne, a lekarzom potrzebne są dodatkowe dowody. Praca ta wskazuje także obszary czołowo-skroniowe jako obiecujące cele dla przyszłych terapii mających na celu spowolnienie zaburzeń poznawczych i emocjonalnych w chorobie Parkinsona. Przy większych i dłuższych badaniach, ujednoliconych metodach skanowania i udoskonalonych narzędziach obrazowania, ta perspektywa „oczyszczania mózgu” może przyczynić się do przesunięcia opieki nad Parkinsonem w stronę wcześniejszego wykrywania i bardziej spersonalizowanych interwencji.
Cytowanie: Ye, Z., Lin, Y., Lu, Y. et al. Imaging and genome-supported association of glymphatic system function and multiregional brain characteristics with Parkinson’s disease. npj Parkinsons Dis. 12, 103 (2026). https://doi.org/10.1038/s41531-026-01314-x
Słowa kluczowe: Choroba Parkinsona, obrazowanie mózgu, układ glimfatyczny, płat skroniowy, wczesna diagnostyka