Clear Sky Science · es
Imagenología y asociación respaldada por genómica de la función del sistema glinfático y características cerebrales multirregionales con la enfermedad de Parkinson
Por qué importa este estudio sobre la limpieza del cerebro
La enfermedad de Parkinson es más conocida por los temblores y la rigidez, pero mucho antes de que aparezcan esos síntomas ya se están produciendo cambios sutiles en las profundidades del cerebro. Este estudio explora un “servicio de limpieza” oculto en el cerebro que ayuda a eliminar los desechos, y muestra cómo su deterioro—junto con microcambios en el tejido cerebral—puede señalar la enfermedad de Parkinson años antes de lo que detectan las pruebas actuales. Comprender y medir estos cambios de forma no invasiva podría abrir la puerta a un diagnóstico más temprano y a tratamientos más precisos.
El equipo de limpieza nocturno del cerebro
Nuestros cerebros producen constantemente desechos que deben ser eliminados, incluidos proteínas como la alfa-sinucleína, que pueden agregarse y dañar las neuronas en la enfermedad de Parkinson. Una red descrita recientemente, llamada sistema glinfático, hace circular líquido a lo largo de los vasos sanguíneos para enjuagar estos residuos. Los autores emplearon una medida de resonancia magnética por difusión conocida como índice ALPS para estimar qué tan bien funciona este sistema de limpieza. También utilizaron otra medida de RM, denominada agua libre, que captura la cantidad de fluido en movimiento libre presente en distintas regiones cerebrales—un indicador de daño microscópico, edema o inflamación. Al combinar estas dos perspectivas del cerebro, el equipo se preguntó: ¿podemos detectar mejor la enfermedad de Parkinson en fase temprana, y puede la genética decirnos qué regiones cerebrales contribuyen de verdad al riesgo?
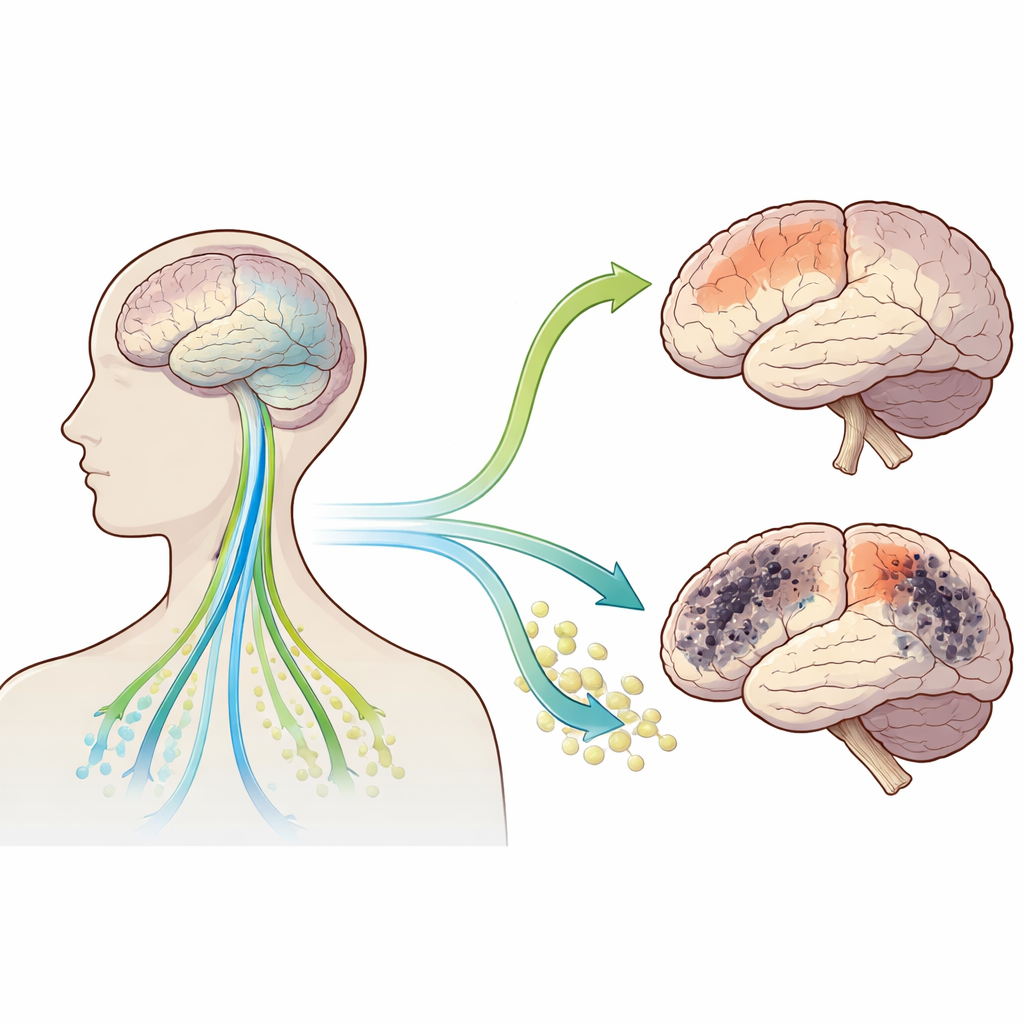
Qué revelaron las exploraciones cerebrales
Los investigadores analizaron datos de 118 personas con Parkinson en fase temprana y 58 voluntarios sanos en un gran estudio internacional. Las personas con Parkinson mostraron un índice ALPS más bajo, lo que indica una aparente función glinfática peor, y mayor agua libre en varias regiones cerebrales. Los cambios más pronunciados en agua libre aparecieron en el lóbulo temporal, con aumentos notables también en los lóbulos frontal, parietal, occipital y en el cerebelo, mientras que estructuras más profundas como el caudado y el tálamo no presentaron grandes diferencias. Un índice ALPS más bajo se asoció con puntuaciones de movilidad peores, lo que sugiere que la reducción de la limpieza cerebral va de la mano con problemas motores más severos, incluso en una etapa temprana.
Construyendo un mejor modelo de alerta temprana
A continuación, el equipo probó qué tan bien estas medidas de RM podían distinguir a los pacientes con Parkinson de los controles sanos. Por separado, tanto el índice ALPS como el agua libre del lóbulo temporal mostraron una potencia predictiva moderada. Al añadirse a información básica como edad, sexo y nivel educativo, cada medida mejoró la precisión de un modelo clínico simple. Pero la ganancia real provino de combinar el índice ALPS con el agua libre del lóbulo temporal: juntos produjeron la estimación de riesgo más precisa, superando a cada medida por separado. Usando este par de marcadores por imagen, los autores construyeron una herramienta de puntuación visual, llamada nomograma, que traduce los valores del escáner de una persona en una probabilidad individualizada de tener enfermedad de Parkinson, con buena consistencia interna en las comprobaciones estadísticas.
Qué dice la genética sobre las regiones cerebrales vulnerables
Para ir más allá de la simple asociación, los investigadores recurrieron a una estrategia genética llamada randomización mendeliana, que utiliza diferencias genéticas naturales como una especie de “experimento incorporado”. Basándose en grandes conjuntos de datos genómicos a escala, preguntaron si los rasgos heredados vinculados a estructuras cerebrales específicas realmente contribuyen a causar la enfermedad de Parkinson. Hallaron que varias características estructurales, especialmente en los lóbulos frontal y temporal, mostraban una relación causal positiva con el riesgo de Parkinson. En otras palabras, variantes genéticas que empujan la estructura de estas regiones en determinadas direcciones se asociaban también con mayores probabilidades de desarrollar la enfermedad. Sorprendentemente, el propio índice ALPS no mostró un efecto causal genético claro sobre la aparición de Parkinson, lo que sugiere que la función glinfática reducida puede ser más importante para la velocidad de progresión de la enfermedad que para desencadenarla inicialmente.
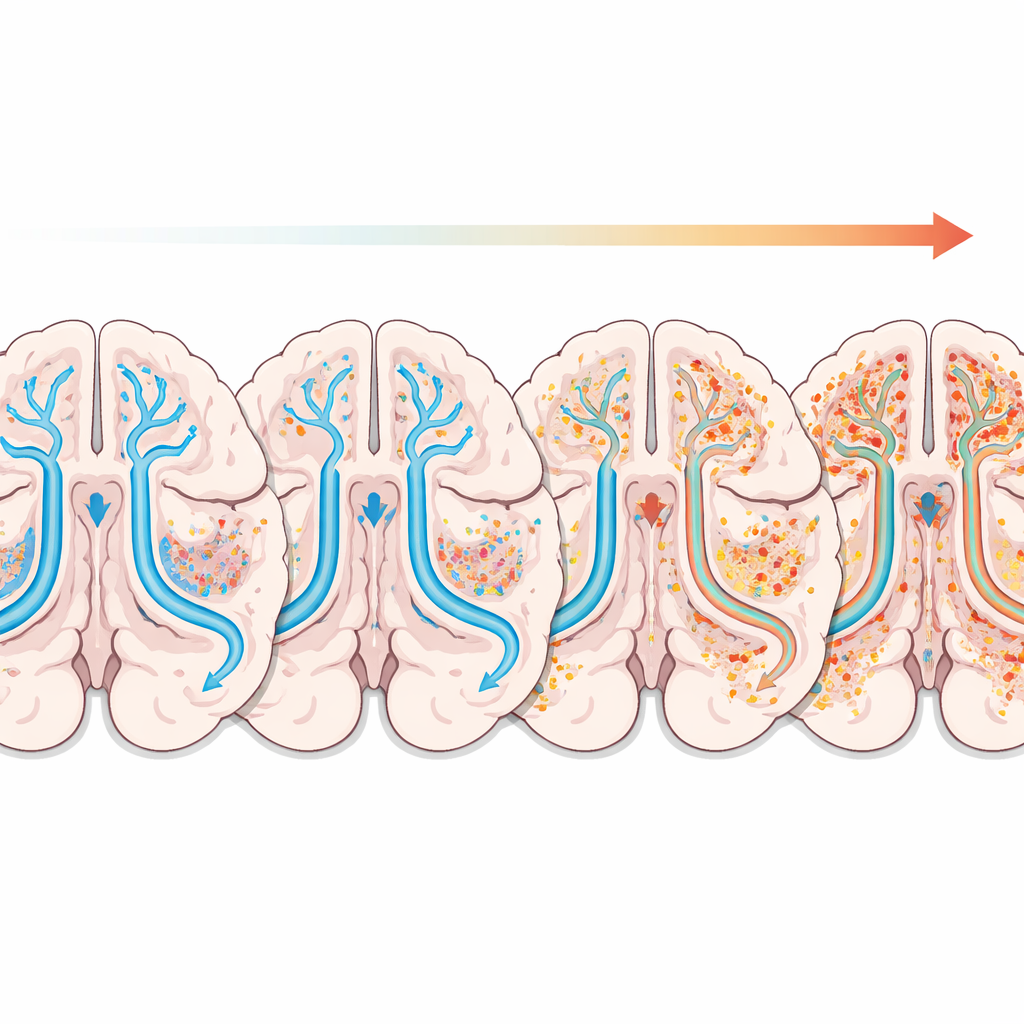
Qué significa esto para la atención futura
En conjunto, los hallazgos dibujan un panorama en el que un sistema de limpieza cerebral en declive y cambios microestructurales tempranos—especialmente en los lóbulos frontal y temporal—viajan junto con la enfermedad de Parkinson. Aunque el modelo de imagen combinado no es lo bastante exacto para servir como prueba diagnóstica independiente, podría convertirse en un complemento valioso cuando los síntomas son vagos y los médicos necesitan evidencia adicional. El trabajo también destaca las regiones frontotemporales como objetivos prometedores para futuras terapias orientadas a frenar los problemas cognitivos y emocionales en la enfermedad de Parkinson. Con estudios más amplios y a más largo plazo, métodos de escaneo estandarizados y herramientas de imagen refinadas, esta perspectiva centrada en la limpieza cerebral podría ayudar a desplazar la atención del Parkinson hacia una detección más temprana y una intervención más personalizada.
Cita: Ye, Z., Lin, Y., Lu, Y. et al. Imaging and genome-supported association of glymphatic system function and multiregional brain characteristics with Parkinson’s disease. npj Parkinsons Dis. 12, 103 (2026). https://doi.org/10.1038/s41531-026-01314-x
Palabras clave: Enfermedad de Parkinson, imagen cerebral, sistema glinfático, lóbulo temporal, diagnóstico temprano