Clear Sky Science · ru
Ингибирование MDM2 препаратом алризомадлин (APG-115) при TP53 дикого типа в раках слюнных желез: клиническое исследование фазы I
Новая надежда при редком раке головы и шеи
Опухоли слюнных желез редки, часто возникают без предупреждения и могут вернуться или дать метастазы спустя годы после первичного лечения. У пациентов с распространённым заболеванием мало проверенных лекарственных вариантов, и большинство терапий направлено скорее на облегчение симптомов, чем на долговременный контроль рака. В этом исследовании тестируют таблетку алризомадлин, призванную вновь включить один из природных механизмов борьбы с опухолями, что может открыть новый путь для пациентов с ограниченными возможностями лечения.
Почему эти опухоли трудно лечить
Злокачественные опухоли слюнных желез составляют лишь малую часть опухолей головы и шеи, но при этом отличаются большим разнообразием. Наиболее распространённым подтипом в этом исследовании была аденоидно-кистозная карцинома — медленно прогрессирующая опухоль, которая может годами оставаться «спящей», а затем внезапно ускориться. Когда заболевание распространилось или вернулось в участки, куда нельзя применить операцию или лучевую терапию, врачи прибегают к системной терапии. Традиционные химиопрепараты и более новые средства, ориентированные на сосуды, дают скромное уменьшение опухолей и часто сопровождаются значительными побочными эффектами; ни один препарат формально не утверждён специально для этих пациентов. Поэтому исследователи оценивают не только уменьшение опухоли, но и продолжительность контроля её роста.
Включение природного «стража»
У многих солидных опухолей нарушён ключевой ген TP53, кодирующий белок, часто называемый «стражем генома». Рак слюнных желез необычен тем, что TP53 чаще всего остаётся интактным, но другой белок — MDM2 — может быть гиперактивен и выключать этого «стража». Алризомадлин — пероральный препарат, предназначенный блокировать MDM2, чтобы собственные защитные механизмы организма вновь могли замедлять или останавливать рост раковых клеток. Предшествующие исследования на мышах с трансляционными опухолями аденоидно-кистозной карциномы показали, что эта стратегия может уменьшать опухоли, особенно в комбинации с платиновой химиотерапией, что и послужило основанием для тестирования метода на пациентах.
Как проводилось исследование
В это исследование фазы I были включены взрослые пациенты с раком слюнных желез, у которых в опухолях подтверждали нормальный TP53 и которые за последний год продемонстрировали явный рост не менее чем на 20 процентов. Сорок пациентов получили по крайней мере одну дозу исследуемого лечения: 36 принимали только алризомадлин, а 4 — алризомадлин в комбинации с карбоплатином. Гибкая схема дозирования помогла определить дозу, сочетающую безопасность и потенциальную пользу. Главной ранней целью было выявление серьёзных побочных эффектов, ограничивающих дозу, а также мониторинг ответов опухоли, времени до прогрессирования и выживаемости.
Сигналы безопасности и побочные эффекты
Алризомадлин в монорежиме в целом переносился удовлетворительно. Среди 37 пациентов, получивших таблетку, у трёх отмечались серьёзные ранние побочные эффекты, попадавшие в строгие критерии ограничивающих дозу, включая кратковременное снижение количества белых кровяных телец и головокружение. У большинства пациентов наблюдалась связанная с лечением усталость, тошнота или изменения показателей крови, и примерно у двух третей был хотя бы один тяжёлый (3-й степени или выше) побочный эффект, но лишь немногие прекратили приём препарата из‑за токсичности. Напротив, при комбинировании алризомадлина с карбоплатином у всех четырёх пациентов появились тяжёлые побочные эффекты, у половины — наиболее выраженное падение показателей крови, что привело к прекращению комбинированной ветви исследования.
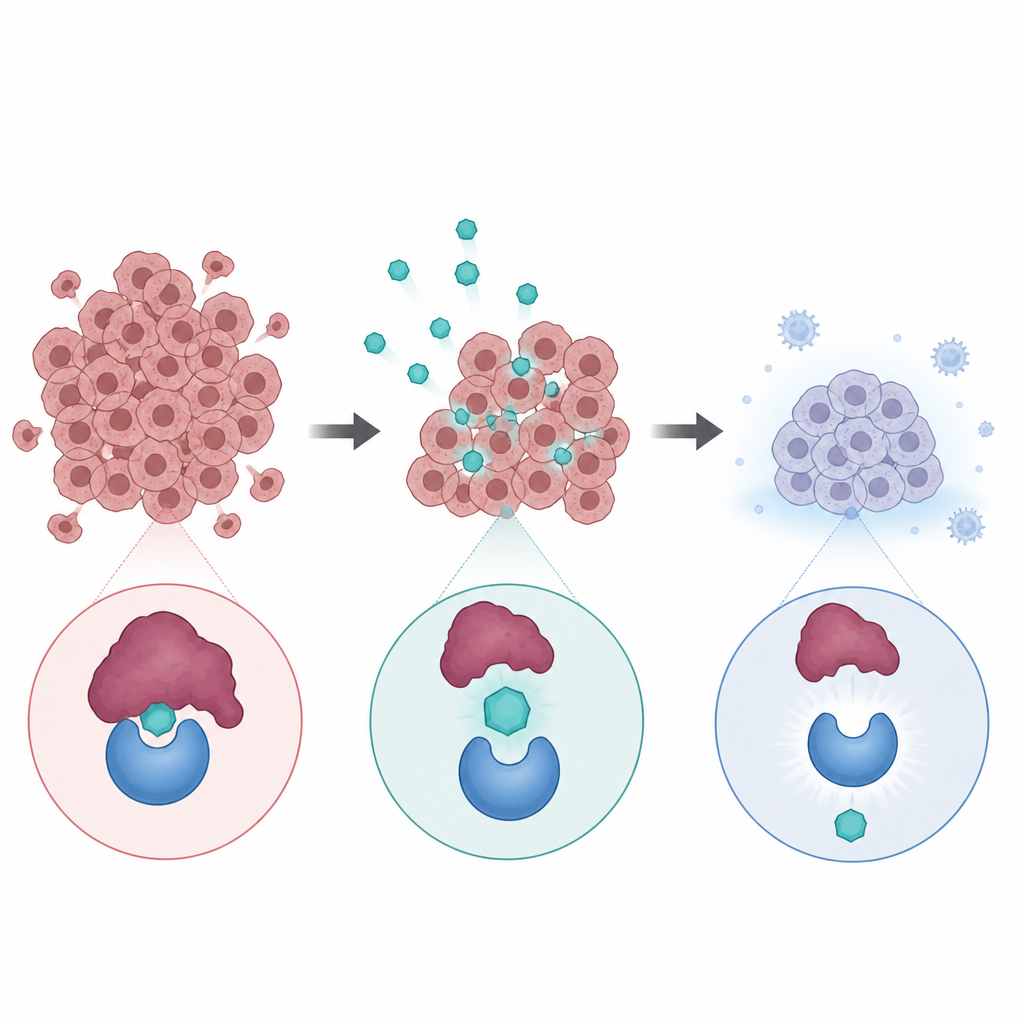
Что препарат сделал с опухолями
Среди 34 пациентов, принимавших алризомадлин достаточно долго для оценки ответа, у 15 процентов наблюдалось очевидное уменьшение опухоли, и почти 80 процентов имели стабилизацию заболевания, что дало общий контроль болезни более чем у 94 процентов. В какой‑то момент наблюдения у примерно трёх четвертей пациентов опухоли уменьшались. Типичное время до возобновления роста составило около девяти — десяти месяцев, и несколько пациентов оставались на лечении более года. Пациенты с аденоидно‑кистозной карциномой, составлявшие большинство участников, похоже, показали особенно благоприятные результаты: схожая частота ответов, но несколько более длительная медиана времени до прогрессирования по сравнению с другими типами рака слюнных желез.
Подсказки из ДНК опухоли
Исследователи также проанализировали хранимые образцы опухоли у подгруппы пациентов. Они подтвердили, что ни в одном из этих образцов не было мутаций TP53, что соответствует дизайну исследования. В целом опухоли демонстрировали относительно небольшое число генетических изменений, и не было обнаружено изменений в MDM2 или его близком партнёре MDM4. Окрасочные тесты для других маркёров, таких как MYB и ALDH1A1, не позволили явно отделить пациентов, получивших пользу, от тех, кто не ответил, что указывает на необходимость дальнейшей работы по поиску простых лабораторных тестов, предсказывающих наилучший ответ на алризомадлин.
Что это значит для пациентов
Для людей с распространёнными раками слюнных желез, особенно с аденоидно‑кистозной карциномой, это раннее исследование показывает, что алризомадлин в виде однотаблеточной терапии может удерживать опухоли под контролем несколько месяцев при управляемых побочных эффектах. Препарат не сработал у всех, а сочетание с стандартной химиотерапией оказалось чрезмерно токсичным при изучавшихся дозах, однако результаты укрепляют идею, что «пробуждение» собственных защитных путей организма может иметь клиническую ценность. Для подтверждения того, продлевает ли алризомадлин выживаемость или улучшает качество жизни, потребуются более крупные рандомизированные исследования — тем не менее эта работа представляет собой конкретный шаг в сторону более таргетированных опций для редкой группы пациентов, долгое время имевших ограниченные лечебные возможности.
Цитирование: Pearson, A.T., Muzaffar, J., Kirtane, K. et al. MDM2 Inhibition with Alrizomadlin (APG-115) in TP53 wild-type salivary gland cancers: a phase I clinical trial. Nat Commun 17, 4240 (2026). https://doi.org/10.1038/s41467-026-70653-3
Ключевые слова: рак слюнной железы, аденоидно-кистозная карцинома, ингибитор MDM2, исследование фазы I, таргетная терапия