Clear Sky Science · ru
Исследование активности гидролазы желчных солей у бактерий кишечника человека выявляет образование конъюгированных вторичных желчных кислот
Почему важна наша кишечная химия
Каждый раз, когда мы едим, организм выделяет в кишечник детергенты — желчные кислоты, которые помогают растворять жиры и транспортировать витамины в кровоток. Те же молекулы служат сигнальными молекулами, взаимодействуя с гормонами, формируя среду, в которой могут выживать те или иные микробы кишечника, и связаны с состояниями от повышенного холестерина до рака. В этом исследовании подробно изучают, как многочисленные обычные кишечные бактерии модифицируют желчные кислоты, и обнаруживают неожиданный путь, с помощью которого они образуют ранее недооценённые формы, способные влиять на здоровье человека.
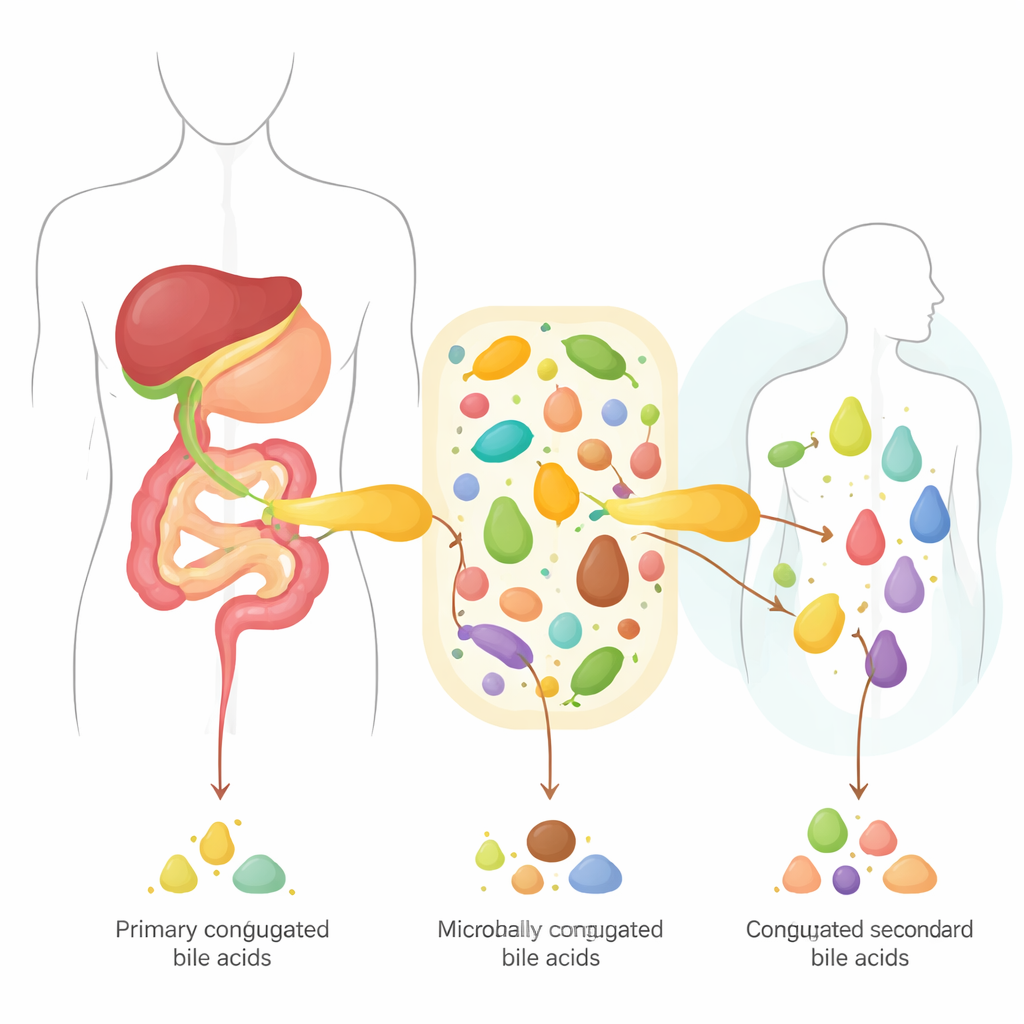
От простых детергентов к сложному химическому коктейлю
Желчные кислоты образуются в печени из холестерина и связываются с малыми молекулами — глицином или таурином. Их хранят в желчном пузыре и выбрасывают в тонкий кишечник во время приёма пищи, где они достигают высоких концентраций, прежде чем большинство снова всосётся и будет рециклировано в петле между кишечником и печенью. Остатки попадают в плотные сообщества кишечных бактерий, которые могут отщеплять глицин или таурин, а затем дополнительно перестраивать стержень желчной кислоты. Эти преобразования превращают относительно простой набор печёночных соединений в разнообразную химическую библиотеку, которая в зависимости от состава может защищать нас от болезней или способствовать им.
Насколько широко распространено ремоделирование желчи
Исследователи систематически протестировали 77 штаммов бактерий, представляющих основные группы, часто встречающиеся в кишечнике человека, чтобы узнать, как они обрабатывают пять типичных человеческих желчных кислот. С помощью современных методов химического анализа они показали, что более 70 процентов штаммов способны выполнять первый шаг — деконъюгацию, то есть удалять присоединённый глицин или таурин. Уровни активности и предпочтения варьировались: одни штаммы отдавали предпочтение тауриновым конъюгатам, другие — глициновым, а некоторые перерабатывали оба типа. Определённые группы, такие как бифидобактерии, энтерококки и многие виды Bacteroides, особенно эффективно проводили деконъюгацию и образовывали классические «вторичные» желчные кислоты, давно известные своим влиянием на метаболизм и риск рака.
Новые игроки: микробные прищёпки и обходные пути
Кроме простого отщепления, многие бактерии также повторно присоединяли желчные кислоты к широкому спектру аминокислот, создавая так называемые микробно конъюгированные желчные кислоты. Эта способность тесно коррелировала с высокой деконъюгационной активностью. Ещё более неожиданно команда неоднократно обнаруживала «конъюгированные вторичные желчные кислоты», которые по традиционной картине желчной химии не должны были возникать. Тщательные эксперименты с отслеживанием во времени и генетические тесты показали, что у нескольких видов ферменты, известные как гидроксистероидные дегидрогеназы, могут действовать непосредственно на стержень желчной кислоты, пока глицин или таурин всё ещё прикреплён. У одного ключевого вида кишечной микробиоты, Bacteroides thetaiotaomicron, удаление одного такого фермента полностью устраняло этот обходной путь, доказывая, что обычно он превращает печёночную желчную кислоту прямо в новый конъюгированный вторичный вариант, минуя свободный промежуточный продукт.
Командная работа микробов кишечника и доказательства в живых организмах
Исследование также рассмотрело, как разные бактерии сотрудничают. Когда штаммы с высокой деконъюгационной активностью выращивали совместно с B. thetaiotaomicron, объединённое сообщество могло выполнять многоэтапные преобразования, которые ни один вид по‑отдельности провести не мог, превращая простые конъюгированные желчные кислоты в каскад окисленных и эпимеризованных продуктов. Чтобы проверить, образуются ли эти необычные конъюгированные вторичные желчные кислоты в животных, учёные колонизировали безмикробных мышей либо нормальным, либо лишённым фермента штаммом B. thetaiotaomicron и добавляли в питьевую воду специфическую человеческую желчную кислоту. У мышей с нормальным штаммом в фекалиях накапливалась характерная конъюгированная вторичная желчная кислота, тогда как у животных с мутантным штаммом её не было, что сильно поддерживает идею о том, что этот обходной путь действует и в живом хозяине.
Что это значит для здоровья и будущих терапий
Десятилетиями в учебниках описывали метаболизм желчных кислот как однонаправленный конвейер: печень синтезирует конъюгированные желчные кислоты, бактерии сначала срывают их боковые цепи, а только затем перестраивают стержень. Эта работа опровергает эту линейную картину, показывая вместо неё разветвлённую сеть, где время и сила действия разных микробных ферментов определяют, станут ли желчные кислоты классическими вторичными формами, микробно реконъюгированными продуктами или недавно признанными конъюгированными вторичными вариантами. Поскольку разные виды желчных кислот могут по‑разному влиять на метаболизм, иммунитет и даже риск рака, детальная карта этой сети будет необходима для разработки диет, пробиотиков или лекарств, которые направляют желчную химию в сторону более здоровых исходов.
Цитирование: Lucas, L.N., Jillella, M., Cattaneo, L.E. et al. Investigation of bile salt hydrolase activity in human gut bacteria reveals production of conjugated secondary bile acids. Nat Commun 17, 3077 (2026). https://doi.org/10.1038/s41467-026-68556-4
Ключевые слова: микробиом кишечника, желчные кислоты, гидролаза желчных солей, микробный метаболизм, взаимодействие хозяина и микробов