Clear Sky Science · fr
Investigation de l’activité de la bile salt hydrolase chez les bactéries intestinales humaines révèle la production d’acides biliaires secondaires conjugués
Pourquoi la chimie de notre intestin compte
Chaque fois que nous mangeons, notre organisme libère dans l’intestin des détergents appelés acides biliaires pour aider à dissoudre les graisses et transporter les vitamines vers la circulation sanguine. Ces mêmes molécules servent aussi de signaux qui dialoguent avec nos hormones, déterminent quelles microbes peuvent coloniser notre intestin et sont associées à des affections allant de l’hypercholestérolémie au cancer. Cette étude examine en profondeur la manière dont de nombreuses bactéries intestinales courantes modifient les acides biliaires et révèle une voie inattendue par laquelle elles produisent des formes jusque‑là négligées susceptibles d’influencer la santé humaine.
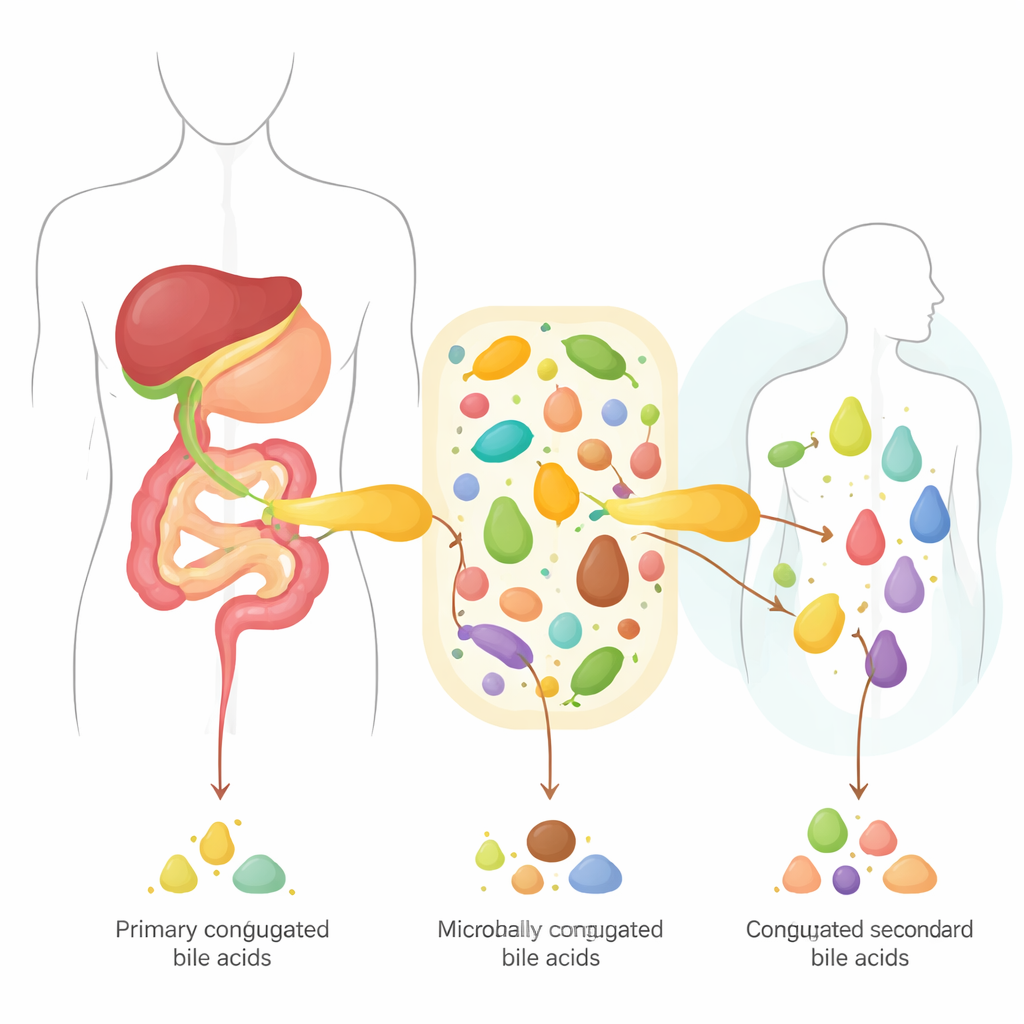
De détergents simples à une soupe chimique complexe
Les acides biliaires naissent dans le foie, où ils sont synthétisés à partir du cholestérol et conjugués à de petites molécules, la glycine ou la taurine. Ils sont stockés dans la vésicule biliaire et expulsés dans l’intestin grêle pendant un repas, atteignant des concentrations élevées avant que la plupart ne soient réabsorbés et recyclés dans une boucle entre l’intestin et le foie. Les restes rencontrent des communautés bactériennes denses, qui peuvent détacher le groupement glycine ou taurine puis remodeler davantage le noyau des acides biliaires. Ces transformations transforment un ensemble simple de composés produits par le foie en une librairie chimique diverse qui peut soit nous protéger des maladies, soit les favoriser, selon le mélange.
À quel point le remodelage biliaire est répandu
Les chercheurs ont testé systématiquement 77 souches bactériennes, représentant les principaux groupes couramment présents dans l’intestin humain, pour voir comment elles traitent cinq acides biliaires humains typiques. Grâce à des analyses chimiques avancées, ils ont montré que plus de 70 % des souches pouvaient réaliser la première étape, appelée déconjugaison, qui élimine l’attachement de la glycine ou de la taurine. Les niveaux d’activité et les préférences variaient : certaines souches privilégiaient les acides biliaires conjugués à la taurine, d’autres à la glycine, et certaines traitaient les deux. Certains groupes, tels que les bifidobactéries, les entérocoques et de nombreuses espèces de Bacteroides, étaient particulièrement efficaces pour la déconjugaison et pour produire les « acides biliaires secondaires » classiques connus depuis longtemps pour affecter le métabolisme et le risque de cancer.
Nouveaux acteurs : additions microbiennes et raccourcis
Au‑delà du simple découpage des acides biliaires, de nombreuses bactéries les reconnectaient aussi à une large gamme d’acides aminés, créant des acides biliaires dits conjugués microbiellement. Cette capacité corrélait fortement avec une activité élevée de déconjugaison. Plus surprenant, l’équipe a détecté de manière répétée des « acides biliaires secondaires conjugués » qui ne devraient pas exister selon la vision traditionnelle de la chimie biliaire. Des expériences temporelles précises et des tests génétiques ont révélé que, chez plusieurs espèces, des enzymes appelées hydroxystéroïde déshydrogénases pouvaient agir directement sur le noyau de l’acide biliaire alors que la glycine ou la taurine était encore attachée. Chez une espèce intestinale clé, Bacteroides thetaiotaomicron, la suppression d’une seule de ces enzymes abolissait complètement ce raccourci, prouvant qu’elle convertit normalement un acide biliaire produit par le foie en une nouvelle forme secondaire conjuguée sans passer par un intermédiaire libre.
Coopération microbienne dans l’intestin et preuves in vivo
L’étude a aussi exploré la manière dont différentes bactéries coopèrent. Lorsque des souches à forte activité de déconjugaison étaient cultivées ensemble avec B. thetaiotaomicron, la communauté combinée pouvait réaliser des conversions multi‑étapes qu’aucune espèce seule ne pouvait accomplir, transformant des acides biliaires conjugués simples en une cascade de produits oxydés et épimérisés. Pour vérifier si ces acides biliaires secondaires conjugués inhabituels sont produits chez les animaux, les scientifiques ont colonisé des souris exemptes de germes avec soit B. thetaiotaomicron normale soit une souche déficiente en enzyme et leur ont fourni un acide biliaire humain spécifique dans l’eau de boisson. Les souris hébergeant la souche normale ont accumulé un acide biliaire secondaire conjugué distinct dans leurs selles, tandis que celles portant la souche mutante ne l’ont pas fait, soutenant fortement que ce raccourci métabolique fonctionne aussi chez des hôtes vivants.
Ce que cela signifie pour la santé et les traitements futurs
Depuis des décennies, les manuels décrivent le métabolisme des acides biliaires comme une conduite unidirectionnelle : le foie produit des acides biliaires conjugués, les bactéries en retirent d’abord les chaînes latérales, puis ne remodelent que le noyau. Ce travail renverse cette image linéaire, montrant plutôt un réseau ramifié où le timing et l’intensité des différentes enzymes microbiennes déterminent si les acides biliaires deviennent des formes secondaires classiques, des produits reconjugués par les microbes ou les variantes récemment reconnues d’acides biliaires secondaires conjugués. Parce que les différentes espèces biliaires peuvent influer de façons opposées sur le métabolisme, l’immunité et même le risque de cancer, cartographier ce réseau en détail sera essentiel pour concevoir des régimes, des probiotiques ou des médicaments qui orientent la chimie biliaire vers des résultats plus sains.
Citation: Lucas, L.N., Jillella, M., Cattaneo, L.E. et al. Investigation of bile salt hydrolase activity in human gut bacteria reveals production of conjugated secondary bile acids. Nat Commun 17, 3077 (2026). https://doi.org/10.1038/s41467-026-68556-4
Mots-clés: microbiome intestinal, acides biliaires, bile salt hydrolase, métabolisme microbien, interactions hôte‑microbe