Clear Sky Science · ru
Картирование эпитопов вакцинных антигенов Tc24 и TSA1 с антителами пациентов, инфицированных Trypanosoma cruzi
Почему это исследование важно для здоровья сердца
Болезнь Шагаса, паразитарная инфекция, широко распространённая в Латинской Америке и всё чаще встречающаяся в других регионах, может годами незаметно повреждать сердце до появления серьёзных последствий — сердечной недостаточности или внезапной смерти. Лекарства существуют, но они наиболее эффективны на ранних стадиях и часто сопровождаются сильными побочными эффектами. Поэтому учёные работают над терапевтической вакциной, которая помогла бы иммунной системе контролировать паразита у уже инфицированных людей. В этом исследовании задан простой, но ключевой вопрос: вырабатывают ли реальные пациенты естественным образом антитела, распознающие те же компоненты вакцины, которые сейчас продвигаются в клинические испытания, и стабильны ли эти мишени среди множества штаммов паразита?
Паразит, угроза и идея вакцины
Болезнь Шагаса вызывается простейшим паразитом Trypanosoma cruzi, который циркулирует среди животных, насекомых и людей. Многие инфицированные годами чувствуют себя нормально, хотя паразит сохраняется в их организме. Примерно у трети со временем развиваются хронические поражения сердца или желудочно-кишечного тракта. Существующие препараты наиболее эффективны вскоре после заражения и становятся менее полезными на хронической стадии, где их переносимость также может быть проблемой. Исследователи долгие годы испытывали стратегию вакцины на основе двух белков паразита, Tc24 и TSA1, модифицированных в версии Tc24-C4 и TSA1-C4, которые проще производить, но сохраняют ключевые иммуногенные свойства. В экспериментах на мышах, нечеловекообразных приматах и даже на естественно инфицированных собаках эти компоненты вакцины помогали снижать уровень паразитемии и защищать сердце.
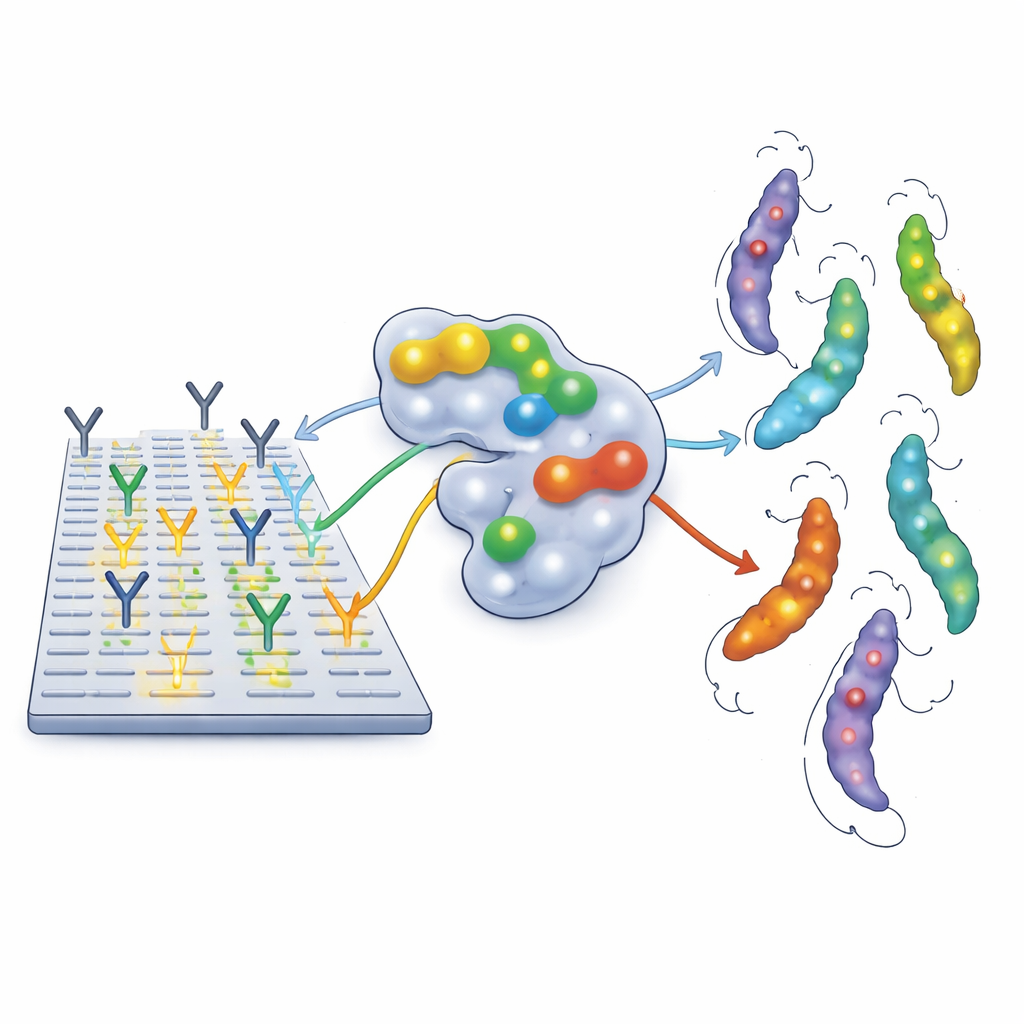
Как команда читала иммунные «отпечатки»
Чтобы точно выяснить, к каким участкам этих вакцинных белков прикрепляются человеческие антитела, авторы использовали метод высокого разрешения — пептидные микрочипы. Они разбили каждый вакцинный белок на серию коротких перекрывающихся фрагментов и зафиксировали эти кусочки на стеклянном слайде. Образцы крови, собранные у 27 беременных женщин с подтверждённой инфекцией T. cruzi в Аргентине, Гондурасе и Мексике, подвергли очистке для выделения IgG и пропускали по слайдам. Там, где антитела прочно связывались, участок подсвечивался, открывая «эпитоп» — небольшую область белка, распознаваемую иммунной системой. Исследователи также сопоставляли эти распознаваемые участки с трёхмерной структурой Tc24 и TSA1 и проверяли, встречаются ли те же последовательности во многих штаммах паразита.
Общий рисунок у разных пациентов и паразитов
У большинства пациентов — почти у трёх четвертей — обнаруживался поразительно похожий узор антительного ответа. Для Tc24-C4 их антитела сильно распознавали одну основную область в середине белка и ещё две более слабые области рядом. Для TSA1-C4 у них были общие четыре основные мишени, в основном расположенные у одного конца белка. Эти «иммунодоминантные» участки обычно находились на наружной поверхности свернутых белков, где антителам легко до них добраться. При сравнительном анализе геномов паразитов, представляющих несколько основных линий T. cruzi, команда обнаружила, что эти ключевые участки сильно консервативны: аминокислотные последовательности мало отличаются между штаммами, а копии эпитопов Tc24 широко распространены в геномах. Это указывает на то, что антитела против этих «горячих точек» в принципе могут распознавать широкий спектр циркулирующих паразитов.
Когда ответы иммунной системы отличались
Не все пациенты укладывались в этот доминирующий шаблон. Примерно у четверти наблюдалось мало или совсем не было связывания антител с основными горячими участками: вместо этого антитела распознавали рассеянные альтернативные области или в нескольких случаях почти не реагировали на вакцинные белки. Исследователи проверили, можно ли объяснить эти различия стандартными диагностическими результатами, уровнем паразитемии в крови, возрастом, анамнезом беременностей или генами HLA пациентов, которые формируют иммунные ответы. Ни один из этих факторов явно не разделял группы. Ограниченная генотипизация паразитов также показала, что люди с одинаковым доминирующим антительным рисунком могли быть инфицированы очень разными наборами штаммов T. cruzi. Это наводит на мысль, что другие факторы — такие как уровень экспрессии каждого белка у паразитов, способ представления эпитопов на их поверхности или постепенная «истощаемость» частей иммунной системы — могут формировать антительный профиль каждого человека.
Что это значит для будущих вакцин
Для вакцины, предназначенной для лечения уже инфицированных людей, обнадёживает то, что у большинства пациентов антитела естественным образом фокусируются на небольшом наборе стабильных, общих участков Tc24 и TSA1, которые присутствуют во многих штаммах паразита и экспонируются на поверхности белка. Эти области представляют собой ясные мишени для усиления защитного иммунитета вакцинацией и для отслеживания изменений антительного ответа в будущих клинических испытаниях. В то же время меньшинство пациентов с атипичным или слабым распознаванием напоминает, что иммунная система у всех реагирует по-разному. В целом эта работа даёт детальную карту того, где человеческие антитела «садятся» на двух ведущих кандидатах в вакцины против болезни Шагаса, и устанавливает базовую линию для оценки того, успешно ли вакцинация перестраивает эти ответы в сторону лучшего контроля этой продолжительной, разрушающей сердце инфекции.
Цитирование: Dumonteil, E., Herrera, C. Epitope mapping of vaccine antigens Tc24 and TSA1 with antibodies from Trypanosoma cruzi-infected patients. Genes Immun 27, 195–202 (2026). https://doi.org/10.1038/s41435-026-00380-8
Ключевые слова: Болезнь Шагаса, Trypanosoma cruzi, терапевтическая вакцина, эпитопы антител, Tc24 и TSA1