Clear Sky Science · nl
Epitoopmapping van vaccenantigenen Tc24 en TSA1 met antilichamen van Trypanosoma cruzi-geïnfecteerde patiënten
Waarom dit onderzoek belangrijk is voor de gezondheid van het hart
De Chagas-ziekte, een parasitaire infectie die veel voorkomt in Latijns-Amerika en steeds vaker wereldwijd wordt gezien, kan jarenlang stil het hart beschadigen voordat ernstige problemen optreden, zoals hartfalen en plotselinge dood. Er bestaan medicijnen, maar die werken het beste vroeg en veroorzaken vaak sterke bijwerkingen. Wetenschappers ontwikkelen daarom een therapeutisch vaccin om het immuunsysteem te helpen de parasiet bij reeds geïnfecteerde mensen onder controle te houden. Deze studie stelt een eenvoudige maar cruciale vraag: maken echte patiënten van nature antilichamen aan die dezelfde vacciningrediënten herkennen die nu richting klinische proeven gaan, en zijn die doelwitten stabiel over de vele stammen van de parasiet?
De parasiet, de dreiging en het vaccinidee
De Chagas-ziekte wordt veroorzaakt door de eencellige parasiet Trypanosoma cruzi, die circuleert in dieren, insecten en mensen. Veel geïnfecteerde mensen voelen zich jarenlang prima, hoewel de parasiet in hun lichaam blijft aanwezig. Ongeveer eenderde ontwikkelt uiteindelijk chronische hartaandoeningen of spijsverteringsproblemen. Huidige medicijnen zijn het meest effectief kort na infectie en worden minder bruikbaar in het chronische stadium, waar ze ook moeilijk te verdragen kunnen zijn. Onderzoekers hebben jaren besteed aan het testen van een vaccinstrategie gebaseerd op twee parasiet-eiwitten, Tc24 en TSA1, die zijn aangepast tot varianten Tc24-C4 en TSA1-C4 die makkelijker te produceren zijn maar hun belangrijke immuunkenmerken behouden. Bij muizen, niet-menselijke primaten en zelfs natuurlijk geïnfecteerde honden hebben deze vaccicomponenten geholpen om het parasietniveau te verlagen en het hart te beschermen.
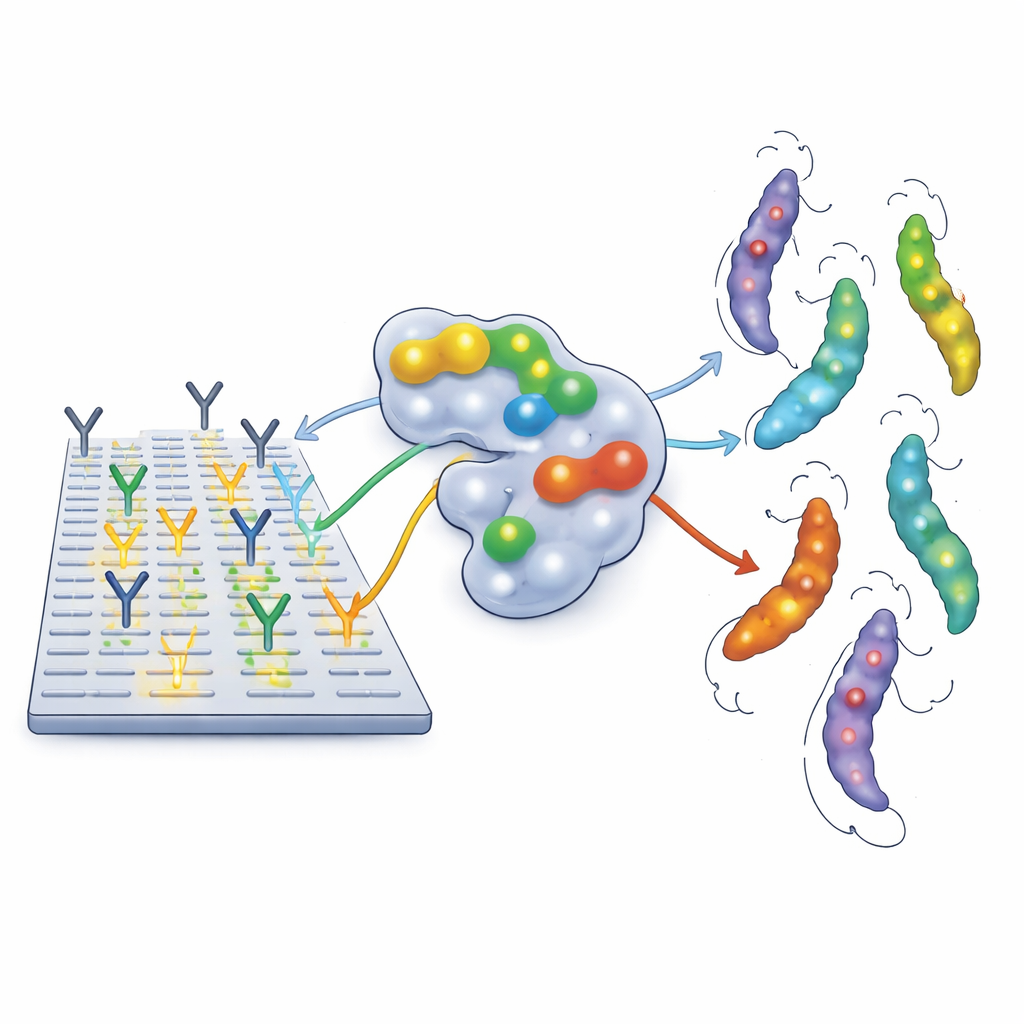
Hoe het team de immuun "vingerafdrukken" las
Om precies te zien waar menselijke antilichamen zich aan deze vaccineiwitten hechten, gebruikten de auteurs een hoogresolutie-techniek genaamd peptide-microarrays. Ze brachten elk vaccineiwit terug tot een reeks korte, overlappende fragmenten en bevestigden deze kleine stukjes op een glazen objectglaasje. Bloedmonsters, verzameld van 27 zwangere vrouwen met gedocumenteerde T. cruzi-infectie in Argentinië, Honduras en Mexico, werden verwerkt om IgG-antilichamen te zuiveren en over de glaasjes te laten stromen. Waar antilichamen sterk binden, lichtte de spot op en onthulde een "epitoop" – een klein gebied van het eiwit dat door het immuunsysteem wordt herkend. De onderzoekers bekeken ook hoe deze herkende regio’s zich verhouden tot de driedimensionale structuren van Tc24 en TSA1 en of dezelfde sequenties in veel verschillende parasietstammen voorkomen.
Een gedeeld patroon bij diverse patiënten en parasieten
De meeste patiënten – bijna driekwart – vertoonden een opvallend vergelijkbaar antilichaampatroon. Voor Tc24-C4 herkenden hun antilichamen sterk één hoofdregio in het midden van het eiwit en twee zwakkere regio’s in de buurt. Voor TSA1-C4 deelden ze vier hoofddoelwitten, meestal dicht bij één uiteinde van het eiwit. Deze "immunodominante" plekken bevonden zich doorgaans aan de buitenkant van de gevouwen eiwitten, waar antilichamen ze gemakkelijk kunnen bereiken. Toen het team parasietgenomen vergeleek die verschillende belangrijke Trypanosoma cruzi-linages vertegenwoordigden, zagen ze dat deze sleutelsites sterk geconserveerd waren: de aminozuursequenties veranderden weinig van stam tot stam, en kopieën van de Tc24-epitopen waren overvloedig aanwezig in genoomgegevens. Dit suggereert dat antilichamen tegen deze hotspots in principe een breed spectrum van circulerende parasieten zouden kunnen herkennen.
Wanneer immuunresponsen van het patroon afwijken
Niet elke patiënt paste in dit dominante patroon. Ongeveer een kwart had weinig of geen antilichaambinding aan de belangrijkste hotspots, en herkende in plaats daarvan verspreide alternatieve regio’s, of in enkele gevallen nauwelijks reageerde op de vaccineiwitten. De onderzoekers onderzochten of dit verschil verklaard kon worden door standaarddiagnostische testresultaten, parasietniveaus in het bloed, leeftijd, zwangerschapsgeschiedenis of de HLA-genen van de patiënten, die helpen immuunresponsen vorm te geven. Geen van deze factoren scheidde de groepen duidelijk. Beperkte parasiet-genotypering toonde ook aan dat individuen met hetzelfde dominante antilichaampatroon geïnfecteerd konden zijn met zeer verschillende mengsels van T. cruzi-stammen. Dit wijst erop dat andere factoren, zoals de hoeveelheid van elk eiwit die parasieten tot expressie brengen, hoe epitopen op hun oppervlak worden gepresenteerd, of geleidelijke "uitputting" van delen van het immuunsysteem, het antilichaamprofiel van een persoon kunnen bepalen.
Wat dit betekent voor toekomstige vaccins
Voor een vaccin dat bedoeld is om reeds geïnfecteerde mensen te behandelen, is het bemoedigend dat de meeste patiënten hun antilichamen van nature richten op een kleine set stabiele, gedeelde regio’s van Tc24 en TSA1 die in veel parasietstammen aanwezig zijn en blootliggen op het eiwitoppervlak. Deze regio’s bieden duidelijke doelwitten om de beschermende immuniteit met vaccinatie te versterken en om te volgen hoe antilichaamresponsen veranderen in toekomstige klinische proeven. Tegelijkertijd herinnert de minderheid van patiënten met atypische of zwakke herkenning ons eraan dat niet ieders immuunsysteem op dezelfde manier reageert. Al met al levert dit werk een gedetailleerde kaart van waar menselijke antilichamen landen op twee leidende Chagas-vaccinkandidaten en schept het een uitgangspunt om te beoordelen of vaccinatie die responsen succesvol herschapen om deze langdurige, hartbeschadigende infectie beter te beheersen.
Bronvermelding: Dumonteil, E., Herrera, C. Epitope mapping of vaccine antigens Tc24 and TSA1 with antibodies from Trypanosoma cruzi-infected patients. Genes Immun 27, 195–202 (2026). https://doi.org/10.1038/s41435-026-00380-8
Trefwoorden: Chagas-ziekte, Trypanosoma cruzi, therapeutisch vaccin, antilichaam-epitopen, Tc24 en TSA1