Clear Sky Science · de
Epitope-Kartierung der Impfantigene Tc24 und TSA1 mit Antikörpern von Trypanosoma cruzi-infizierten Patienten
Warum diese Forschung für die Herzgesundheit wichtig ist
Die Chagas-Krankheit, eine parasitäre Infektion, die in Lateinamerika verbreitet ist und zunehmend weltweit auftritt, kann das Herz über Jahre hinweg stillschweigend schädigen, bevor sie ernsthafte Probleme wie Herzinsuffizienz oder plötzlichen Herztod verursacht. Es gibt Medikamente, die am besten früh wirken, aber häufig starke Nebenwirkungen hervorrufen. Daher entwickeln Wissenschaftler einen therapeutischen Impfstoff, der dem Immunsystem helfen soll, den Parasiten bei bereits Infizierten unter Kontrolle zu halten. Diese Studie stellt eine einfache, aber entscheidende Frage: Bilden reale Patienten natürlicherweise Antikörper, die dieselben Impfstoffbestandteile erkennen, die nun in Richtung klinischer Studien gehen, und sind diese Ziele über die vielen Stämme des Parasiten hinweg stabil?
Der Parasit, die Gefahr und die Impfidee
Die Chagas-Krankheit wird durch den Protozoenparasit Trypanosoma cruzi verursacht, der in Tieren, Insekten und Menschen zirkuliert. Viele Infizierte fühlen sich jahrelang wohl, obwohl der Parasit in ihrem Körper persistiert. Etwa ein Drittel entwickelt schließlich chronische Herzkrankheiten oder Probleme des Verdauungstrakts. Gegenwärtige Medikamente sind kurz nach der Infektion am wirksamsten und werden im chronischen Stadium weniger nützlich; dort sind sie zudem oft schlecht verträglich. Forschende haben Jahre damit verbracht, eine Impfstrategie auf Basis von zwei Parasitenproteinen, Tc24 und TSA1, zu testen, die in Versionen namens Tc24-C4 und TSA1-C4 gentechnisch so verändert wurden, dass sie leichter herzustellen sind, aber ihre wichtigsten immunologischen Eigenschaften behalten. In Mäusen, nicht-menschlichen Primaten und sogar natürlich infizierten Hunden haben diese Impfkomponenten geholfen, die Parasitenspiegel zu senken und das Herz zu schützen.
Wie das Team die immunologischen „Fingerabdrücke" las
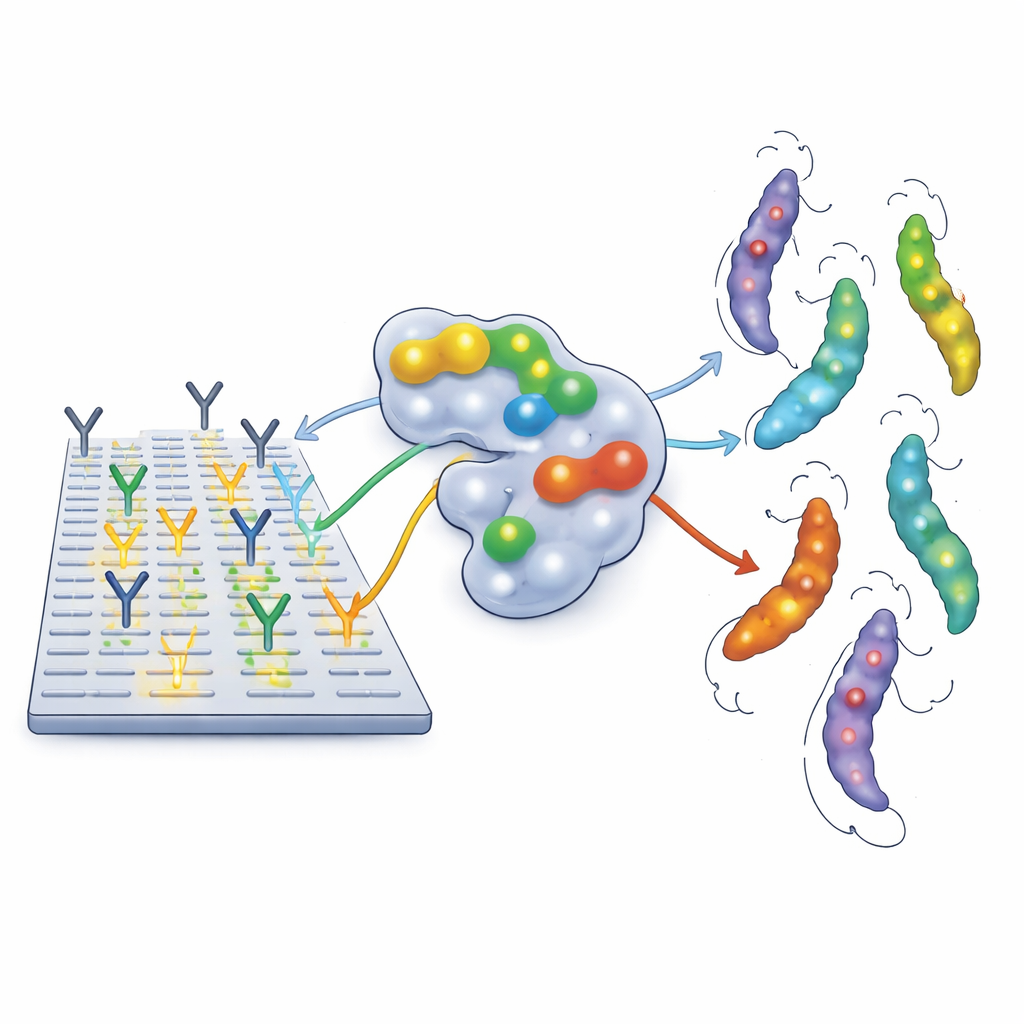
Um genau zu sehen, wo menschliche Antikörper an diese Impfproteine andocken, nutzten die Autoren eine hochauflösende Methode namens Peptidmikroarrays. Sie zerlegten jedes Impfprotein in eine Reihe kurzer, überlappender Fragmente und fixierten diese winzigen Stücke auf einer Glasplatte. Blutproben, gesammelt von 27 schwangeren Frauen mit dokumentierter T. cruzi-Infektion in Argentinien, Honduras und Mexiko, wurden zur Reinigung von IgG-Antikörpern verarbeitet und über die Mikroarrays geleitet. Wo Antikörper stark binden, leuchtet der Punkt auf und zeigt ein „Epitop“ – eine kleine Region des Proteins, die das Immunsystem erkennt. Die Forschenden überprüften außerdem, wie sich diese erkannten Regionen auf die dreidimensionalen Strukturen von Tc24 und TSA1 abbilden und ob dieselben Sequenzen in vielen verschiedenen Parasitenstämmen vorkommen.
Ein gemeinsames Muster bei verschiedenen Patienten und Parasiten
Die Mehrheit der Patienten – nahezu drei Viertel – zeigte ein auffallend ähnliches Antikörpermuster. Für Tc24-C4 erkannten ihre Antikörper stark eine zentrale Region des Proteins und zwei schwächere angrenzende Bereiche. Bei TSA1-C4 teilten sie vier Hauptzielregionen, meist in der Nähe eines Endes des Proteins. Diese „immunodominanten" Stellen lagen zumeist an den äußeren Oberflächen der gefalteten Proteine, wo Antikörper sie leicht erreichen können. Beim Vergleich von Parasitengenomen, die mehrere wichtige Trypanosoma cruzi-Linien repräsentieren, fanden die Forschenden, dass diese Schlüsselregionen hochkonserviert sind: Die Aminosäuresequenzen änderten sich nur wenig von Stamm zu Stamm, und Kopien der Tc24-Epitope waren in den Genomen häufig vorhanden. Das legt nahe, dass Antikörper gegen diese Hotspots prinzipiell eine breite Palette zirkulierender Parasiten erkennen könnten.
Wenn Immunantworten von der Norm abweichen
Nicht jeder Patient passte zu diesem dominanten Muster. Etwa ein Viertel wies kaum oder gar keine Antikörperbindung an die Haupt-Hotspots auf, sondern erkannte verstreute Alternativregionen oder reagierte in einigen Fällen kaum auf die Impfproteine. Die Forschenden untersuchten, ob sich dieser Unterschied durch Standarddiagnostik, Parasitenlast im Blut, Alter, Schwangerschaftsanamnese oder die HLA-Gene der Patienten erklären lässt, die Immunantworten mitformen. Keiner dieser Faktoren trennte die Gruppen eindeutig. Begrenzte Parasiten-Genotypisierung zeigte außerdem, dass Personen mit demselben dominanten Antikörpermuster mit sehr unterschiedlichen Mischungen von T. cruzi-Stämmen infiziert sein konnten. Das deutet darauf hin, dass andere Faktoren, wie die Menge der Proteinexpression durch die Parasiten, die Art, wie Epitope an der Oberfläche präsentiert werden, oder eine allmähliche „Erschöpfung" bestimmter Teile des Immunsystems, das Antikörperprofil jedes Einzelnen beeinflussen können.
Was das für künftige Impfstoffe bedeutet
Für einen Impfstoff, der dafür gedacht ist, bereits Infizierte zu behandeln, ist es ermutigend, dass die meisten Patienten ihre Antikörper natürlicherweise auf eine kleine Gruppe stabiler, geteilter Regionen von Tc24 und TSA1 konzentrieren, die in vielen Parasitenstämmen vorkommen und an der Proteinoberfläche exponiert sind. Diese Regionen bieten klare Ziele, um durch Impfung schützende Immunität zu verstärken und um zu verfolgen, wie sich Antikörperreaktionen in künftigen klinischen Studien verändern. Gleichzeitig erinnert uns die Minderheit von Patienten mit untypischer oder schwacher Erkennung daran, dass nicht jedes Immunsystem gleich reagiert. Insgesamt liefert diese Arbeit eine detaillierte Karte der Stellen, an denen menschliche Antikörper auf zwei führende Chagas-Impfkandidaten treffen, und schafft eine Basislinie, um zu beurteilen, ob eine Impfung diese Antworten erfolgreich so umgestaltet, dass sie diese langanhaltende, das Herz schädigende Infektion besser kontrollieren kann.
Zitation: Dumonteil, E., Herrera, C. Epitope mapping of vaccine antigens Tc24 and TSA1 with antibodies from Trypanosoma cruzi-infected patients. Genes Immun 27, 195–202 (2026). https://doi.org/10.1038/s41435-026-00380-8
Schlüsselwörter: Chagas-Krankheit, Trypanosoma cruzi, therapeutischer Impfstoff, Antikörper-Epitope, Tc24 und TSA1