Clear Sky Science · pt
Aprendizado interpretável informado pela física revela mecanismos de adsorção e envenenamento por enxofre em nanoclusters icosaédricos de 13 átomos
Por que clusters metálicos minúsculos e enxofre importam
Muitos catalisadores industriais são lentamente “envenenados” por enxofre: átomos provenientes de combustíveis e gases de escape aderem às superfícies metálicas e interrompem as reações desejadas. Este estudo aprofunda-se em uma escala extrema — partículas metálicas compostas por apenas 13 átomos — para entender, átomo por átomo, como o enxofre se fixa, como pode danificar esses pequenos catalisadores e como certos metais conseguem manter-se simultaneamente ativos e resilientes. As descobertas fornecem regras de projeto para futuros catalisadores tolerantes ao enxofre usados em tecnologias energéticas e ambientais.
Pequenas gaiolas metálicas na escala nanométrica
Os pesquisadores concentram-se em um sistema-modelo simples, porém poderoso: clusters metálicos de 13 átomos dispostos em uma icosaédrica, uma gaiola altamente simétrica com um átomo no centro e 12 nos vértices. Eles constroem sistematicamente essas gaiolas a partir de 30 metais de transição diferentes, abrangendo três linhas da tabela periódica. Usando simulações quântico-mecânicas, primeiro examinam os clusters “nus”: quão fortemente os átomos se ligam, como vibram, como os elétrons se distribuem e quão reativas essas gaiolas nanométricas podem ser. Mesmo neste tamanho diminuto, surgem tendências claras de um metal para outro, refletindo o preenchimento de seus elétrons externos.
Como o enxofre se prende e inicia o envenenamento
Em seguida, a equipe adiciona átomos únicos de enxofre aos clusters e deixa as estruturas relaxarem até suas formas preferidas. O enxofre pode pousar em três tipos de sítios na gaiola — diretamente acima de um átomo, fazendo ponte entre dois átomos, ou sentado em uma pequena cavidade cercada por três átomos. Para a maioria dos metais, o enxofre prefere o sítio de cavidade, onde pode se ligar a vários vizinhos ao mesmo tempo. As simulações mostram que a ligação do enxofre é sempre energeticamente favorável e frequentemente muito forte, o que explica por que o envenenamento por enxofre é um problema tão persistente. Em muitos casos, a atração metal–enxofre domina, enquanto a gaiola metálica se deforma apenas moderadamente — embora, para alguns metais, o enxofre possa desencadear grandes rearranjos do cluster.
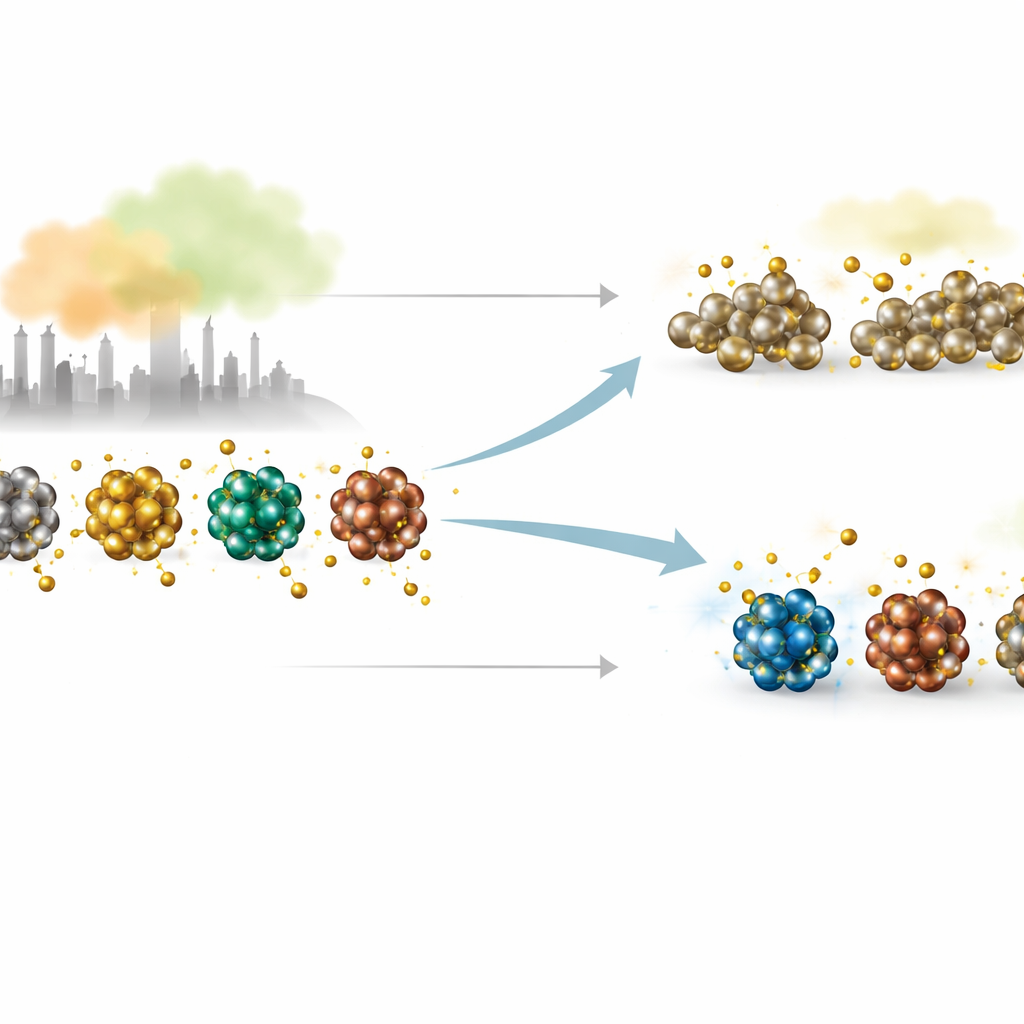
Padrões através da tabela periódica
Como esses clusters são tão pequenos, regras simples de um único número não capturam completamente o quão fortemente o enxofre irá se ligar. Para entender os dados complexos, os autores combinam seus cálculos baseados em física com aprendizado de máquina. Eles alimentam os modelos com um conjunto rico de descritores: comprimentos de ligação e coordenação, quão rígidas ou suaves são as vibrações, como os estados eletrônicos estão organizados e quanto carga flui do metal para o enxofre. Aprendizado não supervisionado agrupa metais que se comportam de forma semelhante quando o enxofre se liga, enquanto modelos de regressão testam quais propriedades subjacentes são mais úteis para prever a adsorção de enxofre. Juntas, essas análises revelam padrões periódicos e destacam onde o enxofre causa mudanças superficiais suaves versus grandes rearranjos estruturais que poderiam degradar um catalisador.
Um trio de candidatos resistentes e equilibrados
Do mapa orientado por dados, surge um grupo de destaque: clusters feitos de titânio, zircônio e háfnio. Esses três metais compartilham o mesmo número de elétrons externos e apresentam comportamento notavelmente semelhante em todos os descritores. O enxofre se liga às suas gaiolas de 13 átomos com força suficiente para ativar moléculas contendo enxofre, mas não tão fortemente a ponto de a gaiola colapsar ou se reconfigurar dramaticamente. Para testar isso mais a fundo, os autores estudam um poluente mais realista, dióxido de enxofre (SO2), nesses três clusters. Suas simulações revelam que o SO2 tende a se dissociar ao contato, formando ligações metal–enxofre e metal–oxigênio robustas, contudo a gaiola metálica mantém em grande parte sua estrutura geral — um equilíbrio promissor entre atividade e durabilidade.
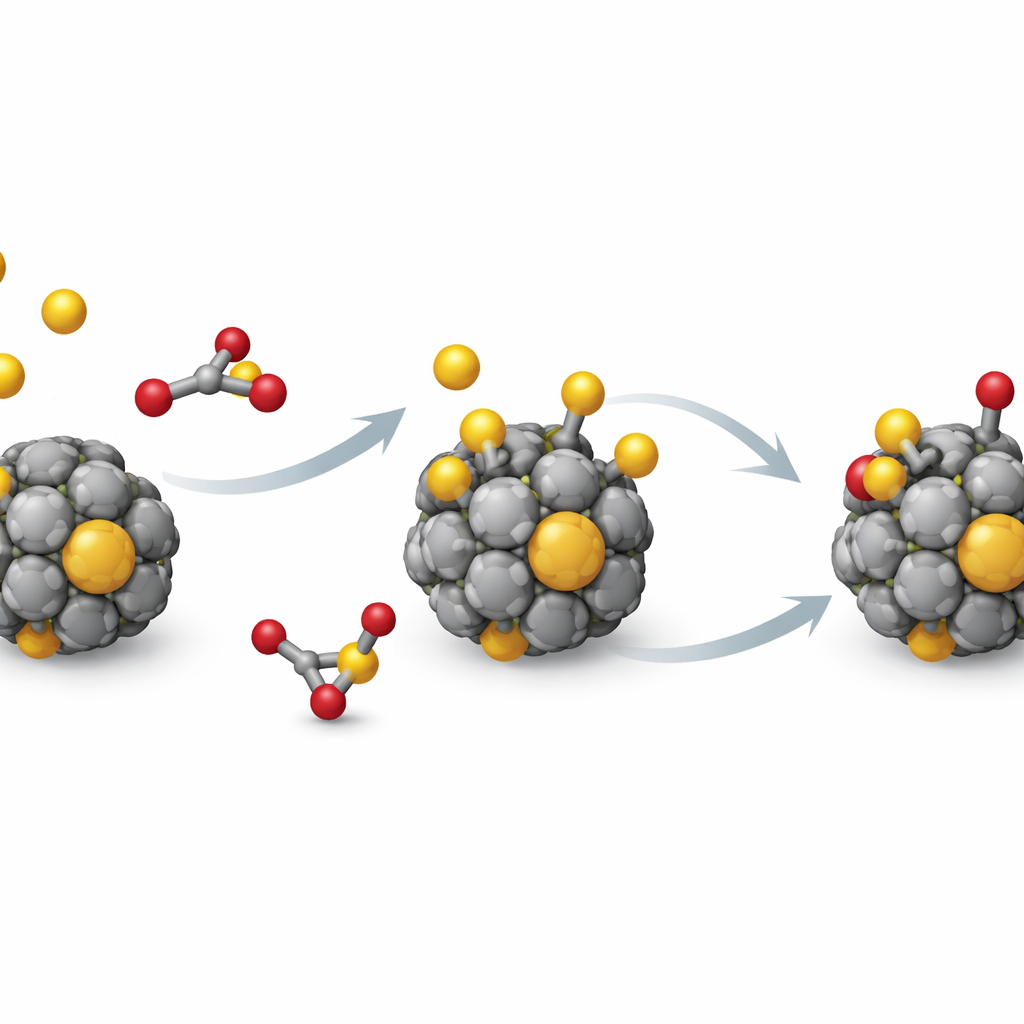
O que isso significa para catalisadores futuros
Em termos simples, o estudo mostra que nem todas as partículas metálicas minúsculas sucumbem ao enxofre da mesma forma. Ao conectar cuidadosamente estrutura, vibrações e comportamento eletrônico à ligação do enxofre, os autores identificam quais metais têm maior probabilidade de sobreviver em ambientes ricos em enxofre. O trio titânio–zircônio–háfnio, em particular, atinge um ponto ideal: prende o enxofre com intensidade suficiente para ajudar a decompor gases de enxofre nocivos, mas resiste aos danos severos que inutilizariam um catalisador. Esses insights, destilados de cálculos quânticos detalhados e aprendizado de máquina interpretável, oferecem diretrizes práticas para projetar nanocatalisadores tolerantes ao enxofre de próxima geração.
Citação: Monteiro, R.F., Palheta, J.M.T., Grison, T.G. et al. Interpretable, physics-informed learning reveals sulfur adsorption and poisoning mechanisms in 13-atom icosahedra nanoclusters. Sci Rep 16, 14174 (2026). https://doi.org/10.1038/s41598-026-50998-x
Palavras-chave: nanocatalisadores, envenenamento por enxofre, clusters de metais de transição, teoria do funcional da densidade, aprendizado de máquina em ciência dos materiais