Clear Sky Science · it
Apprendimento interpretabile e informato dalla fisica rivela meccanismi di adsorbimento e avvelenamento da zolfo in nanocluster icosaedrici a 13 atomi
Perché contano i cluster metallici minuscoli e lo zolfo
Molti catalizzatori industriali vengono lentamente “avvelenati” dallo zolfo: atomi provenienti da combustibili e gas di scarico si attaccano alle superfici metalliche e bloccano le reazioni desiderate. Questo studio si concentra su una scala estrema—particelle metalliche composte da appena 13 atomi—per capire, atomo per atomo, come lo zolfo si lega, come può danneggiare questi catalizzatori minuscoli e come certi metalli riescano a restare sia attivi che resilienti. Le intuizioni forniscono regole di progetto per futuri catalizzatori tolleranti allo zolfo impiegati nelle tecnologie energetiche e ambientali.
Piccole gabbie metalliche alla scala dei nanometri
I ricercatori si concentrano su un sistema modello semplice ma potente: cluster metallici a 13 atomi disposti in un icosaedro, una gabbia altamente simmetrica con un atomo al centro e 12 agli angoli. Costruiscono sistematicamente tali gabbie a partire da 30 diversi metalli di transizione, coprendo tre file della tavola periodica. Usando simulazioni di meccanica quantistica, esaminano prima i cluster “nudi”: quanto strettamente gli atomi si legano tra loro, come vibrano, come sono distribuiti gli elettroni e quanto facilmente queste gabbie nanoscalari potrebbero reagire. Anche a questa dimensione piccolissima emergono tendenze chiare da un metallo all’altro, riflettendo il riempimento dei loro elettroni esterni.
Come lo zolfo si lega e innesca l’avvelenamento
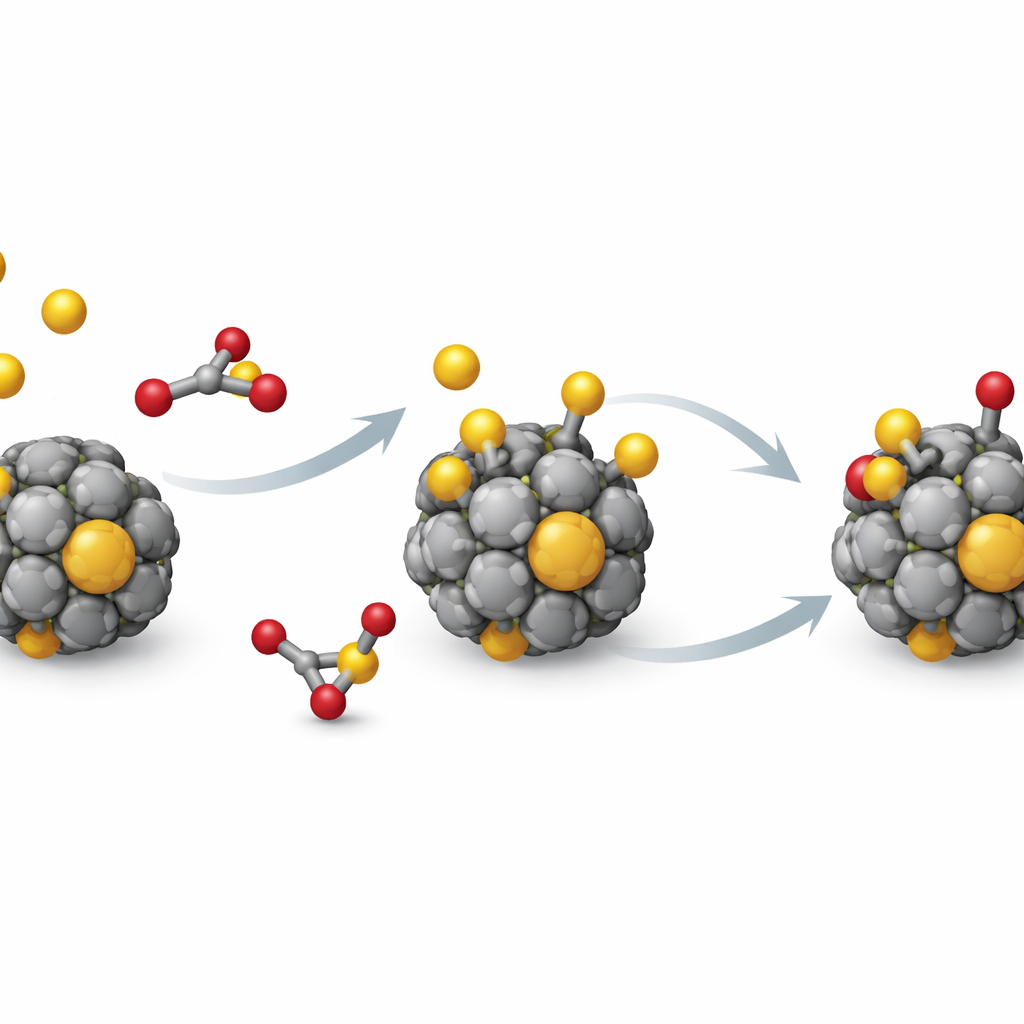
Successivamente, il team aggiunge singoli atomi di zolfo ai cluster e lascia che le strutture si rilassino verso le configurazioni preferite. Lo zolfo può posizionarsi su tre tipi di siti sulla gabbia—direttamente sopra un atomo, in ponte tra due atomi o in una piccola cavità circondata da tre atomi. Per la maggior parte dei metalli, lo zolfo preferisce il sito cava, dove può legarsi a più vicini contemporaneamente. Le simulazioni mostrano che il legame zolfo–metallo è sempre energeticamente favorevole e spesso molto forte, il che spiega perché l’avvelenamento da zolfo sia un problema così persistente. In molti casi l’attrazione metallo–zolfo predomina, mentre la gabbia metallica si deforma solo moderatamente—sebbene per alcuni metalli lo zolfo possa scatenare grandi rinnovamenti strutturali del cluster.
Schemi attraverso la tavola periodica
Poiché questi cluster sono così piccoli, regole semplici basate su un unico numero non catturano appieno quanto fortemente lo zolfo si legherà. Per interpretare il complesso insieme di dati, gli autori combinano i loro calcoli basati sulla fisica con l’apprendimento automatico. Forniscono ai modelli un ricco insieme di descrittori: lunghezze di legame e coordinazione, quanto rigide o morbide sono le vibrazioni, come sono distribuiti gli stati elettronici e quanta carica fluisce dal metallo allo zolfo. L’apprendimento non supervisionato raggruppa i metalli che si comportano in modo simile quando lo zolfo si lega, mentre modelli di regressione testano quali proprietà sottostanti sono più utili per prevedere l’adsorbimento dello zolfo. Insieme, queste analisi rivelano schemi periodici e mettono in evidenza dove lo zolfo induce cambiamenti superficiali lievi rispetto a riorganizzazioni strutturali importanti che potrebbero degradare un catalizzatore.
Un trio di candidati resistenti ed equilibrati
Da questa mappa guidata dai dati emerge un gruppo distintivo: cluster composti da titanio, zirconio e hafnio. Questi tre metalli condividono lo stesso numero di elettroni esterni e mostrano comportamenti sorprendentemente simili in tutti i descrittori. Lo zolfo si lega alle loro gabbie a 13 atomi con sufficiente forza da attivare molecole contenenti zolfo, ma non così fortemente da far collassare o rimodellare drasticamente la gabbia. Per verificare ulteriormente questo risultato, gli autori studiano un inquinante più realistico, il biossido di zolfo (SO2), su questi tre cluster. Le loro simulazioni rivelano che l’S O2 tende a frammentarsi al contatto, formando robusti legami metallo–zolfo e metallo–ossigeno, eppure la gabbia metallica mantiene in gran parte la sua struttura complessiva—un equilibrio promettente tra attività e durabilità.
Cosa significa per i catalizzatori futuri
In termini semplici, lo studio dimostra che non tutte le particelle metalliche piccolissime soccombono allo zolfo nello stesso modo. Collegando con cura struttura, vibrazioni e comportamento elettronico al legame con lo zolfo, gli autori identificano quali metalli hanno maggiori probabilità di sopravvivere in ambienti ricchi di zolfo. Il trio titanio–zirconio–hafnio, in particolare, raggiunge un punto ideale: cattura lo zolfo con abbastanza forza da aiutare a degradare gas zolfati nocivi, ma resiste ai danni severi che comprometterebbero un catalizzatore. Queste intuizioni, distillate da calcoli quantistici dettagliati e da apprendimento automatico interpretabile, offrono linee guida pratiche per progettare nanocatalizzatori di nuova generazione tolleranti allo zolfo.
Citazione: Monteiro, R.F., Palheta, J.M.T., Grison, T.G. et al. Interpretable, physics-informed learning reveals sulfur adsorption and poisoning mechanisms in 13-atom icosahedra nanoclusters. Sci Rep 16, 14174 (2026). https://doi.org/10.1038/s41598-026-50998-x
Parole chiave: nanocatalizzatori, avvelenamento da zolfo, cluster di metalli di transizione, teoria del funzionale della densità, apprendimento automatico nella scienza dei materiali