Clear Sky Science · de
Interpretierbares, physik-informiertes Lernen zeigt Schwefeladsorption und Vergiftungsmechanismen in 13‑Atom‑Ikosaeder‑Nanoklustern
Warum winzige Metallcluster und Schwefel wichtig sind
Viele industrielle Katalysatoren werden allmählich durch Schwefel „vergiftet“: Atome aus Treibstoffen und Abgasen haften an Metalloberflächen und unterbinden die gewünschten Reaktionen. Diese Studie zoomt auf ein extremes Maßstabniveau — Metallpartikel aus nur 13 Atomen — um atomgenau zu verstehen, wie Schwefel anhaftet, wie er diese winzigen Katalysatoren schädigen kann und wie bestimmte Metalle aktiv und gleichzeitig widerstandsfähig bleiben. Die Erkenntnisse liefern Gestaltungsregeln für künftige schwefeltolerante Katalysatoren in Energie‑ und Umwelttechnologien.
Kleine Metallkäfige im Nanobereich
Die Forschenden konzentrieren sich auf ein einfaches, aber aussagekräftiges Modellsystem: 13‑Atom‑Metallcluster, die ein Ikosaeder bilden, einen hochsymmetrischen Käfig mit einem Atom im Zentrum und 12 an den Ecken. Systematisch bauen sie solche Käfige aus 30 verschiedenen Übergangsmetallen auf, die sich über drei Perioden des Periodensystems erstrecken. Mithilfe quantenmechanischer Simulationen untersuchen sie zunächst die „nackten“ Cluster: wie fest die Atome zusammengebunden sind, wie sie schwingen, wie die Elektronen verteilt sind und wie reaktiv diese nanoskaligen Käfige sein könnten. Selbst in dieser winzigen Größe zeigen sich klare Trends von einem Metall zum nächsten, die widerspiegeln, wie ihre äußeren Elektronen besetzt sind.
Wie Schwefel haftet und Vergiftung beginnt
Als Nächstes setzen die Autoren einzelne Schwefelatome auf die Cluster und lassen die Strukturen in ihre bevorzugten Formen entspannen. Schwefel kann an drei Arten von Stellen landen — direkt über einem Atom, zwischen zwei Atomen als Brücke oder in einer kleinen Mulde, die von drei Atomen umgeben ist. Bei den meisten Metallen bevorzugt Schwefel die Muldenstelle, wo es an mehrere Nachbarn gleichzeitig binden kann. Die Simulationen zeigen, dass die Schwefelbindung energetisch immer günstig und oft sehr stark ist, was erklärt, warum Schwefelvergiftung ein so hartnäckiges Problem ist. In vielen Fällen dominiert die Metall‑Schwefel‑Anziehung, während sich der Metallkäfig nur mäßig verformt — obwohl bei einigen Metallen Schwefel große Umgestaltungen des Clusters auslösen kann.
Mustern über das Periodensystem hinweg
Weil diese Cluster so klein sind, erfassen einfache Ein‑Zahlen‑Regeln nicht vollständig, wie stark Schwefel binden wird. Um die komplexen Daten zu durchdringen, kombinieren die Autoren ihre physikbasierten Rechnungen mit maschinellem Lernen. Sie füttern die Modelle mit einem reichhaltigen Satz von Deskriptoren: Bindungslängen und Koordination, wie steif oder weich die Schwingungen sind, wie die elektronischen Zustände angeordnet sind und wie viel Ladung vom Metall zum Schwefel fließt. Unüberwachtes Lernen gruppiert Metalle, die sich beim Schwefel‑Bindungsprozess ähnlich verhalten, während Regressionsmodelle testen, welche zugrunde liegenden Eigenschaften am besten zur Vorhersage der Schwefeladsorption geeignet sind. Gemeinsam zeigen diese Analysen periodische Muster und heben hervor, wo Schwefel sanfte Oberflächenänderungen verursacht versus größere strukturelle Umordnungen, die einen Katalysator degradieren könnten.
Ein Trio robuster, ausgewogener Kandidaten
Aus dieser datengetriebenen Karte ragt eine Gruppe besonders hervor: Cluster aus Titan, Zirkonium und Hafnium. Diese drei Metalle haben dieselbe Anzahl äußerer Elektronen und zeigen über alle Deskriptoren hinweg bemerkenswert ähnliches Verhalten. Schwefel bindet an ihre 13‑Atom‑Käfige stark genug, um schwefelhaltige Moleküle zu aktivieren, aber nicht so stark, dass der Käfig zusammenbricht oder sich dramatisch umformt. Um das weiter zu prüfen, untersuchen die Autoren ein realistischeres Schadstoffmolekül, Schwefeldioxid (SO2), auf diesen drei Clustern. Ihre Simulationen zeigen, dass SO2 dazu neigt, beim Kontakt zu zerfallen und robuste Metall‑Schwefel‑ und Metall‑Sauerstoff‑Bindungen zu bilden, während der Metallkäfig weitgehend seine Gesamtstruktur beibehält — ein vielversprechender Kompromiss zwischen Aktivität und Dauerhaftigkeit.
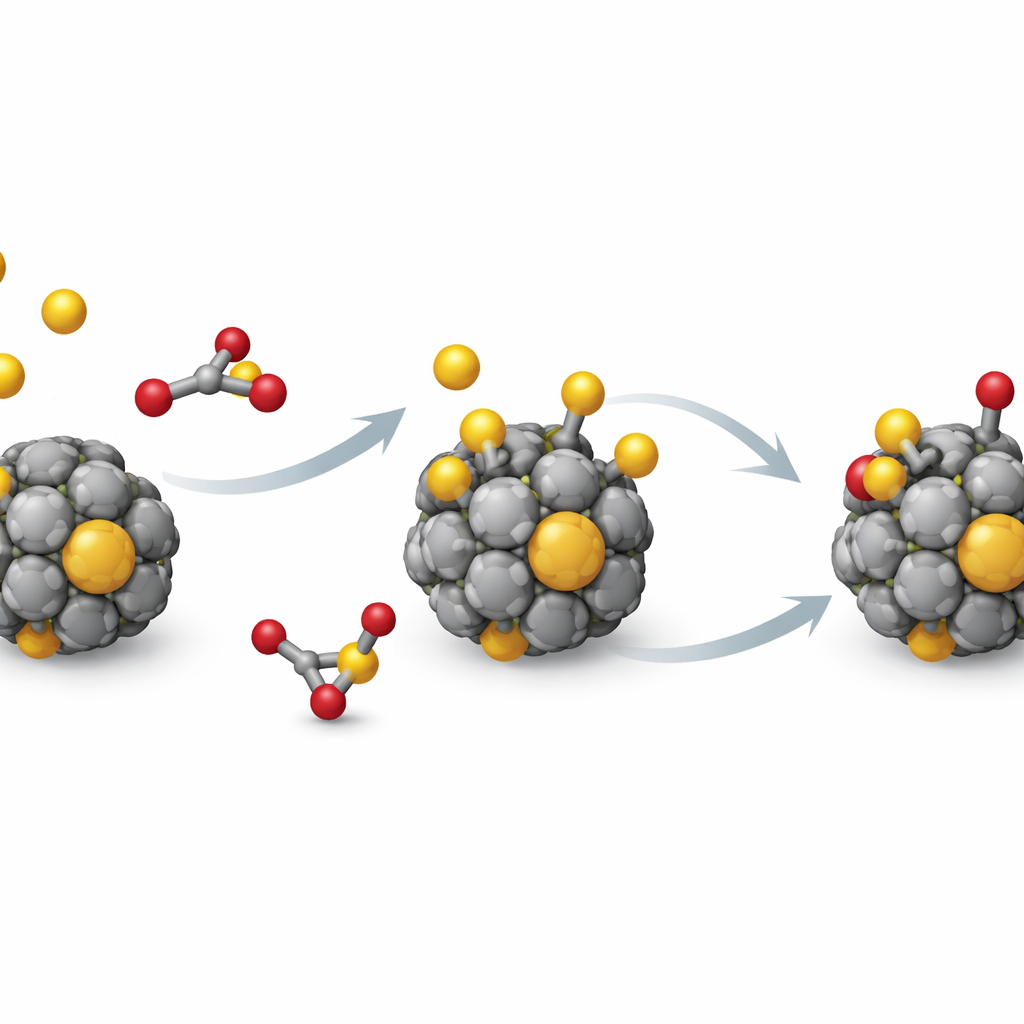
Was das für zukünftige Katalysatoren bedeutet
Einfach gesagt zeigt die Studie, dass nicht alle winzigen Metallpartikel auf dieselbe Weise dem Schwefel erliegen. Indem Struktur, Schwingungen und elektronisches Verhalten sorgfältig mit der Schwefelbindung verknüpft werden, identifizieren die Autoren, welche Metalle in schwefelreichen Umgebungen eher überleben. Insbesondere das Titan‑Zirkonium‑Hafnium‑Trio trifft einen Sweet Spot: Sie binden Schwefel stark genug, um schädliche Schwefelgase zu zersetzen, widerstehen aber den schweren Schäden, die einen Katalysator lahmlegen würden. Diese Erkenntnisse, gewonnen aus detaillierten Quantenrechnungen und interpretierbarem maschinellen Lernen, liefern praktische Leitlinien für das Design der nächsten Generation schwefeltoleranter Nanokatalysatoren.
Zitation: Monteiro, R.F., Palheta, J.M.T., Grison, T.G. et al. Interpretable, physics-informed learning reveals sulfur adsorption and poisoning mechanisms in 13-atom icosahedra nanoclusters. Sci Rep 16, 14174 (2026). https://doi.org/10.1038/s41598-026-50998-x
Schlüsselwörter: Nanokatalysatoren, Schwefelvergiftung, Übergangsmetall‑Cluster, Dichtfunktionaltheorie, Maschinelles Lernen in der Materialwissenschaft