Clear Sky Science · pt
Análise de célula única revela que o hormônio T3 afeta a diferenciação do epitélio do cólon e induz uma população mista de células semelhantes a progenitoras
Por que a história de um hormônio intestinal importa
Todos os dias, o revestimento do seu intestino se renova silenciosamente, substituindo milhões de células para digerir alimentos, absorver nutrientes e proteger contra germes. Essa renovação constante depende de células‑tronco enterradas no fundo de pequenas cavidades chamadas criptas. O hormônio T3, produzido pela tireoide, é conhecido por influenciar o crescimento e o metabolismo em todo o corpo, mas seu impacto em pequena escala sobre as células em renovação do cólon tem sido pouco claro. Este estudo usa perfilagem genética de célula única para ampliar o exame de células individuais no cólon de camundongos e revela como o T3 pode empurrá‑las para um estado incomum e misto que pode ser relevante para a saúde intestinal e possivelmente para o risco de câncer.
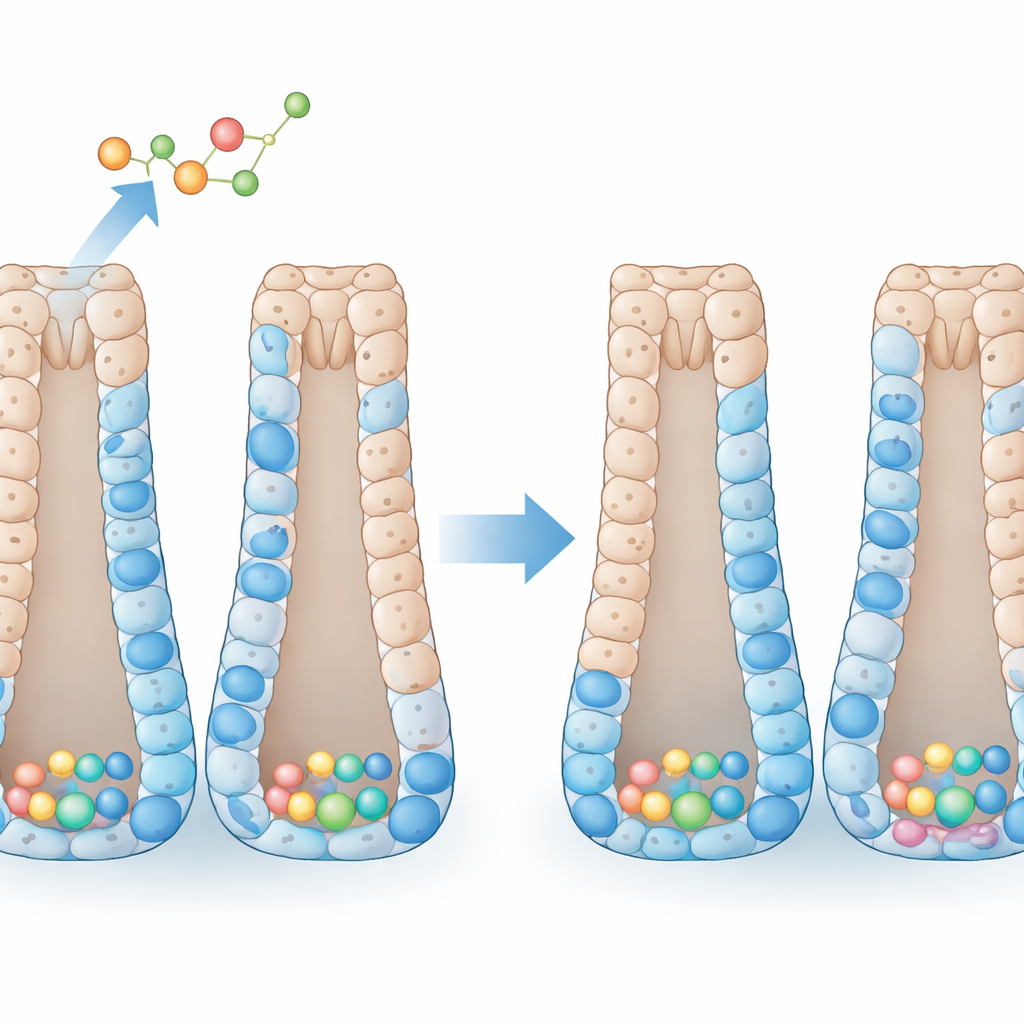
Como o cólon se mantém em forma
O revestimento interno do cólon está organizado como uma série de tubos invertidos. No fundo de cada tubo ficam as células‑tronco, que se dividem para gerar células progenitoras. À medida que essas progenitoras sobem, elas se especializam em vários tipos maduros: células absorventes que captam água e nutrientes, células caliciformes que secretam muco protetor, células enteroendócrinas produtoras de hormônios e células tuft que ajudam a perceber o ambiente. Em condições normais, um equilíbrio rígido entre autorrenovação e especialização mantém o sistema estável. Muitas sinalizações internas já são conhecidas por orientar esse processo, mas entende‑se menos como hormônios corporais de larga escala, como os hormônios tireoidianos, o refinam, especialmente no cólon, que é um local frequente de tumores em humanos.
Um censo de célula única após exposição ao hormônio
Para descobrir o papel do T3, os pesquisadores injetaram camundongos adultos com T3 ou com uma solução salina inócua por dois dias e, em seguida, isolaram células epiteliais do cólon para sequenciamento de RNA de célula única. Essa técnica lê quais genes estão ativos em milhares de células individuais, permitindo ao time agrupar células em tipos distintos com base em seus padrões de expressão. Após controle de qualidade, eles analisaram mais de 15.000 células e identificaram as famílias esperadas: células‑tronco/progenitoras, células secretoras (incluindo caliciformes e tipos relacionados), células absorventes proximais e distais, células produtoras de hormônio e células tuft. Cada grupo exibiu assinaturas gênicas condizentes com sua função conhecida, confirmando que o mapa de célula única capturou fielmente a paisagem celular do cólon.
O hormônio T3 altera destinos celulares sem mudar os tipos celulares
Ao comparar amostras tratadas com T3 e controles, os autores descobriram que o T3 não mudou dramaticamente quantas células se enquadravam em cada categoria ampla, mas alterou o que muitas dessas células estavam fazendo. Em vários grupos—especialmente células‑tronco/progenitoras, secretoras e absorventes—o T3 aumentou a atividade de genes tipicamente associados a células caliciformes, como aqueles envolvidos na produção de muco. De forma notável, isso ocorreu mesmo em células que não eram caliciformes clássicas. Ao mesmo tempo, genes envolvidos na desintoxicação de químicos e no gerenciamento do estresse oxidativo foram geralmente reduzidos, enquanto genes relacionados à defesa e à inflamação foram ativados. Ainda assim, marcadores da identidade central de células‑tronco, como Lgr5, mudaram pouco no geral, sugerindo que o T3 remodela principalmente o comportamento de células precursoras em vez de redefinir completamente os tipos celulares.
Um estado celular misto, preso entre escolhas
O grupo então usou ferramentas computacionais para reconstruir prováveis “trajetórias” de diferenciação, traçando como as células progridem de estados de célula‑tronco/progenitora rumo a destinos maduros. Nos cólons controle, esses caminhos formaram ramos claros conduzindo às linhagens secretora e absorvente. Após a exposição ao T3, os caminhos ficaram borrados: os ramos celulares estavam menos distintos, e certas linhagens, como as produtoras de hormônio e as tuft, pareceram menos separadas de suas origens progenitoras. Uma análise mais detalhada revelou uma população “mista” no tecido tratado com T3 cujas células coexpressavam marcadores de genes de decisão precoce tanto para destinos absorventes quanto secretórios, juntamente com genes tardios relacionados a caliciformes. Importante, muitas dessas células também apresentavam altos níveis de marcadores de proliferação, indicando que ainda estavam ativamente se dividindo.
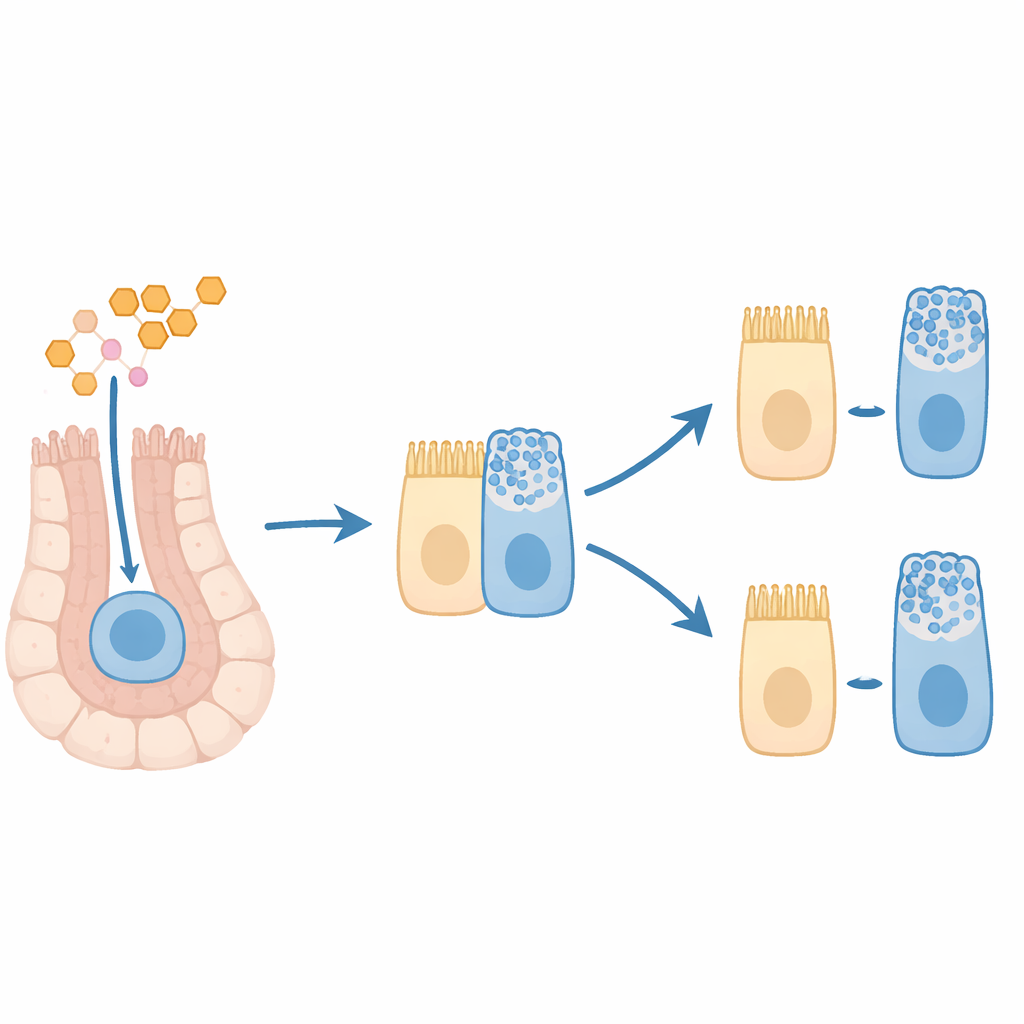
Observando células iniciais com viés caliciforme no tecido
Para testar se esse estado misto aparece na arquitetura real do cólon, os pesquisadores coraram seções de cólon de camundongos controle e tratados com T3 para proteínas que marcam proliferação e tipos celulares específicos. Eles observaram que o T3 não alterou muito o número total de células caliciformes maduras ao longo das criptas. Em vez disso, o T3 causou um acúmulo de células positivas para marcadores de caliciformes no fundo mesmo das criptas—a zona normalmente ocupada por células‑tronco e progenitoras iniciais. Muitas dessas células marcadas para muco também eram positivas para um marcador de proliferação, reforçando a ideia de que o T3 gera progenitores em divisão já inclinados a um destino caliciforme, mas ainda não totalmente maduros.
O que isso significa para a saúde intestinal
Para um leitor leigo, a mensagem central do estudo é que o hormônio tireoidiano T3 pode empurrar precursores do cólon para um estado híbrido: eles se dividem como células semelhantes a tronco, mas já exibem características de células caliciformes secretoras de muco, e parecem estagnar antes de completar a maturação. Como o momento adequado das decisões de destino celular é essencial para um revestimento colônico saudável, populações mistas e imaturas assim poderiam, sob exposição prolongada ou excessiva ao hormônio, tornar‑se mais vulneráveis ao estresse ou à transformação maligna. Embora este trabalho tenha sido feito em camundongos e foque em tratamento de curto prazo, ele destaca uma maneira até então pouco reconhecida pela qual o hormônio tireoidiano molda a renovação do cólon e levanta novas questões sobre como estados tireoidianos alterados podem influenciar doenças do cólon e o risco de câncer em humanos.
Citação: Bidoli, C., Reslinger, M., Sieffert, C. et al. Single-cell analysis reveals that the hormone T3 affects colon epithelial differentiation and induces a mixed progenitor-like cell population. Sci Rep 16, 10369 (2026). https://doi.org/10.1038/s41598-026-40397-7
Palavras-chave: epitélio do cólon, hormônio tireoidiano T3, sequenciamento de RNA de célula única, diferenciação de células caliciformes, células‑tronco intestinais