Clear Sky Science · fr
L’analyse unicellulaire révèle que l’hormone T3 influence la différenciation de l’épithélium colique et induit une population cellulaire mixte de type progéniteur
Pourquoi une histoire d’hormone intestinale importe
Chaque jour, la muqueuse de votre intestin se renouvelle silencieusement, remplaçant des millions de cellules pour digérer les aliments, absorber les nutriments et se protéger contre les microbes. Ce renouvellement constant dépend de cellules souches enfouies au fond de petites cavités appelées cryptes. L’hormone T3, produite par la thyroïde, est connue pour influencer la croissance et le métabolisme dans tout le corps, mais son impact à l’échelle fine sur les cellules en renouvellement du côlon était jusqu’ici peu clair. Cette étude utilise le profilage génétique unicellulaire pour zoomer sur des cellules individuelles du côlon de souris et révèle comment la T3 peut les pousser vers un état inhabituel et mixte, susceptible d’avoir des conséquences pour la santé intestinale et, peut‑être, le risque de cancer.
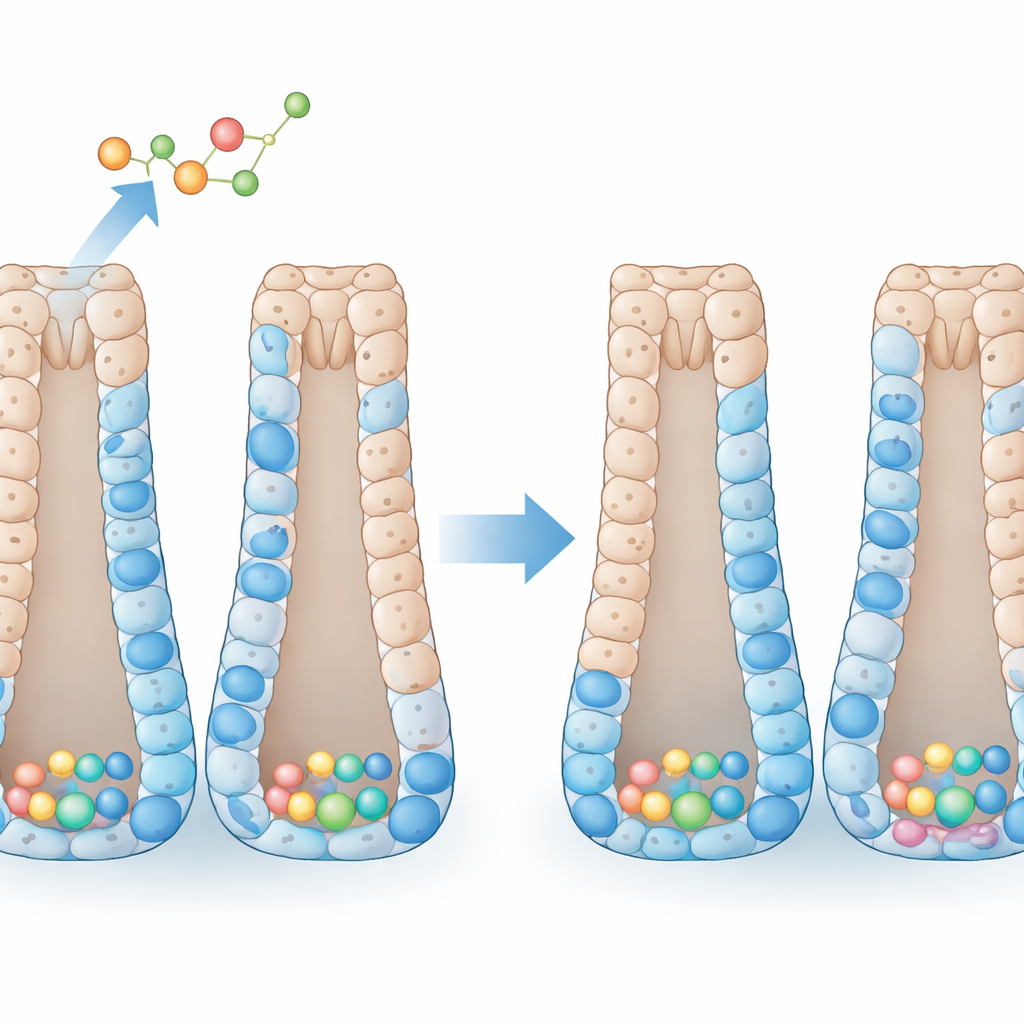
Comment le côlon se maintient
La muqueuse interne du côlon est organisée comme une série de tubes retournés. Au fond de chaque tube se trouvent les cellules souches, qui se divisent pour produire des cellules progénitrices. À mesure que ces progénitrices remontent, elles se spécialisent en plusieurs types matures : des cellules absorbantes qui prélèvent l’eau et les nutriments, des cellules caliciformes qui sécrètent le mucus protecteur, des cellules enteroendocrines productrices d’hormones, et des cellules tuft qui contribuent à la détection de l’environnement. Dans des conditions normales, un équilibre strict entre auto‑renouvellement et spécialisation maintient ce système stable. De nombreux signaux internes guident ce processus, mais on comprend moins comment des hormones générales de l’organisme, comme les hormones thyroïdiennes, l’accordent finement, en particulier dans le côlon, site fréquent de tumeurs chez l’humain.
Un recensement unicellulaire après exposition à l’hormone
Pour découvrir le rôle de la T3, les chercheurs ont injecté à des souris adultes soit de la T3 soit une solution saline inoffensive pendant deux jours, puis isolé des cellules épithéliales du côlon pour un séquençage ARN unicellulaire. Cette technique lit l’activité des gènes dans des milliers de cellules individuelles, permettant à l’équipe de regrouper les cellules en types distincts selon leurs profils d’expression. Après contrôle de qualité, ils ont analysé plus de 15 000 cellules et identifié les familles attendues : cellules souches/progénitrices, cellules sécrétoires (incluant les caliciformes et types apparentés), cellules absorbantes proximales et distales, cellules productrices d’hormones et cellules tuft. Chaque groupe présentait les signatures géniques correspondant à sa fonction connue, confirmant que la carte unicellulaire rendait fidèlement le paysage cellulaire du côlon.
L’hormone T3 infléchit les destins cellulaires sans changer les types
En comparant les échantillons traités par la T3 et les témoins, les auteurs ont constaté que la T3 ne modifiait pas de façon spectaculaire la proportion de cellules dans chaque grande catégorie, mais qu’elle altérait les activités de nombreuses cellules. Dans plusieurs groupes — en particulier les cellules souches/progénitrices, sécrétoires et absorbantes — la T3 a augmenté l’activité de gènes typiquement associés aux cellules caliciformes, tels que ceux impliqués dans la production de mucus. De manière frappante, cela s’observait même dans des cellules qui n’étaient pas des caliciformes classiques. Parallèlement, les gènes impliqués dans la détoxification des composés chimiques et la gestion du stress oxydatif étaient généralement diminués, tandis que les gènes liés à la défense et à l’inflammation étaient augmentés. Cependant, les marqueurs de l’identité fondamentale des cellules souches, comme Lgr5, ont peu changé globalement, ce qui suggère que la T3 remodèle surtout le comportement des précurseurs plutôt que de redéfinir complètement les types cellulaires.
Un état cellulaire mixte, coincé entre deux stades
L’équipe a ensuite utilisé des outils computationnels pour reconstruire les « trajectoires » probables de différenciation, retraçant la progression des cellules depuis des états souches/progéniteurs vers des destins matures. Dans les côlons témoins, ces trajectoires formaient des branches claires menant aux lignées sécrétoires et absorbantes. Après exposition à la T3, les trajectoires se sont estompées : les branches étaient moins distinctes et certaines lignées, comme les cellules productrices d’hormones et les cellules tuft, semblaient moins nettement séparées de leurs origines progénitrices. Un examen plus poussé a révélé une population « mixte » dans les tissus traités à la T3 dont les cellules co‑exprimaient des marqueurs précoces de décision pour les destinées absorbante et sécrétoire, aux côtés de gènes tardifs associés aux caliciformes. Beaucoup de ces cellules affichaient aussi des niveaux élevés de marqueurs de prolifération, indiquant qu’elles se divisaient encore activement.
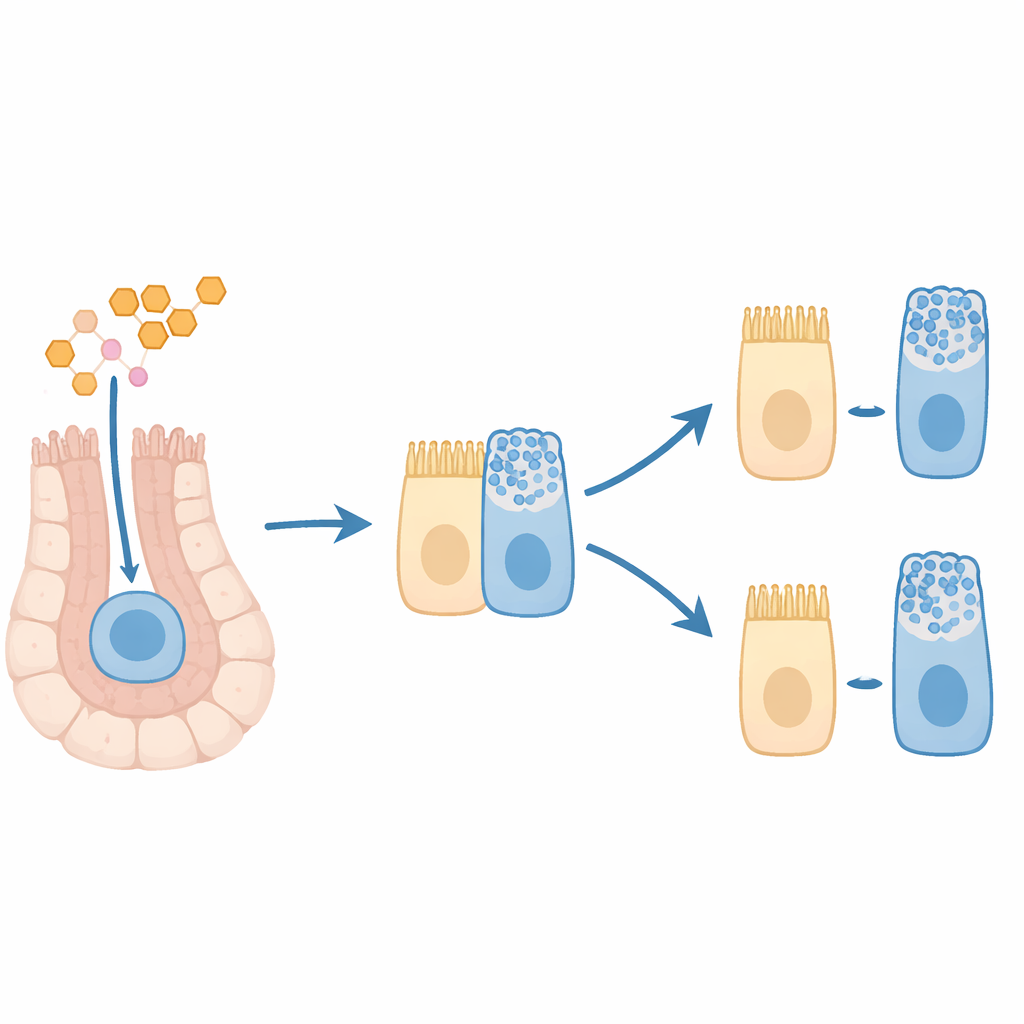
Observer les cellules précocement engagées vers le devenir caliciforme dans le tissu
Pour vérifier si cet état mixte se manifeste dans l’architecture réelle du côlon, les chercheurs ont coloré des coupes de côlon de souris témoins et traitées par T3 pour des protéines marquant la prolifération et des types cellulaires spécifiques. Ils ont observé que la T3 ne modifiait pas fortement le nombre total de cellules caliciformes matures le long des cryptes. En revanche, la T3 provoquait une accumulation de cellules positives pour des marqueurs caliciformes tout au fond des cryptes — la zone normalement occupée par les cellules souches et les progéniteurs précoces. Bon nombre de ces cellules marquées pour le mucus étaient également positives pour un marqueur de prolifération, renforçant l’idée que la T3 génère des progéniteurs en division déjà orientés vers un destin caliciforme mais pas encore complètement matures.
Ce que cela implique pour la santé intestinale
Pour un lecteur non spécialiste, le message central de l’étude est que l’hormone thyroïdienne T3 peut pousser les précurseurs coliques vers un état hybride : ils se divisent comme des cellules de type souches mais portent déjà des caractéristiques des cellules caliciformes sécrétrices de mucus, et semblent se bloquer avant d’atteindre la maturité complète. Parce que la bonne synchronisation des décisions de destin cellulaire est essentielle pour une muqueuse colique saine, de telles populations mixtes et immatures pourraient, en cas d’exposition prolongée ou excessive à l’hormone, devenir plus vulnérables au stress ou à une transformation maligne. Bien que ce travail soit réalisé chez la souris et porte sur un traitement de courte durée, il met en lumière une manière jusque‑là méconnue dont l’hormone thyroïdienne façonne le renouvellement colique et soulève de nouvelles questions sur la façon dont des états thyroïdiens altérés pourraient influencer les maladies coliques et le risque de cancer chez l’humain.
Citation: Bidoli, C., Reslinger, M., Sieffert, C. et al. Single-cell analysis reveals that the hormone T3 affects colon epithelial differentiation and induces a mixed progenitor-like cell population. Sci Rep 16, 10369 (2026). https://doi.org/10.1038/s41598-026-40397-7
Mots-clés: épithélium du côlon, hormone thyroïdienne T3, séquençage ARN unicellulaire, différenciation des cellules caliciformes, cellules souches intestinales