Clear Sky Science · de
Einzelzell-Analyse zeigt, dass das Hormon T3 die Differenzierung des Kolonepithels beeinflusst und eine gemischte progenitorähnliche Zellpopulation induziert
Warum eine Geschichte über Darmhormone wichtig ist
Jeden Tag erneuert sich die Auskleidung Ihres Darms stillschweigend und ersetzt Millionen von Zellen, um Nahrung zu verdauen, Nährstoffe aufzunehmen und vor Krankheitserregern zu schützen. Dieser ständige Austausch hängt von Stammzellen ab, die tief in kleinen Taschen, den Krypten, verborgen liegen. Das Hormon T3, das von der Schilddrüse gebildet wird, beeinflusst Wachstum und Stoffwechsel im ganzen Körper, doch sein feinfacettiger Einfluss auf die erneuernden Zellen des Kolons war bislang unklar. Diese Studie nutzt Einzelzell-Genprofilierung, um einzelne Zellen im Mauskolon heranzuzoomen und zeigt, wie T3 sie in einen ungewöhnlichen, gemischten Zustand drängen kann, der für die Darmgesundheit und möglicherweise das Krebsrisiko von Bedeutung sein könnte.
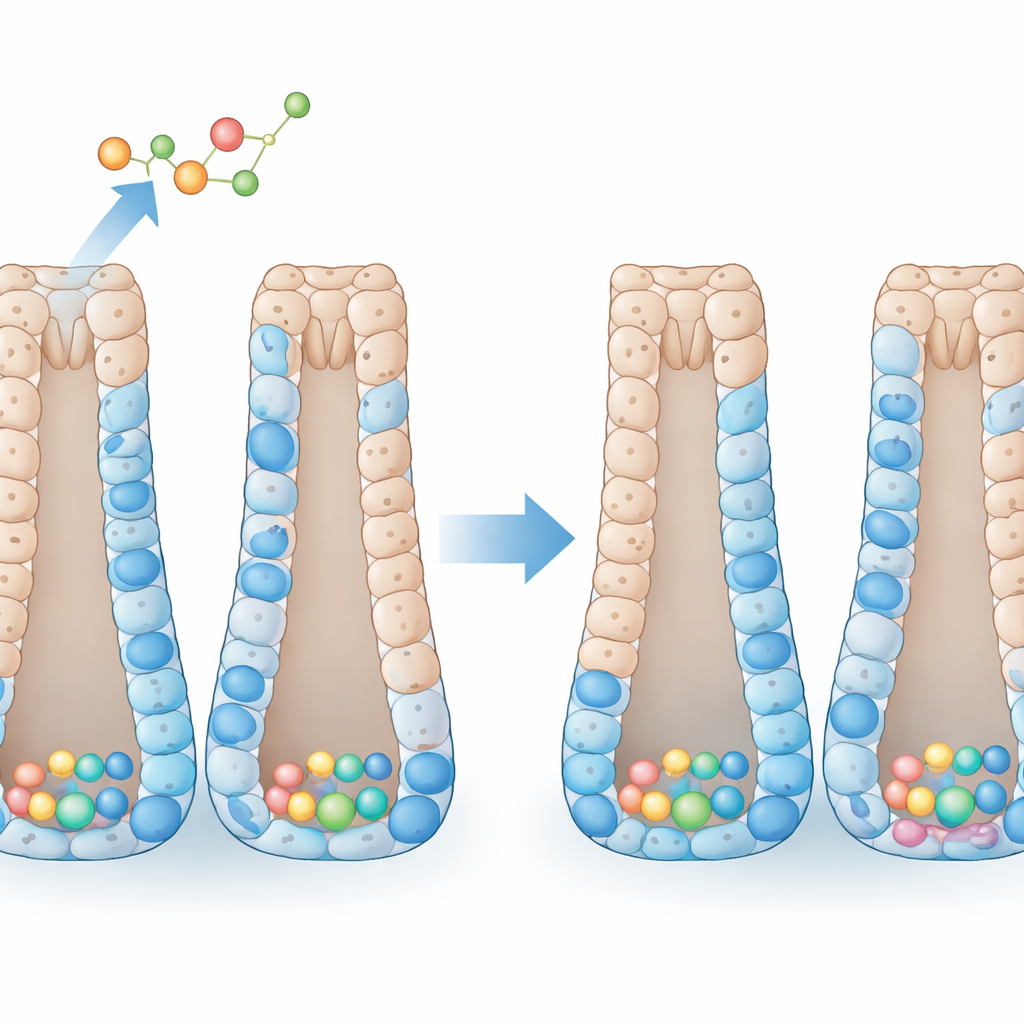
Wie das Kolon seine Form bewahrt
Die innere Schleimhaut des Kolons ist organisiert wie eine Reihe umgedrehter Reagenzgläser. Am Boden jedes Röhrchens sitzen Stammzellen, die sich teilen, um Progenitorzellen zu erzeugen. Während diese Progenitoren nach oben wandern, spezialisieren sie sich zu mehreren ausgereiften Typen: resorbierende Zellen, die Wasser und Nährstoffe aufnehmen, Becherzellen, die schützenden Schleim absondern, enteroendokrine Zellen, die Hormone produzieren, und Tuft-Zellen, die bei der Umweltsensorik helfen. Unter normalen Bedingungen hält ein enges Gleichgewicht zwischen Selbsterneuerung und Spezialisierung dieses System stabil. Viele interne Signale steuern diesen Prozess, aber weniger ist darüber bekannt, wie Ganzkörperhormone wie Schilddrüsenhormone ihn feinabstimmen, insbesondere im Kolon, das beim Menschen eine häufige Stelle für Tumoren ist.
Eine Einzelzell-Bestandsaufnahme nach Hormonexposition
Um T3s Rolle zu entschlüsseln, injizierten die Forscher erwachsenen Mäusen entweder T3 oder eine harmlose Salzlösung für zwei Tage und isolierten dann Kolonepithelzellen für die Einzelzell-RNA-Sequenzierung. Diese Technik liest ab, welche Gene in tausenden einzelnen Zellen aktiv sind, und erlaubt dem Team, Zellen anhand ihrer Expressionsmuster in verschiedene Typen einzuteilen. Nach Qualitätskontrolle analysierten sie mehr als 15.000 Zellen und identifizierten die erwarteten Familien: Stamm-/Progenitorzellen, sekretorische Zellen (einschließlich Becher- und verwandter Typen), proximale und distale resorbierende Zellen, hormonproduzierende Zellen und Tuft-Zellen. Jeder Cluster zeigte die erwarteten Gensignaturen entsprechend seiner bekannten Funktion, was bestätigt, dass die Einzelzell-Karte die zelluläre Landschaft des Kolons treu erfasste.
Das Hormon T3 lenkt Zellschicksale, ohne Zelltypen zu verändern
Im Vergleich zwischen T3-behandelten und Kontrollproben stellten die Autoren fest, dass T3 nicht dramatisch die Anzahl der Zellen in jeder breiten Kategorie veränderte, wohl aber die Aktivitäten vieler dieser Zellen. In mehreren Gruppen – besonders Stamm/Progenitor-, sekretorischen und resorbierenden Zellen – steigerte T3 die Aktivität von Genen, die typischerweise mit Becherzellen assoziiert sind, etwa solche, die an der Schleimproduktion beteiligt sind. Auffällig war, dass dies selbst in Zellen geschah, die keine klassischen Becherzellen waren. Gleichzeitig waren Gene, die an der Entgiftung von Chemikalien und dem Umgang mit oxidativem Stress beteiligt sind, allgemein heruntergeregelt, während Gene, die mit Abwehr und Entzündung verknüpft sind, hochreguliert wurden. Marker der Kernidentität von Stammzellen, wie Lgr5, änderten sich jedoch insgesamt wenig, was darauf hindeutet, dass T3 hauptsächlich das Verhalten von Vorläuferzellen umgestaltet statt Zelltypen vollständig neu zu definieren.
Ein gemischter, zwischen zwei Zuständen verhakter Zelltyp
Das Team nutzte anschließend rechnerische Werkzeuge, um wahrscheinliche „Trajektorien“ der Differenzierung zu rekonstruieren und nachzuzeichnen, wie Zellen sich von Stamm-/Progenitorzuständen zu ausgereiften Schicksalen entwickeln. In Kontrollkolons bildeten diese Pfade klare Verzweigungen, die zu sekretorischen und resorptiven Linien führten. Nach T3-Exposition verschwammen die Pfade: Die Zellzweige waren weniger deutlich, und bestimmte Linien, wie hormonproduzierende und Tuft-Zellen, erschienen weniger vollständig von ihren Progenitor-Ursprüngen getrennt. Ein genauerer Blick enthüllte eine „gemischte“ Population im T3-behandelten Gewebe, deren Zellen Marker früher Entscheidungsgene für sowohl resorptive als auch sekretorische Schicksale gleichzeitig exprimierten, zusammen mit späten becherzellbezogenen Genen. Wichtig ist, dass viele dieser Zellen auch hohe Werte von Proliferationsmarkern trugen, was darauf hinweist, dass sie sich noch aktiv teilten.
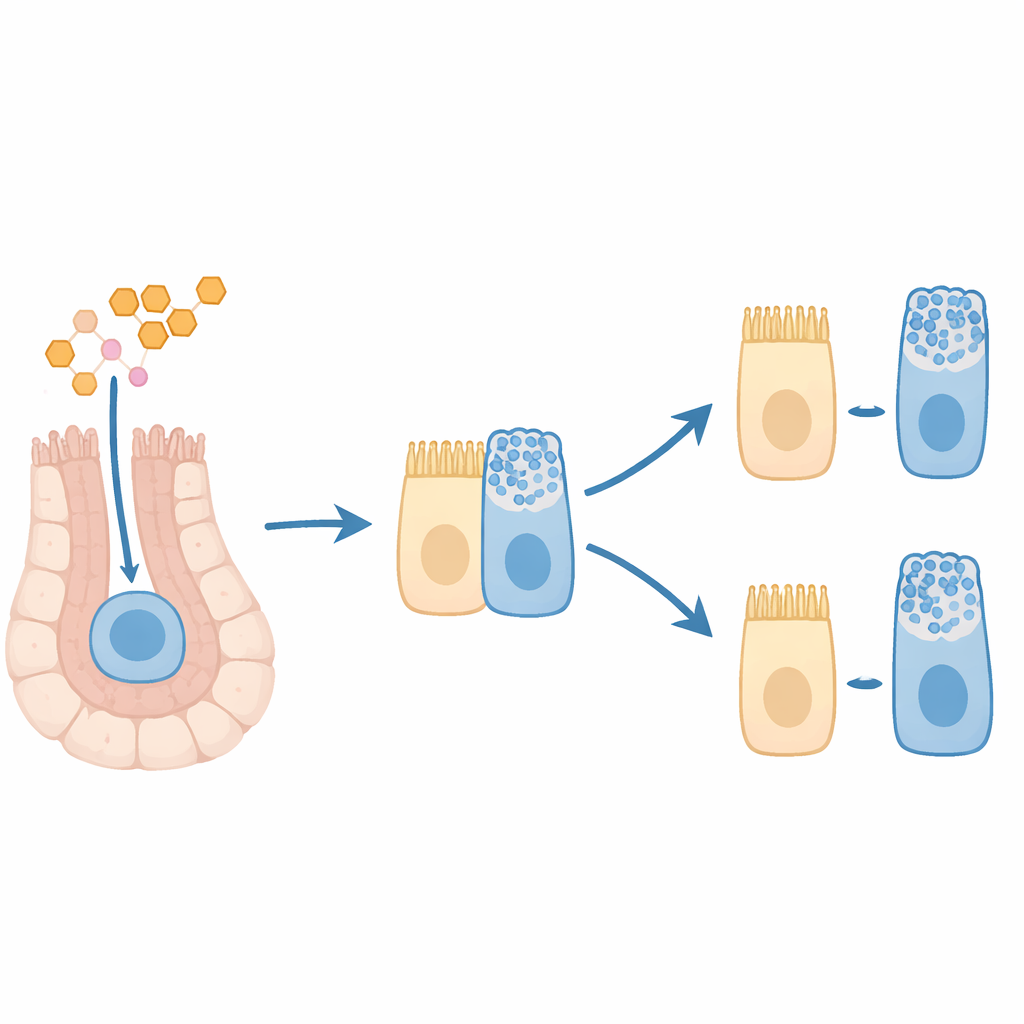
Früh zu Becherzellen tendierende Zellen im Gewebe sichtbar machen
Um zu prüfen, ob dieser gemischte Zustand in der tatsächlichen Kolongewebearchitektur auftaucht, färbten die Forscher Kolonabschnitte von Kontroll- und T3-behandelten Mäusen für Proteine an, die Proliferation und spezifische Zelltypen markieren. Sie beobachteten, dass T3 die Gesamtzahl ausgereifter Becherzellen entlang der Krypten nicht stark veränderte. Stattdessen führte T3 zu einer Ansammlung becherzellmarkerpositiver Zellen ganz unten in den Krypten – in der Zone, die normalerweise von Stamm- und frühen Progenitorzellen eingenommen wird. Viele dieser schleimmarkerpositiven Zellen waren auch positiv für einen Proliferationsmarker, was die Vorstellung stützt, dass T3 teilende Vorläufer erzeugt, die bereits in Richtung Becherzellschicksal tendieren, aber noch nicht voll ausgereift sind.
Was das für die Darmgesundheit bedeutet
Für eine nichtfachliche Beobachterin ist die zentrale Botschaft der Studie: Das Schilddrüsenhormon T3 kann Kolonvorläuferzellen in einen Hybridzustand drängen: Sie teilen sich wie stammzellähnliche Zellen, tragen aber bereits Merkmale schleimabsondernder Becherzellen und scheinen vor der vollständigen Reifung ins Stocken zu geraten. Da das richtige Timing von Schicksalsentscheidungen für eine gesunde Kolonschleimhaut entscheidend ist, könnten solche gemischten, unreifen Populationen bei längerer oder übermäßiger Hormonexposition anfälliger für Stress oder maligne Veränderungen werden. Obwohl diese Arbeit an Mäusen und mit Kurzzeitbehandlung durchgeführt wurde, hebt sie eine zuvor unerkannte Weise hervor, wie Schilddrüsenhormon die Kolonregeneration prägt, und wirft neue Fragen darauf auf, wie veränderte Schilddrüsenzustände das Kolonleiden und Krebsrisiko beim Menschen beeinflussen könnten.
Zitation: Bidoli, C., Reslinger, M., Sieffert, C. et al. Single-cell analysis reveals that the hormone T3 affects colon epithelial differentiation and induces a mixed progenitor-like cell population. Sci Rep 16, 10369 (2026). https://doi.org/10.1038/s41598-026-40397-7
Schlüsselwörter: Kolonepithel, Schilddrüsenhormon T3, Einzelzell-RNA-Sequenzierung, Becherzell-Differenzierung, intestinale Stammzellen