Clear Sky Science · pt
Transmissão de clones de Salmonella entre diferentes espécies animais em uma região de criação de cavalos e bovinos no Japão
Por que germes que saltam entre animais de fazenda importam
O envenenamento alimentar por Salmonella é um problema global que pode começar muito antes dos alimentos chegarem às nossas cozinhas. Frequentemente tem início nas fazendas, onde os mesmos germes podem se mover silenciosamente entre diferentes animais e depois entrar na cadeia alimentar humana. Este estudo examina de perto uma movimentada região de criação de cavalos e bovinos no norte do Japão para entender como um tipo particularmente bem‑sucedido de Salmonella se espalha entre espécies, e se isso faz parte de um problema local, de uma onda global de infecção, ou de ambos.
Um germe resistente com gosto por muitos hospedeiros
Os pesquisadores concentraram‑se em uma forma de Salmonella, chamada tipo de sequência 34 (ST34), que hoje é uma das causas mais comuns de diarreia tanto em pessoas quanto em animais no mundo todo. Ao contrário de algumas cepas de Salmonella que se especializam em um hospedeiro, a ST34 infecta livremente muitos mamíferos e aves. Frequentemente carrega múltiplos genes que a tornam resistente a antibióticos importantes e capaz de tolerar metais como cobre ou zinco — características que a ajudam a sobreviver nas fazendas modernas. O Japão tem visto ondas repetidas de diferentes cepas de Salmonella nas últimas quatro décadas, e a ST34 tornou‑se o tipo dominante em bovinos desde os anos 2010.
Rastreando infecções entre fazendas e ao longo dos anos
Para entender como a ST34 se comporta onde cavalos e bovinos convivem lado a lado, a equipe analisou 42 amostras de Salmonella coletadas de animais em um distrito de Hokkaido entre 1981 e 2023. Usando sequenciamento do genoma completo, eles leram quase todo o código de DNA de cada isolado bacteriano e compararam pequenas diferenças, conhecidas como alterações de nucleotídeo único, em seus genomas centrais. Cepas que diferiam por menos de 25 dessas alterações foram agrupadas em cinco “aglomerados” intimamente relacionados, indicando que se separaram de um ancestral comum relativamente recentemente. Na maioria dos aglomerados, bactérias quase idênticas foram encontradas tanto em cavalos quanto em bovinos em fazendas diferentes, às vezes anos depois e a dezenas de quilômetros de distância, o que aponta fortemente para transmissão entre espécies e entre fazendas.
Surtos locais dentro de uma árvore genealógica global
Os cientistas então colocaram as cepas de Hokkaido em um contexto global ao compará‑las com quase 500 genomas ST34 de 28 países. Essa análise mais ampla revelou três ramos principais, ou clados, na árvore genealógica da Salmonella. Dois ramos consistiam em grande parte de cepas que circularam dentro do Japão e foram rotulados como linhagens epidêmicas japonesas, enquanto o terceiro ramo continha uma mistura de cepas da Europa, Ásia, Américas, África e Oceania e foi considerado a linhagem global. Três dos aglomerados de Hokkaido enquadraram‑se claramente em uma linhagem epidêmica japonesa, mostrando que infecções locais em cavalos e bovinos faziam parte de um problema nacional mais amplo e de longa duração. Outro aglomerado agrupou‑se com cepas de países do Leste Asiático, como China e Coreia do Sul, e ainda outro mostrou vínculos genéticos com cepas europeias, sugerindo introduções repetidas do exterior.
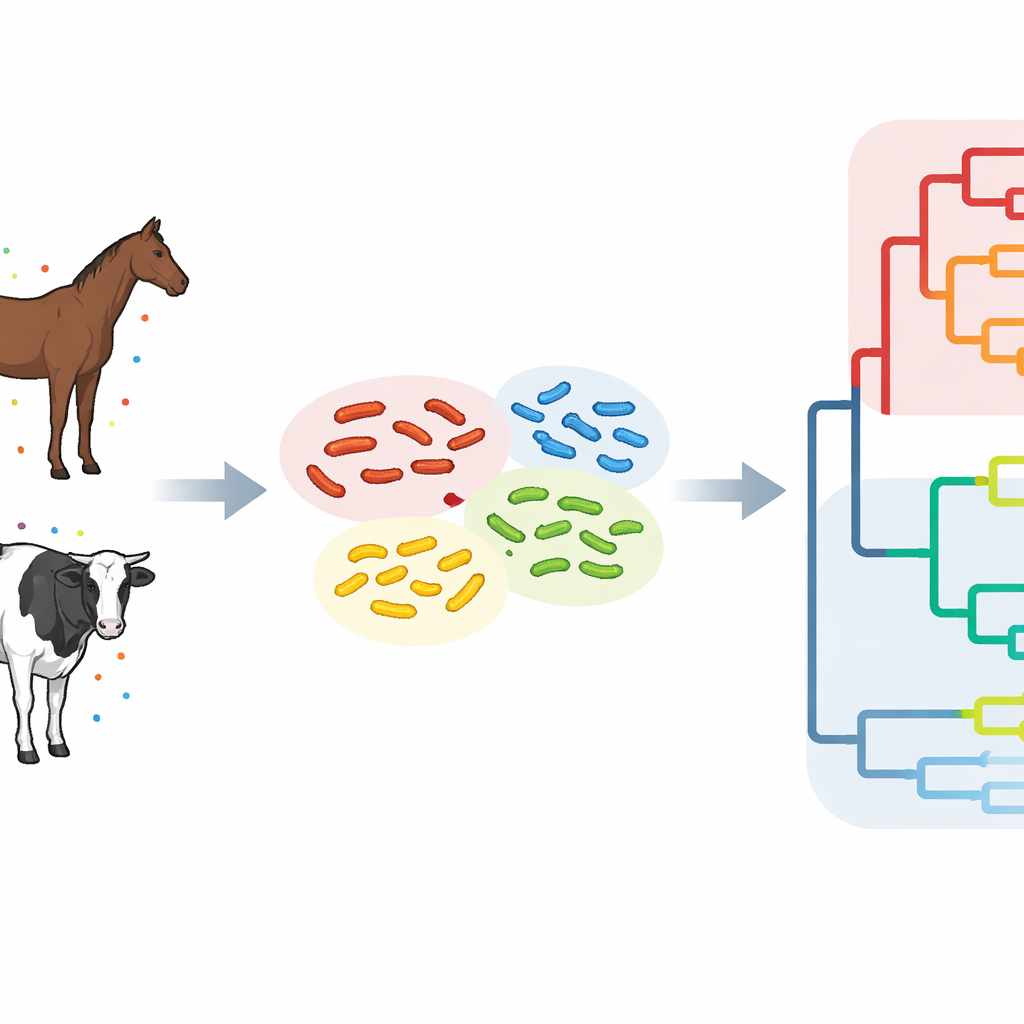
Rotas de viagem ocultas e aumento da resistência a medicamentos
Ao estimar quando diferentes ramos se separaram uns dos outros, a equipe concluiu que a principal linhagem ST34 do Japão se separou da linhagem global no final dos anos 1990 ou início dos anos 2000 e então se adaptou a animais de produção dentro do país. Ao mesmo tempo, pelo menos uma sublinhagem do Leste Asiático que carrega genes extras de resistência a medicamentos parece ter entrado no Japão separadamente. Embora os caminhos exatos não sejam claros, os padrões sugerem que o movimento de animais, rações contaminadas, veículos ou até animais selvagens como aves e guaxinins podem estar transportando essas bactérias entre fazendas e espécies. Quase todas as cepas carregavam um conjunto central de genes de resistência a antibióticos comuns, e algumas possuíam genes adicionais que poderiam dificultar o tratamento caso essas bactérias atinjam pessoas.
O que isso significa para fazendas e segurança alimentar
Para o leitor em geral, a mensagem principal é que germes perigosos não respeitam fronteiras entre espécies nem cercas de fazenda. Neste distrito japonês, os mesmos clones de Salmonella foram encontrados tanto em cavalos quanto em bovinos e puderam ser ligados geneticamente a ondas maiores de infecção em nível nacional e internacional. O estudo mostra que o rastreamento cuidadoso por DNA pode revelar como essas bactérias se movem silenciosamente através de animais, regiões e fronteiras. Para reduzir o risco de intoxicação alimentar e doenças animais, os programas de controle de doenças não podem focar em uma única espécie ou em um único país: eles devem vigiar saltos entre espécies, limitar a disseminação de cepas resistentes a medicamentos e encarar fazendas, vida selvagem e comércio global como partes de um sistema interconectado.
Citação: Arai, N., Niwa, H., Uchida-Fujii, E. et al. Transmission of Salmonella clones between different animal species in a horse and cattle breeding region in Japan. Sci Rep 16, 12412 (2026). https://doi.org/10.1038/s41598-026-39311-y
Palavras-chave: Salmonella, transmissão entre espécies, resistência a antibióticos, pecuária, sequenciamento do genoma