Clear Sky Science · pt
Sintese eletrossintética pulsada otimiza ortogonalmente o acoplamento C‒N e a hidrogenação para produção de aminas com um catalisador molecular
Transformando Resíduos em Ingredientes Úteis
Dióxido de carbono no ar e nitrato na água costumam ser vistos como poluentes, associados às mudanças climáticas e a florescimentos de algas. Este estudo explora como tratá‑los em vez disso como matérias‑primas, convertendo‑os em aminas – compostos básicos usados em fertilizantes, medicamentos e produtos do dia a dia. Ao aplicar pulsos de eletricidade de forma inteligente através de um catalisador molecular especial, os pesquisadores mostram que podemos produzir esses compostos de forma mais rápida e seletiva, ao mesmo tempo em que potencialmente reduzimos fluxos de resíduos.
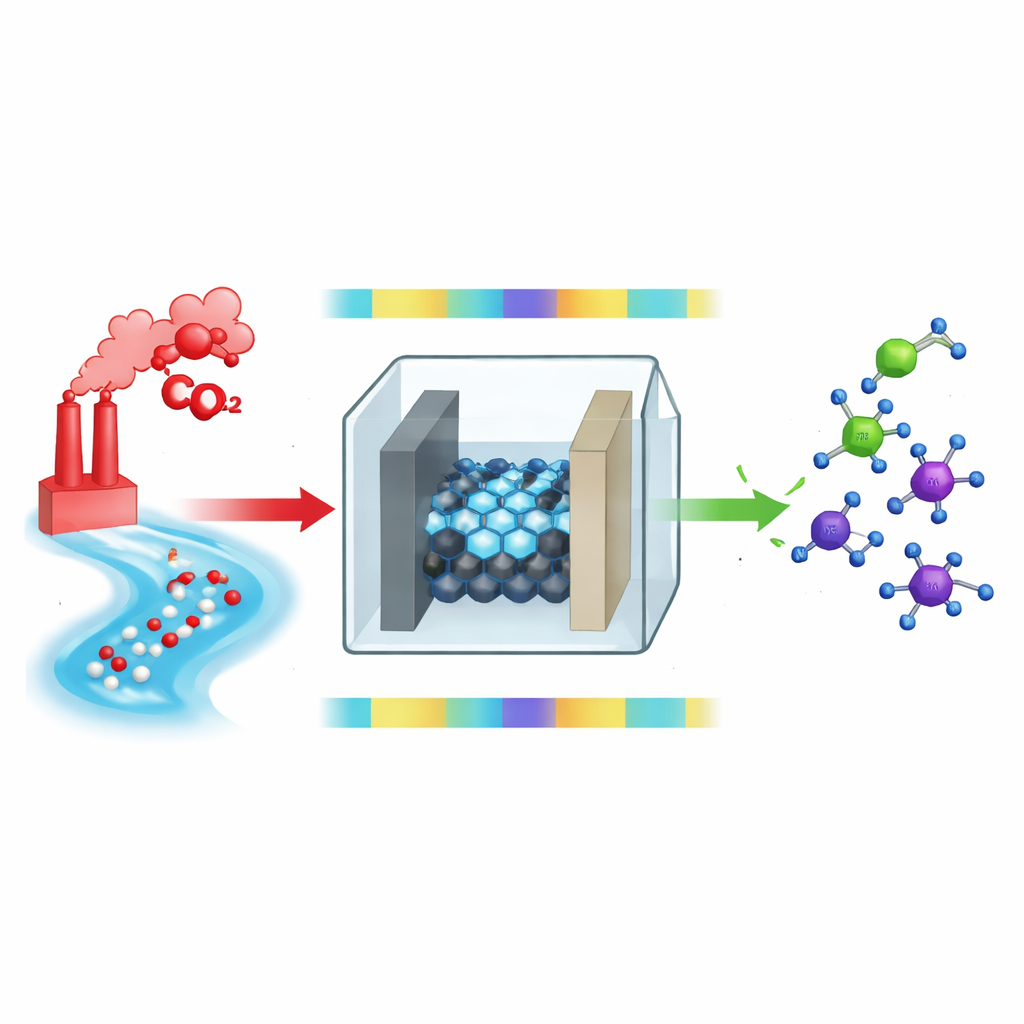
De Poluentes a Moléculas Valiosas
A ideia central é alimentar dióxido de carbono do ar e nitrato de água contaminada em uma célula eletroquímica, onde a eletricidade os conduz a formar novas ligações entre carbono e nitrogênio. Essas ligações geram aminas, que são ingredientes centrais em muitos processos industriais e farmacêuticos. Em um arranjo típico, o dióxido de carbono e o nitrato são reduzidos – isto é, ganham elétrons e prótons – e reagem para formar compostos intermediários como oximas, que então precisam ser ainda “hidrogenados” para se tornarem aminas. Enquanto a primeira etapa de formação da ligação é relativamente rápida, as etapas posteriores de hidrogenação são lentas e ineficientes, criando um gargalo que limita tanto o rendimento quanto a eficiência energética.
Por Que Eletricidade Estática é Insuficiente
Tradicionalmente, químicos aplicam uma única voltagem fixa nos eletrodos e tentam escolher um compromisso que funcione para todas as etapas da reação. Mas os estágios iniciais e finais preferem condições muito diferentes. Em tensões firmes e negativas, a superfície do catalisador fica saturada de hidrogênio, o que acelera a hidrogenação, mas também promove reações colaterais indesejadas, como formação de gás hidrogênio e amônia. Em voltagens mais brandas, os acoplamentos carbono–nitrogênio cruciais se formam de maneira mais limpa, porém os intermediários não podem ser totalmente convertidos em aminas. Esse descompasso dificulta projetar um único ponto operacional estático que ofereça alta seletividade para os produtos desejados.
Pulsando a Corrente para Dividir a Função
Para resolver isso, os autores introduzem uma estratégia pulsada: alternam rapidamente entre uma voltagem menos negativa e outra mais negativa. Durante a fase suave, a superfície de um catalisador de fitalocianina de cobalto suportado em nanotubos de carbono acumula intermediários carbono–nitrogênio, como formaldoxima, sem superreduzi‑los. Em seguida, durante os pulsos mais profundos e breves, a força adicional acelera a hidrogenação, empurrando esses intermediários em direção à metilamina e até a aminas superiores como dimetilamina e trimetilamina. Essa abordagem de compartilhamento temporal permite que cada etapa da reação viva suas condições preferidas, em vez de forçar todas a ocorrerem sob o mesmo compromisso de voltagem.
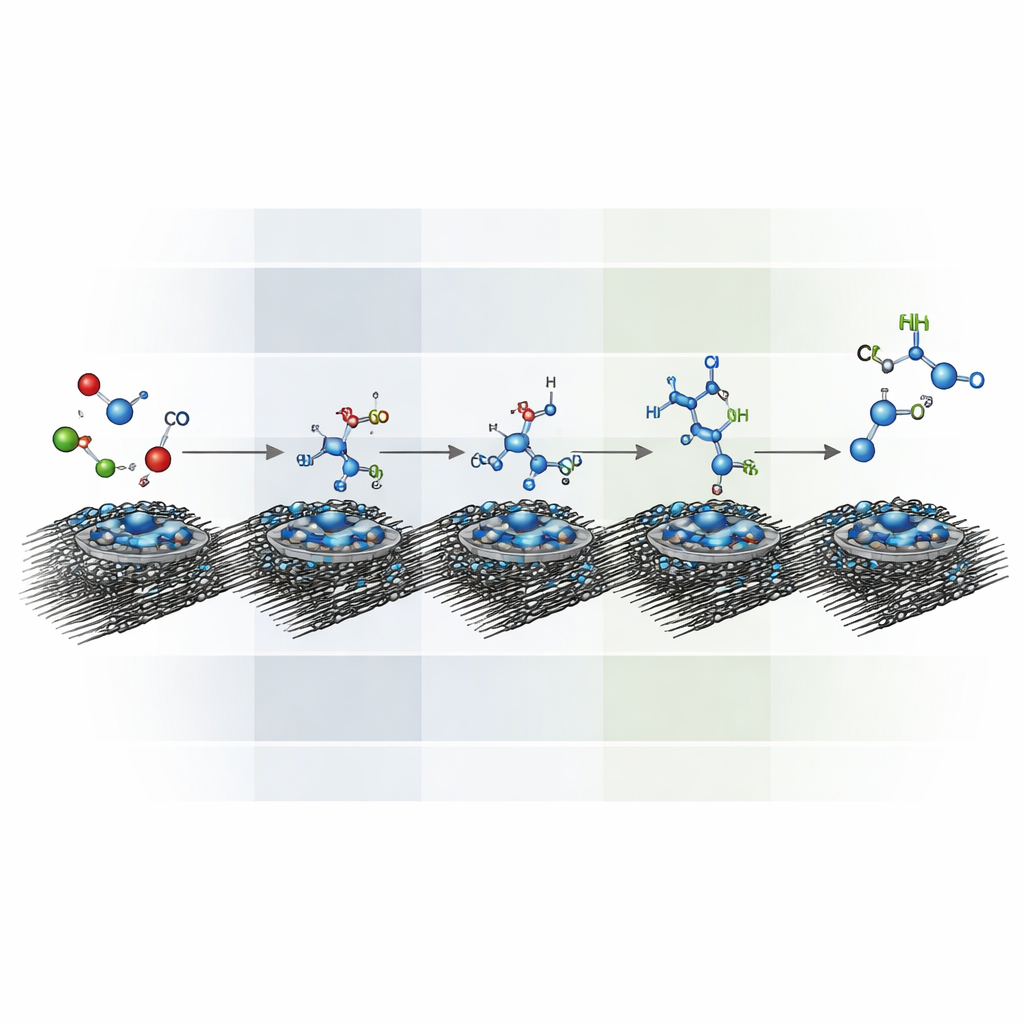
Vendo Dentro das Etapas da Reação
A equipe usou uma combinação de ferramentas avançadas para observar e calcular o que acontece na superfície do catalisador. Espectroscopia no infravermelho detectou assinaturas vibracionais específicas de espécies intermediárias, mostrando como duplas ligações carbono–nitrogênio cedem lugar a ligações simples conforme a hidrogenação avança nos pulsos mais negativos. Espectrometria de massa monitorou fragmentos gasosos como monóxido de carbono, unidades semelhantes a formaldeído e hidroxilamina, revelando como eles aparecem e desaparecem conforme a voltagem varia. Experimentos com marcação isotópica, nos quais versões mais pesadas de carbono e nitrogênio foram usadas, confirmaram que todos os átomos de carbono e nitrogênio nos produtos realmente se originam do dióxido de carbono e do nitrato. Simulações computacionais baseadas na mecânica quântica então mapearam o panorama energético, indicando que pulsos mais profundos tornam etapas-chave de hidrogenação mais favoráveis, embora ainda exijam controle cuidadoso para evitar reações secundárias.
Construindo Aminas Mais Complexas
Ao realimentar parte dos produtos como matérias‑primas, os pesquisadores traçaram como se formam as aminas superiores. Seus testes sugerem uma via em etapas: dióxido de carbono e nitrato primeiro produzem hidroxilamina e formaldeído, que se unem para formar formaldoxima; esta é então hidrogenada a metilhidroxilamina e adiante para metilamina. Metilhidroxilamina e metilamina podem então reagir com mais formaldeído e sofrer hidrogenação adicional para gerar dimetilamina e, finalmente, trimetilamina. A operação em pulsos não só acelera a reação como também melhora a seletividade, aproximadamente triplicando a taxa e dobrando a fração de corrente que resulta em metilamina em comparação com condições estáticas, mantendo o catalisador molecular à base de cobalto em grande parte intacto.
O Que Isso Significa para um Futuro Mais Limpo
Para um leitor não especialista, a mensagem principal é que rajadas de eletricidade cuidadosamente cronometradas podem dirigir reações químicas complexas assim como um maestro guia uma orquestra. Em vez de lutar contra as diferenças naturais entre etapas rápidas e lentas, essa abordagem pulsada dá a cada estágio as condições que precisa, transformando poluentes problemáticos em produtos úteis com mais eficiência. Embora avanços adicionais sejam necessários antes da aplicação em larga escala, o trabalho delineia um roteiro geral: o controle dinâmico da voltagem pode desbloquear novas rotas para transformar carbono e nitrogênio residuais em produtos valiosos, aproximando a fabricação química mais sustentável.
Citação: Yan, S., Wang, Y., Chen, S. et al. Pulsed electrosynthesis orthogonally optimizes C‒N coupling and hydrogenation for amine production with a molecular catalyst. Nat Commun 17, 4027 (2026). https://doi.org/10.1038/s41467-026-72678-0
Palavras-chave: síntese eletroquímica de aminas, upcycling de CO2, redução de nitrato, eletrólise em pulsos, formação de ligações C–N