Clear Sky Science · fr
Synthèse électrochimique par impulsions optimisant orthogonalement l’assemblage C‒N et l’hydrogénation pour la production d’amines avec un catalyseur moléculaire
Transformer les déchets en ingrédients utiles
Le dioxyde de carbone dans l’air et les nitrates dans l’eau sont généralement considérés comme des polluants, liés au changement climatique et aux proliférations d’algues. Cette étude examine comment les considérer plutôt comme des matières premières, en les convertissant en amines – des produits chimiques de base utilisés dans les engrais, les médicaments et des produits du quotidien. En appliquant intelligemment des impulsions électriques à travers un catalyseur moléculaire spécial, les chercheurs montrent qu’on peut fabriquer ces composés utiles plus rapidement et de manière plus sélective, tout en réduisant potentiellement les flux de déchets.
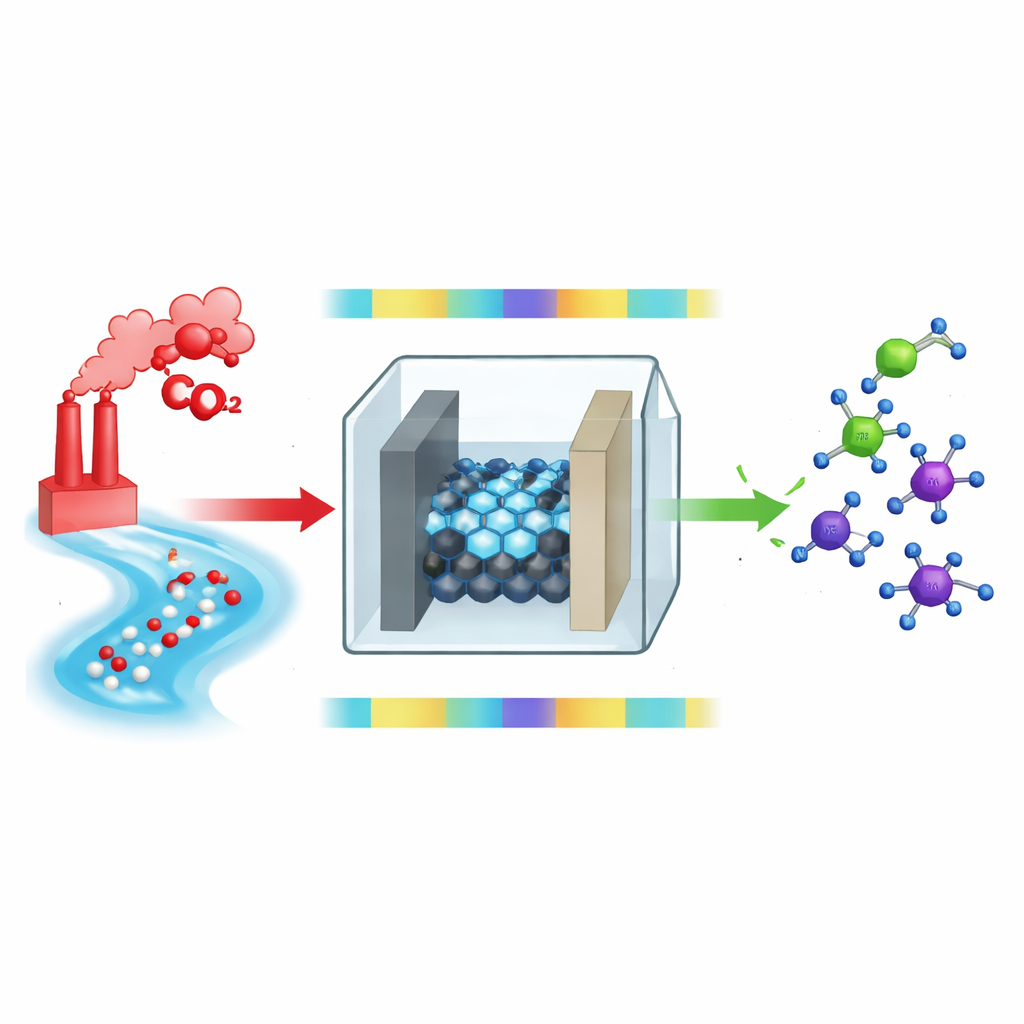
Des polluants aux molécules de valeur
L’idée centrale est d’alimenter du dioxyde de carbone de l’air et des nitrates d’eaux contaminées dans une cellule électrochimique, où l’électricité les conduit à former de nouvelles liaisons entre le carbone et l’azote. Ces liaisons donnent des amines, qui sont des ingrédients essentiels dans de nombreux procédés industriels et pharmaceutiques. Dans un dispositif type, le CO2 et les nitrates sont réduits – c’est‑à‑dire qu’ils gagnent des électrons et des protons – et réagissent pour former des composés intermédiaires tels que des oximes, qui doivent ensuite être davantage « hydrogénés » pour devenir des amines. Alors que la première étape de formation de la liaison est relativement rapide, les étapes d’hydrogénation ultérieures sont lentes et inefficaces, créant un goulet d’étranglement qui limite à la fois le rendement et l’efficacité énergétique.
Pourquoi l’électricité statique ne suffit pas
Traditionnellement, les chimistes appliquent une tension fixe aux électrodes en espérant trouver un compromis qui conviendra à toutes les étapes de la réaction. Mais les étapes initiales et finales préfèrent des conditions très différentes. À des tensions fortement négatives et constantes, la surface du catalyseur devient saturée d’hydrogène, ce qui accélère l’hydrogénation mais favorise aussi des réactions secondaires indésirables, comme la formation d’hydrogène gazeux et d’ammoniac. À des tensions plus modérées, les couplages carbone–azote se forment plus proprement, mais les intermédiaires ne peuvent pas être entièrement convertis en amines. Ce décalage rend difficile la conception d’un point de fonctionnement statique unique donnant une forte sélectivité pour les produits désirés.
Pulser le courant pour séparer les tâches
Pour remédier à cela, les auteurs proposent une stratégie pulsée : ils alternent rapidement entre une tension moins négative et une tension plus négative. Pendant la phase douce, la surface d’un catalyseur à base de phthalocyanine de cobalt soutenu sur des nanotubes de carbone accumule des intermédiaires carbone–azote tels que le formaldoxime, sans les sur-réduire. Puis, durant de brèves impulsions plus profondes, la force motrice supplémentaire accélère l’hydrogénation, poussant ces intermédiaires vers la méthylamine et des amines supérieures comme la diméthylamine et la triméthylamine. Cette approche de partage temporel permet à chaque étape réactionnelle de bénéficier des conditions qui lui conviennent, plutôt que d’imposer un même compromis à toutes les étapes.
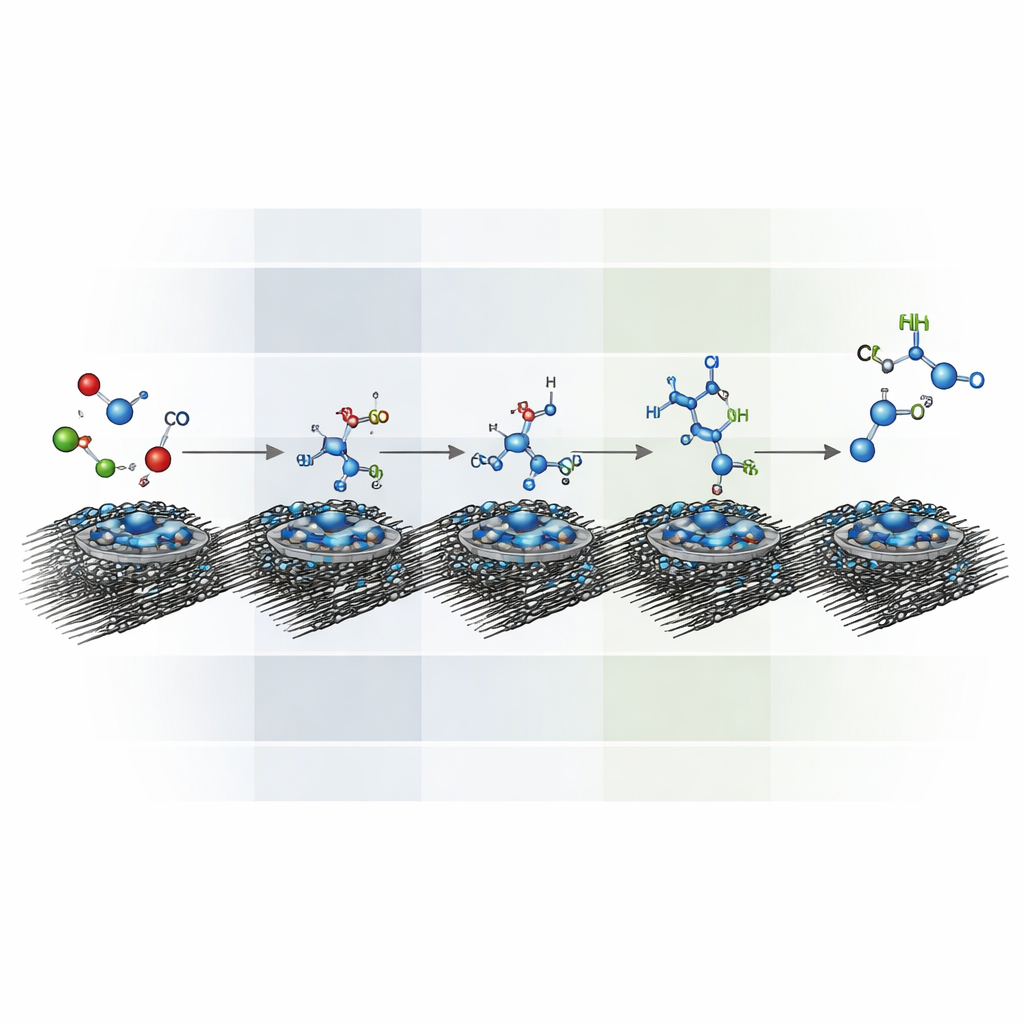
Observer l’intérieur des étapes réactionnelles
L’équipe a utilisé une combinaison d’outils avancés pour observer et calculer ce qui se passe à la surface du catalyseur. La spectroscopie infrarouge a détecté des empreintes vibrationnelles spécifiques d’espèces intermédiaires, montrant comment les doubles liaisons carbone–azote cèdent la place à des liaisons simples au fur et à mesure que l’hydrogénation progresse lors des impulsions plus négatives. La spectrométrie de masse a suivi des fragments gazeux tels que le monoxyde de carbone, des unités proches du formaldéhyde et l’hydroxylamine, révélant leur apparition et disparition au fil des variations de tension. Des expériences d’étiquetage isotopique, où des versions plus lourdes du carbone et de l’azote ont été utilisées, ont confirmé que tous les atomes de carbone et d’azote présents dans les produits proviennent bien du CO2 et des nitrates. Des simulations informatiques basées sur la mécanique quantique ont ensuite cartographié le paysage énergétique, indiquant que les impulsions plus profondes rendent certaines étapes clés d’hydrogénation plus favorables, tout en nécessitant un contrôle précis pour éviter les réactions secondaires.
Évolution vers des amines plus complexes
En réinjectant certains des produits comme matières premières, les chercheurs ont retracé la formation des amines supérieures. Leurs essais suggèrent une voie étape par étape : le CO2 et les nitrates produisent d’abord de l’hydroxylamine et du formaldéhyde, qui se combinent pour former le formaldoxime ; celui‑ci est ensuite hydrogéné en méthylhydroxylamine puis en méthylamine. La méthylhydroxylamine et la méthylamine peuvent alors réagir avec davantage de formaldéhyde et subir d’autres hydrogénations pour donner la diméthylamine puis la triméthylamine. L’opération pulsée accélère non seulement la réaction mais améliore aussi la sélectivité, multipliant approximativement par trois la vitesse et doublant la fraction du courant qui aboutit en méthylamine par rapport aux conditions statiques, tout en préservant largement l’intégrité du catalyseur moléculaire à base de cobalt.
Ce que cela signifie pour un avenir plus propre
Pour un non‑spécialiste, le message principal est que des rafales d’électricité soigneusement chronométrées peuvent orienter des réactions chimiques complexes comme un chef d’orchestre guide une symphonie. Plutôt que de lutter contre les différences naturelles entre étapes rapides et lentes, cette approche pulsée offre à chaque phase les conditions dont elle a besoin, transformant des polluants problématiques en produits utiles de façon plus efficiente. Bien que des avancées supplémentaires soient nécessaires avant une utilisation à grande échelle, le travail esquisse un plan général : le contrôle dynamique de la tension peut débloquer de nouvelles voies pour transformer le carbone et l’azote issus de déchets en produits de valeur, rapprochant la chimie industrielle d’une option plus verte.
Citation: Yan, S., Wang, Y., Chen, S. et al. Pulsed electrosynthesis orthogonally optimizes C‒N coupling and hydrogenation for amine production with a molecular catalyst. Nat Commun 17, 4027 (2026). https://doi.org/10.1038/s41467-026-72678-0
Mots-clés: synthèse électrochimique d’amines, recyclage du CO2, réduction des nitrates, électrolyse pulsée, formation de liaison C–N