Clear Sky Science · es
La electrosíntesis pulsada optimiza de forma ortogonal el acoplamiento C‒N y la hidrogenación para la producción de aminas con un catalizador molecular
Convertir residuos en ingredientes útiles
El dióxido de carbono en el aire y el nitrato en el agua suelen considerarse contaminantes, asociados al cambio climático y a las proliferaciones de algas. Este trabajo explora cómo tratarlos en cambio como materias primas, convirtiéndolos en aminas: compuestos básicos empleados en fertilizantes, medicamentos y productos de uso cotidiano. Mediante pulsos eléctricos aplicados con astucia sobre un catalizador molecular especial, los autores demuestran que es posible fabricar estos compuestos de forma más rápida y selectiva, al mismo tiempo que se reducen potencialmente los flujos de residuos.
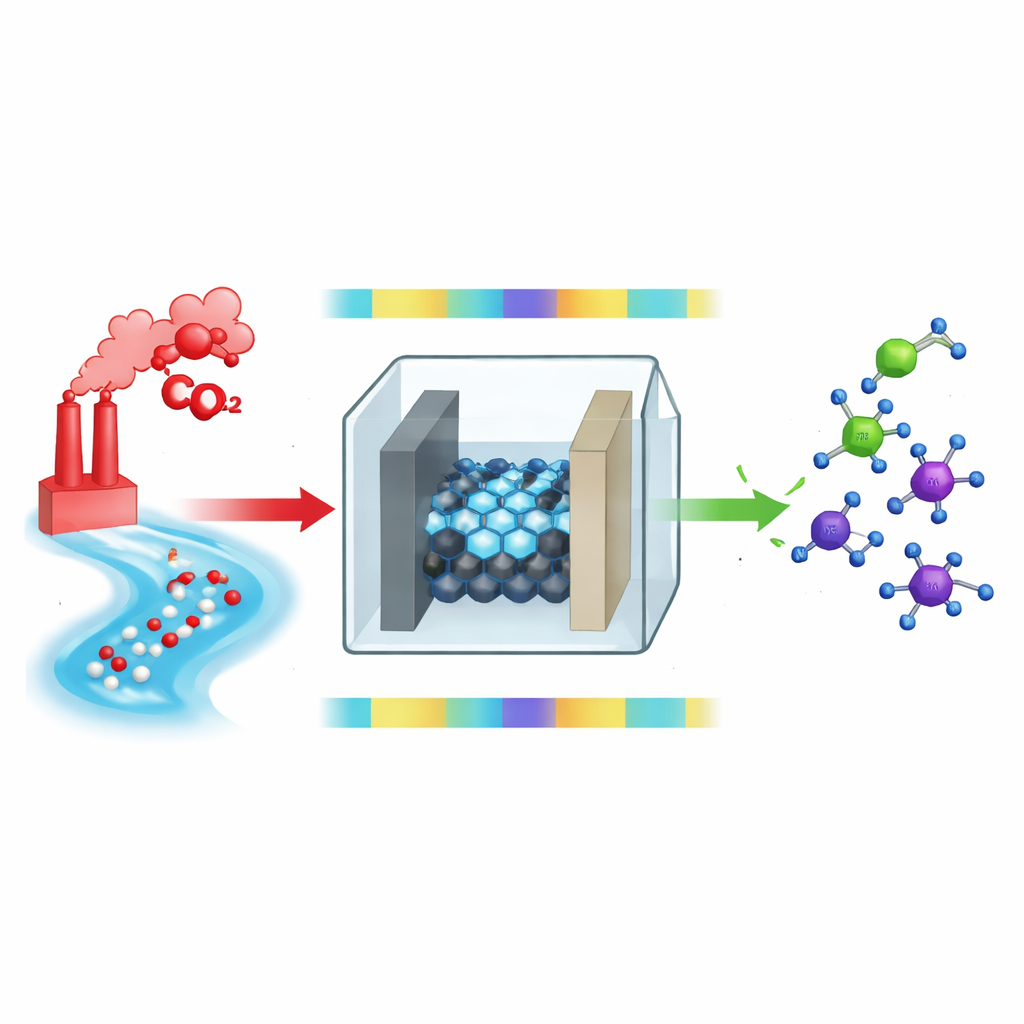
De contaminantes a moléculas valiosas
La idea central es alimentar dióxido de carbono del aire y nitrato de agua contaminada a una celda electroquímica, donde la electricidad los impulsa a formar nuevos enlaces entre carbono y nitrógeno. Esos enlaces generan aminas, que son ingredientes clave en muchos procesos industriales y farmacéuticos. En una configuración típica, el dióxido de carbono y el nitrato se reducen —es decir, ganan electrones y protones— y reaccionan para formar compuestos intermedios como oximas, que luego deben ser “hidrogenados” adicionalmente para convertirse en aminas. Mientras que el primer paso de unión es relativamente rápido, las etapas posteriores de hidrogenación son lentas e ineficientes, creando un cuello de botella que limita tanto el rendimiento como la eficiencia energética.
Por qué la electricidad estática se queda corta
Tradicionalmente, los químicos aplican una única tensión fija a los electrodos esperando hallar un compromiso que funcione para todos los pasos de la reacción. Pero las etapas tempranas y tardías prefieren condiciones muy diferentes. A tensiones constantes y fuertemente negativas, la superficie del catalizador se llena de hidrógeno, lo que acelera la hidrogenación pero también promueve reacciones secundarias indeseadas como la formación de gas hidrógeno y amoníaco. A tensiones más suaves, las parejas carbono–nitrógeno se forman con mayor limpieza, sin embargo los intermedios no pueden convertirse completamente en aminas. Esta descoordinación dificulta diseñar un único punto operativo estático que ofrezca alta selectividad hacia los productos deseados.
Pulsar la corriente para dividir la tarea
Para resolverlo, los autores introducen una estrategia pulsada: alternan rápidamente entre una tensión menos negativa y otra más negativa. Durante la fase suave, la superficie de un catalizador de ftalocianina de cobalto soportado sobre nanotubos de carbono acumula intermedios carbono–nitrógeno como la formaldoxima, sin sobrerreducirlos. Luego, durante los pulsos más profundos y breves, el mayor impulso acelera la hidrogenación, empujando esos intermedios hacia la metilamina e incluso aminas superiores como dimetilamina y trimetilamina. Este enfoque de reparto temporal permite que cada paso reaccional experimente sus condiciones preferidas en lugar de forzar todos los pasos bajo el mismo voltaje de compromiso.
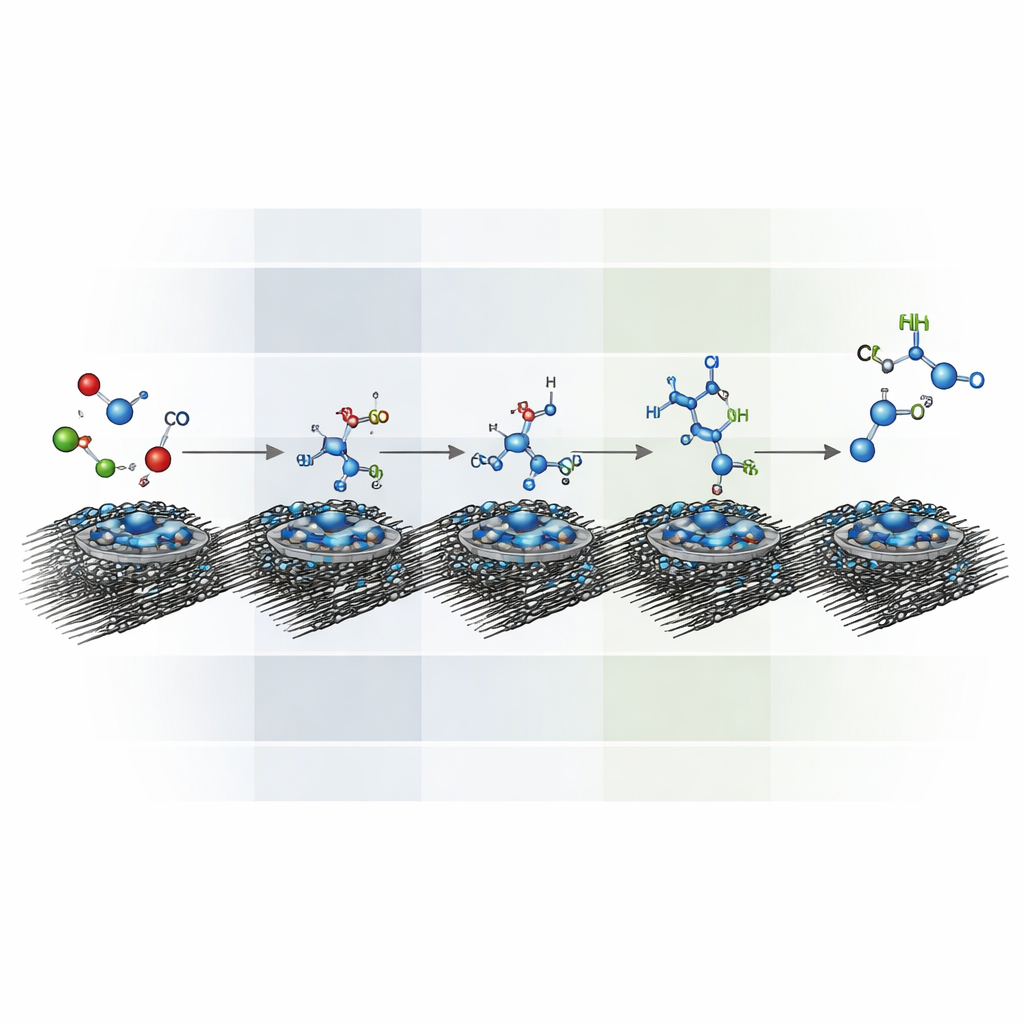
Asomarse al interior de los pasos de reacción
El equipo empleó una combinación de herramientas avanzadas para observar y calcular lo que ocurre en la superficie del catalizador. La espectroscopía infrarroja detectó huellas vibracionales específicas de especies intermedias, mostrando cómo los dobles enlaces carbono–nitrógeno dan paso a enlaces sencillos conforme la hidrogenación avanza en los pulsos más negativos. La espectrometría de masas monitorizó fragmentos gaseosos como monóxido de carbono, unidades tipo formaldehído e hidroxilamina, revelando cómo aparecen y desaparecen al cambiar la tensión. Experimentos de marcado isotópico, donde se usaron versiones más pesadas de carbono y nitrógeno, confirmaron que todos los átomos de carbono y nitrógeno en los productos proceden efectivamente del dióxido de carbono y del nitrato. Simulaciones computacionales basadas en la mecánica cuántica trazaron luego el paisaje energético, indicando que los pulsos más profundos hacen que pasos clave de hidrogenación resulten más favorables aunque requieren control cuidadoso para evitar reacciones secundarias.
Construyendo aminas más complejas
Al reintroducir parte de los productos como materias primas, los investigadores siguieron la formación de aminas superiores. Sus pruebas sugieren una vía escalonada: dióxido de carbono y nitrato primero producen hidroxilamina y formaldehído, que se combinan para formar formaldoxima; esta se hidrogena entonces a metilhidroxilamina y, sucesivamente, a metilamina. Metilhidroxilamina y metilamina pueden reaccionar con más formaldehído y sufrir hidrogenación adicional para dar dimetilamina y finalmente trimetilamina. La operación pulsada no solo acelera la reacción sino que también mejora la selectividad: aproximadamente triplica la velocidad y duplica la fracción de corriente que termina como metilamina en comparación con condiciones estáticas, manteniendo a la vez el catalizador molecular a base de cobalto en gran medida intacto.
Qué significa esto para un futuro más limpio
Para un público no especializado, el mensaje principal es que pulsos eléctricos cuidadosamente temporizados pueden dirigir reacciones químicas complejas como un director guía a una orquesta. En lugar de combatir las diferencias naturales entre pasos rápidos y lentos, este enfoque pulsado proporciona a cada etapa las condiciones que necesita, convirtiendo contaminantes problemáticos en productos útiles con mayor eficiencia. Aunque se requieren avances adicionales antes de su escalado industrial, el trabajo traza un plano general: el control dinámico de la tensión puede desbloquear nuevas vías para transformar el carbono y el nitrógeno residuales en productos valiosos, acercando un paso más una química manufacturera más verde.
Cita: Yan, S., Wang, Y., Chen, S. et al. Pulsed electrosynthesis orthogonally optimizes C‒N coupling and hydrogenation for amine production with a molecular catalyst. Nat Commun 17, 4027 (2026). https://doi.org/10.1038/s41467-026-72678-0
Palabras clave: síntesis electroquímica de aminas, revalorización del CO2, reducción de nitratos, electrólisis pulsada, formación de enlaces C–N