Clear Sky Science · pt
Complexo repressivo-deubiquitinase Polycomb protege o epigenoma do oócito e a fertilidade feminina ao conter a atividade do Polycomb
Por que óvulos saudáveis importam para a vida futura
Toda gravidez começa com uma única célula-óvulo, que precisa carregar não só o DNA, mas também as instruções moleculares que guiam o desenvolvimento inicial. Este estudo revela como uma espécie de “equipe de limpeza” molecular dentro dos oócitos de camundongo mantém seu material genético em bom funcionamento, favorecendo embriões saudáveis e a fertilidade feminina. Ao observar como esse sistema funciona quando está intacto e o que dá errado quando falha, os cientistas obtêm pistas que podem, no futuro, ajudar a explicar algumas formas de infertilidade.
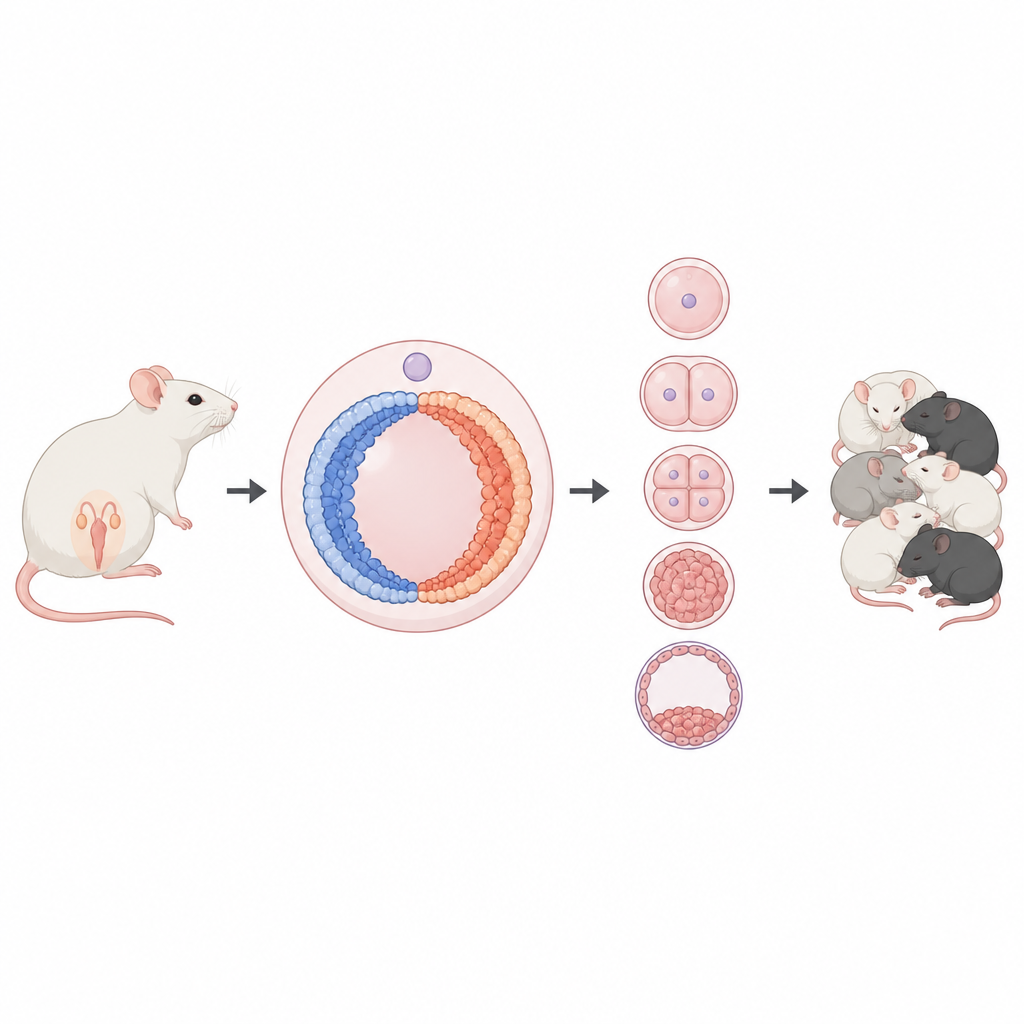
Uma disputa pelo DNA do óvulo
Dentro de cada oócito, o DNA está enrolado em proteínas para formar a cromatina, que pode estar frouxamente empacotada e ativa ou densamente compactada e silenciosa. Duas marcas químicas nessas proteínas ajudam a identificar esses estados: uma está associada à atividade e a outra ao silenciamento. Os autores concentram-se em uma proteína chamada BAP1, parte de um complexo desmarcador que remove uma marca de silenciamento da cromatina. Em muitos tipos celulares esse complexo tem sido associado ao desligamento de genes, mas nos oócitos a equipe suspeitava que ele poderia ter um papel bem diferente.
Protegendo regiões ativas do avanço do silêncio
Usando engenharia genética em camundongos, os pesquisadores removeram seletivamente o BAP1 dos oócitos em crescimento e mapearam onde diferentes marcas de cromatina estavam localizadas. Sem BAP1, uma marca de silenciamento se espalhou amplamente pelo genoma, especialmente em trechos de DNA que normalmente abrigam elementos regulatórios chamados enhancers. Em muitos desses locais, a marca ligada à atividade foi perdida e a marca de silenciamento tomou seu lugar. As regiões afetadas costumavam ficar em zonas pobres em genes que ganham marcas ativas apenas tardiamente no crescimento do óvulo, sugerindo que o BAP1 é particularmente importante para ativar novos programas pouco antes de o óvulo atingir a maturidade completa.
Mantendo genes-chave do óvulo ligados
Em seguida, os autores examinaram quais genes tiveram a atividade alterada quando o BAP1 estava ausente. Muito mais genes foram desativados do que ativados, demonstrando que, nos oócitos, o BAP1 apoia principalmente a atividade gênica em vez do silenciamento. Muitos dos genes reduzidos ajudam células a aderir umas às outras ou a responder a sinais de crescimento, funções conhecidas por serem importantes para a qualidade do óvulo e o desenvolvimento embrionário inicial. Curiosamente, alvos clássicos de outro sistema de silenciamento, chamado Polycomb, permaneceram em grande parte repressos mesmo sem BAP1, o que significa que a tarefa principal desse complexo desmarcador nos oócitos é proteger regiões ativas contra o silenciamento, em vez de reforçar um silêncio já existente.
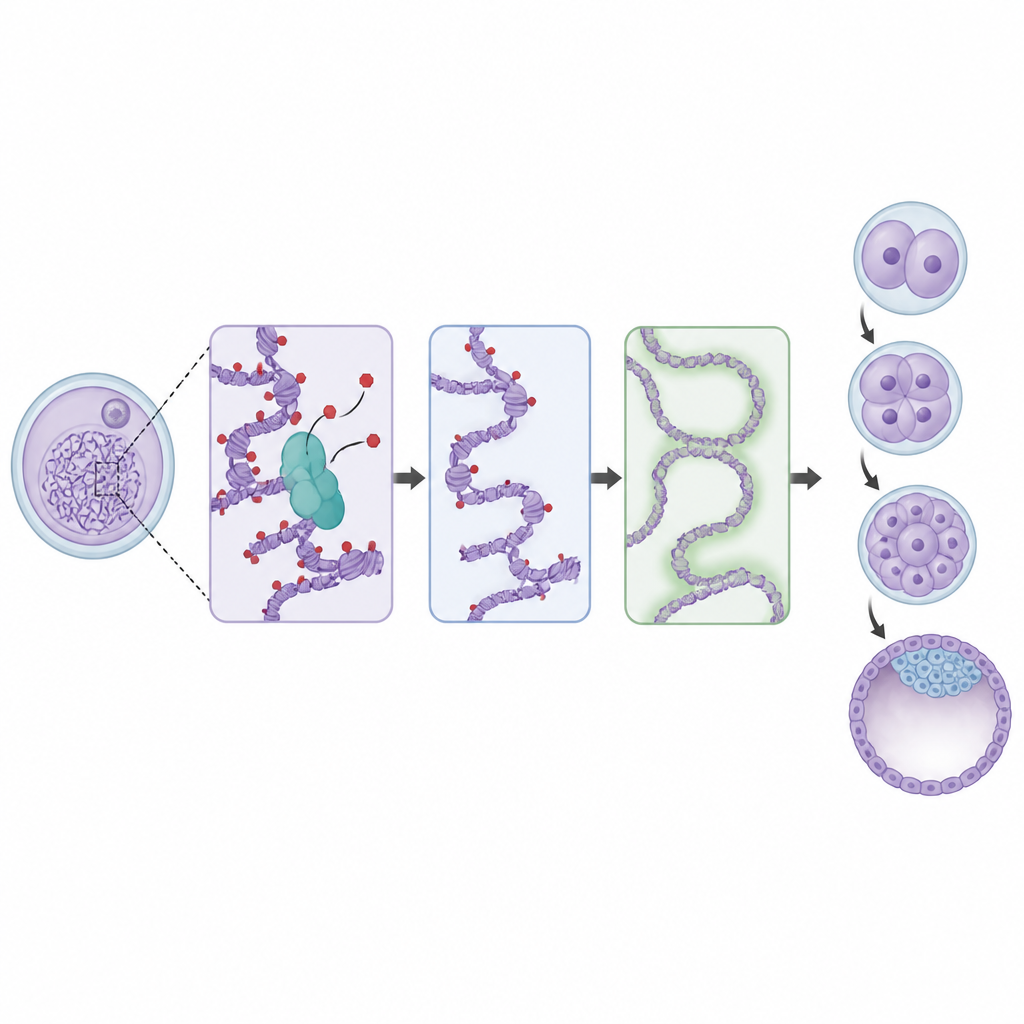
De óvulos defeituosos a embriões em dificuldade
A equipe então acompanhou o que ocorreu após a fertilização. Óvulos sem BAP1 podiam ser fertilizados, mas seus embriões se dividiam mais lentamente e muitos paravam antes de formar blastocistos saudáveis, a fase que implanta no útero. Quando tanto o BAP1 materno quanto o embrionário inicial estavam ausentes, o desenvolvimento frequentemente cessava com apenas algumas células. Medições detalhadas de RNA mostraram que esses embriões tiveram dificuldade na transição materno-para-zigótica, a transferência de mensagens armazenadas no óvulo para a atividade gênica própria do embrião. Muitos genes que deveriam ser ativados precocemente permaneceram fracos, enquanto algumas mensagens maternas perduraram por mais tempo que o normal. Ao mesmo tempo, novos enhancers no embrião não conseguiram adquirir marcas de atividade fortes, embora marcas de silenciamento herdadas em certas regiões persistissem por vários estágios.
Marcas duradouras que desaparecem no momento certo
Ao rastrear marcas químicas na cromatina por estágios posteriores, os pesquisadores descobriram que as marcas anormais de silenciamento estabelecidas em óvulos sem BAP1 perduraram em embriões iniciais e mórulas, mas foram em grande parte removidas após a implantação. Apesar dessas alterações iniciais, o imprinting genômico padrão, que faz com que alguns genes sejam expressos apenas a partir da cópia materna ou paterna, permaneceu em sua maior parte intacto. Isso sugere que o impacto principal da perda de BAP1 não é embaralhar o imprinting, mas enfraquecer a atividade de enhancers e a expressão gênica exatamente quando o embrião mais delas precisa.
O que isso significa para a fertilidade e além
Em termos simples, este trabalho mostra que o BAP1 atua como um guardião do epigenoma do óvulo, removendo marcas de silenciamento em excesso para que regiões-chave do DNA possam permanecer ativas. Quando esse guardião se perde, o silêncio avança para lugares que deveriam permanecer ativos, os óvulos perdem mensagens desenvolvimentais importantes, os embriões iniciais enfraquecem e a fertilidade feminina declina. Embora o estudo tenha sido realizado em camundongos, ele destaca quão delicado é o equilíbrio das marcas de cromatina em óvulos e embriões iniciais, e como pequenas alterações nesse equilíbrio podem ter grandes consequências para a reprodução.
Citação: Kang, J., Liu, P., Ichimura, S. et al. Polycomb repressive-deubiquitinase complex safeguards oocyte epigenome and female fertility by restraining Polycomb activity. Nat Commun 17, 4149 (2026). https://doi.org/10.1038/s41467-026-70845-x
Palavras-chave: epigenoma do oócito, transição materno-para-zigótica, BAP1, desenvolvimento embrionário inicial, fertilidade feminina