Clear Sky Science · es
El complejo represor-desubiquitinasa de Polycomb protege el epigenoma del ovocito y la fertilidad femenina al frenar la actividad de Polycomb
Por qué importan los óvulos sanos para la vida futura
Toda gestación comienza con una sola célula ovocitaria, que debe portar no solo el ADN sino también las instrucciones moleculares que guían el desarrollo temprano. Este estudio revela cómo una especie de “equipo de limpieza” molecular dentro de los ovocitos de ratón mantiene su material genético en buen estado, favoreciendo embriones sanos y la fertilidad femenina. Al observar cómo funciona este sistema cuando está intacto y qué falla cuando deja de hacerlo, los científicos obtienen pistas que podrían ayudar a explicar algunas formas de infertilidad.
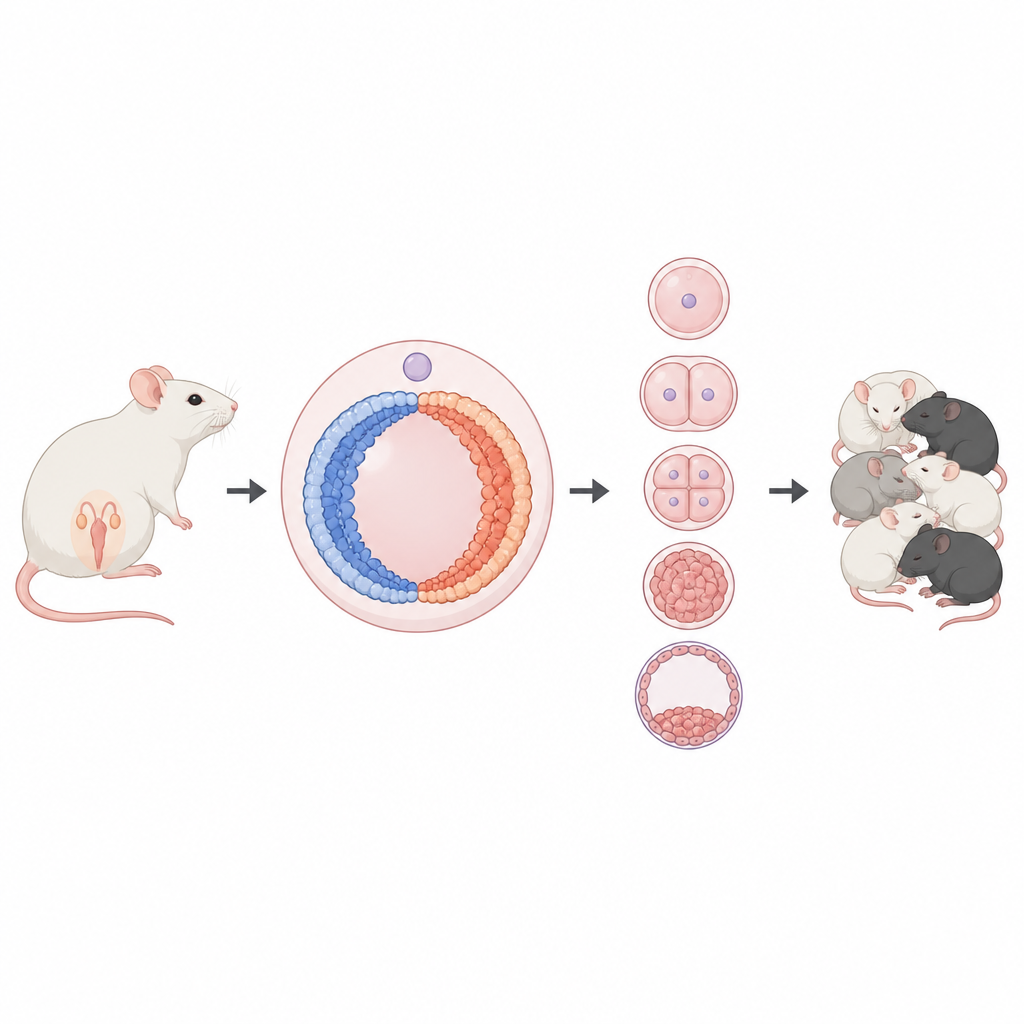
Una lucha de fuerzas sobre el ADN del óvulo
Dentro de cada ovocito, el ADN se enrolla alrededor de proteínas para formar la cromatina, que puede estar suelta y activa o compacta y silenciosa. Dos marcas químicas en estas proteínas ayudan a señalar esos estados: una está asociada a la actividad y la otra al silenciamiento. Los autores se centran en una proteína llamada BAP1, parte de un complejo que elimina una marca de silenciamiento de la cromatina. En muchos tipos celulares este complejo se ha vinculado a apagar genes, pero en los ovocitos el equipo sospechaba que podría desempeñar un papel muy distinto.
Protegiendo regiones activas del avance del silencio
Mediante ingeniería genética en ratones, los investigadores eliminaron selectivamente BAP1 de ovocitos en crecimiento y luego mapearon dónde se ubicaban las distintas marcas de cromatina. Sin BAP1, una marca de silenciamiento se extendió ampliamente por el genoma, especialmente hacia tramos de ADN que normalmente albergan elementos reguladores llamados potenciadores. En muchos de esos sitios, la marca habitual ligada a la actividad se perdió y la marca de silenciamiento ocupó su lugar. Las regiones afectadas a menudo se encontraban en zonas pobres en genes que adquieren marcas activas solo al final del crecimiento ovocitario, lo que sugiere que BAP1 es particularmente importante para activar nuevos programas justo antes de que el ovocito esté plenamente maduro.
Mantener encendidos los genes clave del óvulo
A continuación, los autores examinaron qué genes cambiaron su actividad cuando faltaba BAP1. Muchísimos más genes disminuyeron su expresión que los que aumentaron, lo que muestra que en los ovocitos BAP1 sostiene principalmente la actividad génica más que el silenciamiento. Muchos de los genes reducidos ayudan a las células a adherirse entre sí o a responder a señales de crecimiento, funciones conocidas por ser importantes para la calidad del óvulo y el desarrollo embrionario temprano. Curiosamente, los blancos clásicos de otro sistema de silenciamiento, llamado Polycomb, permanecieron en gran medida reprimidos incluso sin BAP1, lo que indica que la función principal de este complejo des-etiquetador en los ovocitos es proteger regiones activas de ser silenciadas en lugar de reforzar silencios ya existentes.
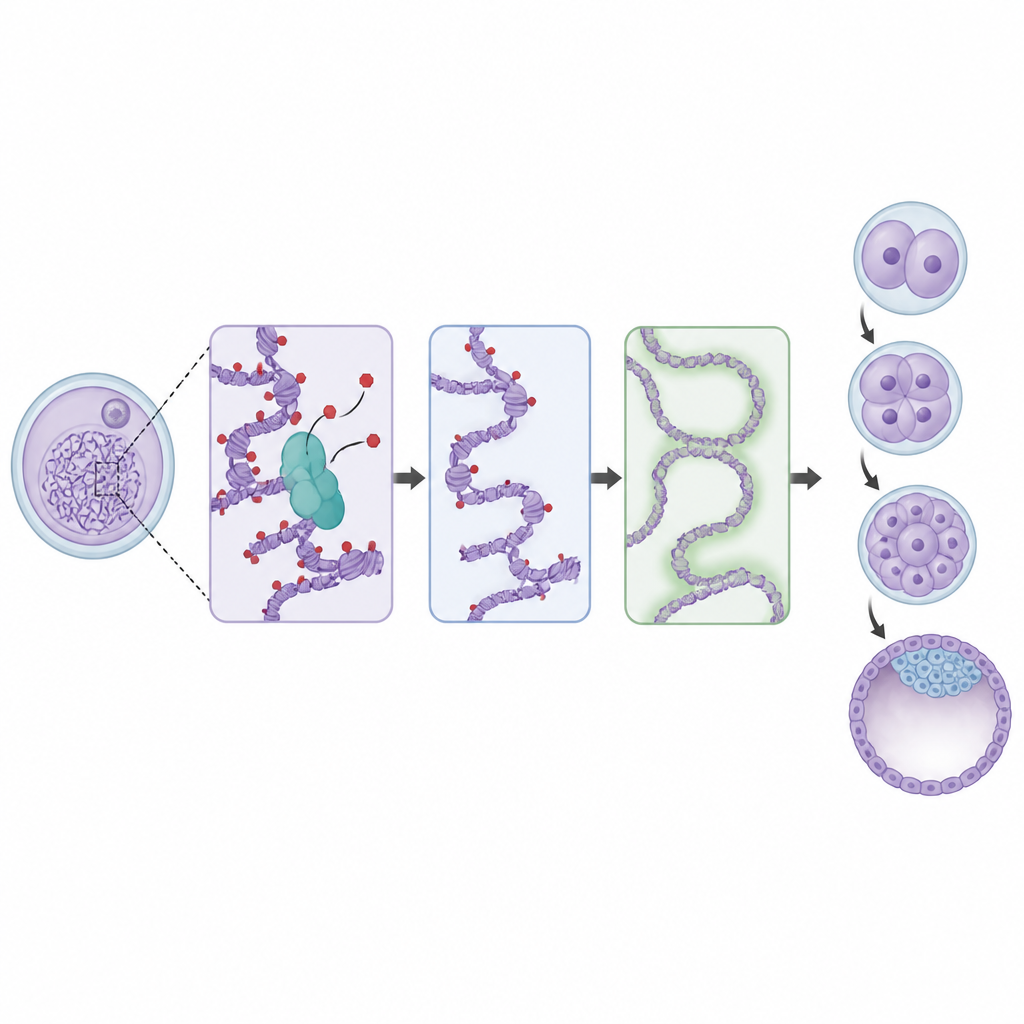
De óvulos defectuosos a embriones en apuros
El equipo siguió luego lo que ocurría tras la fecundación. Los ovocitos sin BAP1 podían ser fecundados, pero sus embriones se dividían más despacio y muchos se detenían antes de formar blastocistos saludables, la fase que se implanta en el útero. Cuando faltaba tanto BAP1 materno como el temprano del embrión, el desarrollo a menudo se interrumpía con apenas unas pocas células. Mediciones detalladas de ARN mostraron que estos embriones tenían dificultades con la transición materno-a-cigótica, la transferencia de mensajes almacenados en el óvulo a la actividad génica propia del embrión. Muchos genes que deberían activarse temprano permanecieron débiles, mientras que algunos mensajeros maternos persistieron más tiempo de lo normal. Al mismo tiempo, los nuevos potenciadores en el embrión no lograron adquirir marcas de actividad fuertes, aunque marcas heredadas de silenciamiento en ciertas regiones persistieron a lo largo de varias etapas.
Marcas duraderas que desaparecen en el momento adecuado
Al seguir las marcas químicas en la cromatina en etapas posteriores, los investigadores hallaron que las marcas anómalas de silenciamiento establecidas en ovocitos sin BAP1 perduraron en embriones tempranos y mórulas pero se eliminaron en gran medida después de la implantación. A pesar de estos cambios tempranos, el imprinting genómico estándar, que hace que algunos genes se expresen solo desde la copia materna o paterna, se mantuvo en su mayoría intacto. Esto sugiere que el impacto principal de perder BAP1 no es desordenar el imprinting, sino debilitar la actividad de potenciadores y la expresión génica justamente cuando el embrión más las necesita.
Qué implica esto para la fertilidad y más allá
En resumen, este trabajo muestra que BAP1 actúa como guardián del epigenoma del ovocito, eliminando marcas de silenciamiento excesivas para que regiones clave del ADN puedan permanecer activas. Cuando se pierde este guardián, el silencio avanza hacia lugares que deberían permanecer encendidos, los ovocitos pierden mensajes de desarrollo importantes, los embriones tempranos flaquean y la fertilidad femenina disminuye. Aunque el estudio se realizó en ratones, pone de relieve lo delicado que es el equilibrio de las marcas de cromatina en los ovocitos y embriones tempranos, y cómo pequeños cambios en ese equilibrio pueden tener grandes consecuencias para la reproducción.
Cita: Kang, J., Liu, P., Ichimura, S. et al. Polycomb repressive-deubiquitinase complex safeguards oocyte epigenome and female fertility by restraining Polycomb activity. Nat Commun 17, 4149 (2026). https://doi.org/10.1038/s41467-026-70845-x
Palabras clave: epigenoma del ovocito, transición materno-a-cigótica, BAP1, desarrollo embrionario temprano, fertilidad femenina