Clear Sky Science · de
Das Polycomb-repressive-Deubiquitinase-Komplex schützt das Epigenom der Eizelle und die weibliche Fruchtbarkeit, indem es Polycomb-Aktivität einschränkt
Warum gesunde Eizellen für das zukünftige Leben wichtig sind
Jede Schwangerschaft beginnt mit einer einzelnen Eizelle, die nicht nur DNA, sondern auch die molekularen Anweisungen tragen muss, die die frühe Entwicklung steuern. Diese Studie beschreibt, wie eine molekulare „Aufräumtruppe“ in Maus-Eizellen das genetische Material in funktionsfähigem Zustand hält und so gesunde Embryonen und die weibliche Fruchtbarkeit unterstützt. Indem untersucht wird, wie dieses System im intakten Zustand arbeitet und was schiefgeht, wenn es versagt, gewinnen Wissenschaftler Hinweise, die schließlich helfen könnten, manche Formen von Unfruchtbarkeit zu erklären.
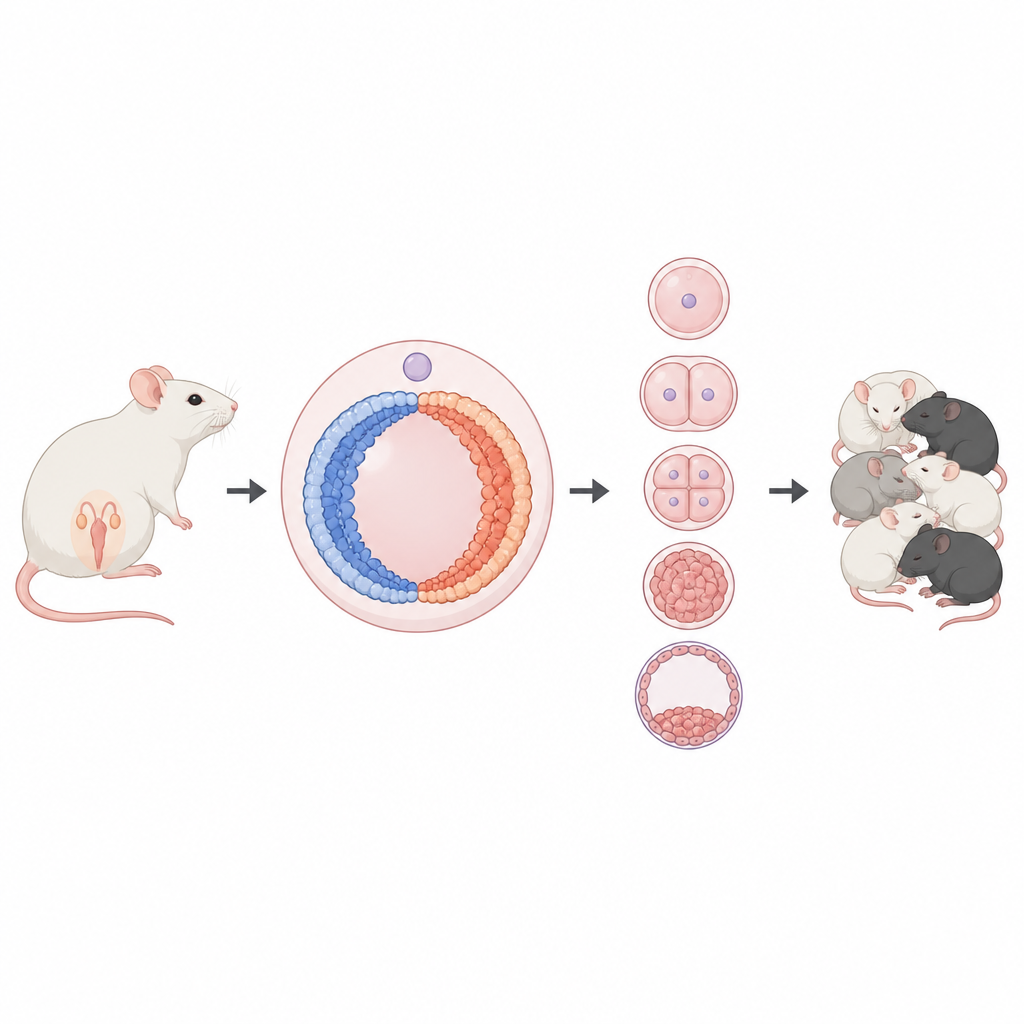
Ein Tauziehen um die DNA der Eizelle
Innerhalb jeder Eizelle ist DNA um Proteine gewickelt und bildet Chromatin, das locker gepackt und aktiv oder dicht gepackt und still sein kann. Zwei chemische Markierungen auf diesen Proteinen kennzeichnen diese Zustände: eine ist mit Aktivität verknüpft, die andere mit Stilllegung. Die Autoren konzentrieren sich auf ein Protein namens BAP1, das Teil eines De-Tagging-Komplexes ist, der eine Silenzierungsmarke vom Chromatin entfernt. In vielen Zelltypen wurde dieser Komplex mit dem Abschalten von Genen in Verbindung gebracht, aber in Eizellen vermutete das Team, dass er eine ganz andere Rolle spielen könnte.
Aktive Regionen vor schleichender Stille schützen
Mit genetischer Manipulation bei Mäusen entfernten die Forscher BAP1 selektiv aus wachsenden Eizellen und kartierten dann, wo sich verschiedene Chromatin-Markierungen befanden. Ohne BAP1 breitete sich eine Silenzierungsmarke über das Genom aus, besonders in Bereiche, die normalerweise Kontroll-Elemente namens Enhancer beherbergen. An vielen dieser Stellen ging die übliche aktivitätsgebundene Markierung verloren und die Silenzierungsmarke nahm ihren Platz ein. Die betroffenen Regionen lagen häufig in genarmen Zonen, die erst spät im Eizellwachstum aktive Markierungen gewinnen, was darauf hindeutet, dass BAP1 besonders wichtig ist, um kurz vor der vollständigen Reife der Eizelle neue Programme einzuschalten.
Wichtige Eizell-Gene eingeschaltet halten
Als Nächstes untersuchten die Autoren, welche Gene ihre Aktivität änderten, wenn BAP1 fehlte. Weit mehr Gene wurden herunterreguliert als hochreguliert, was zeigt, dass BAP1 in Eizellen hauptsächlich die Genaktivität unterstützt statt Stille zu fördern. Viele der verminderten Gene helfen Zellen, aneinander zu haften oder auf Wachstumssignale zu reagieren — Funktionen, die für Eizellqualität und frühe Embryonalentwicklung wichtig sind. Interessanterweise blieben klassische Ziele eines anderen Silenzierungssystems, genannt Polycomb, weitgehend reprimiert, selbst ohne BAP1, was bedeutet, dass die Hauptaufgabe dieses De-Tagging-Komplexes in Eizellen darin besteht, aktive Bereiche vor Stilllegung zu bewahren, statt bestehende Stille zu verstärken.
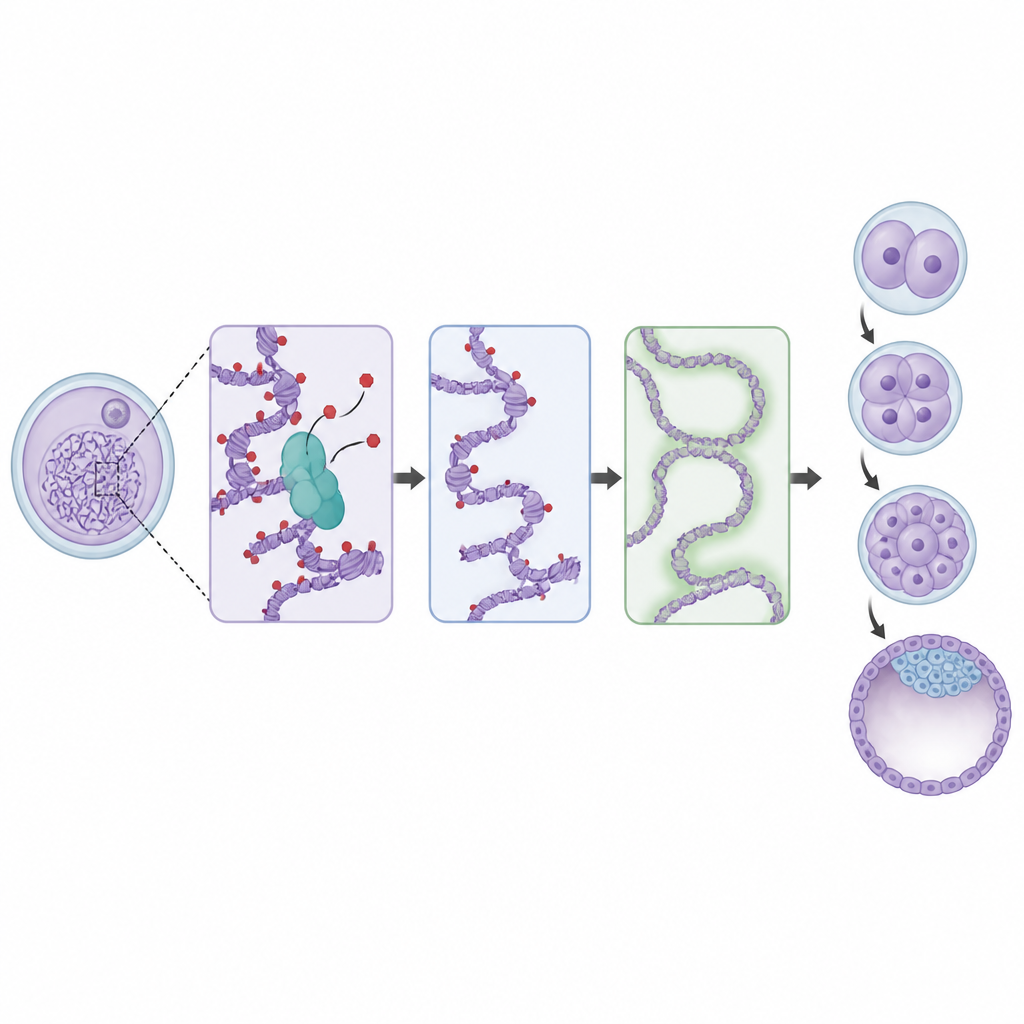
Von fehlerhaften Eizellen zu geschwächten Embryonen
Das Team verfolgte anschließend die Folgen nach der Befruchtung. Eizellen ohne BAP1 konnten zwar befruchtet werden, doch ihre Embryonen teilten sich langsamer und viele blieben stehen, bevor sie gesunde Blastozysten bildeten — die Stufe, die in die Gebärmutter implantiert. Wenn sowohl mütterliches als auch frühembryonales BAP1 fehlten, blieb die Entwicklung oft schon nach wenigen Zellteilungen stehen. Detaillierte RNA-Messungen zeigten, dass diese Embryonen Schwierigkeiten mit dem mütterlich-zu-zygotischen Übergang hatten, dem Wechsel von gespeicherten Eizell-Botschaften zur eigenen Genaktivität des Embryos. Viele Gene, die früh angeschaltet werden sollten, blieben schwach, während einige mütterliche Botschaften länger anhielten als normal. Gleichzeitig konnten neue Enhancer im Embryo keine starken Aktivitätsmarken aufbauen, obwohl vererbte Silenzierungsmarken in bestimmten Regionen über mehrere Stadien hinweg persistierten.
Beständige Markierungen, die zur richtigen Zeit verschwinden
Durch die Verfolgung chemischer Markierungen auf Chromatin in späteren Stadien fanden die Forscher heraus, dass die abnormalen Silenzierungsmarken, die in BAP1-freien Eizellen etabliert wurden, in frühe Embryonen und Morulae hineinreichten, aber nach der Implantation weitgehend entfernt wurden. Trotz dieser frühen Verschiebungen blieb das normale genomische Imprinting, das bewirkt, dass einige Gene nur von der Mutter- oder Vaterseite exprimiert werden, größtenteils intakt. Das deutet darauf hin, dass der Hauptauswirkung des Verlustes von BAP1 nicht in einer Verwürfelung des Imprintings liegt, sondern darin, die Enhancer-Aktivität und Genexpression genau in der Phase zu schwächen, in der der Embryo sie am dringendsten braucht.
Was das für Fruchtbarkeit und darüber hinaus bedeutet
Kurz gesagt zeigt diese Arbeit, dass BAP1 als Wächter des Epigenoms der Eizelle fungiert, indem es überschüssige Silenzierungsmarken entfernt, damit wichtige DNA-Regionen aktiv bleiben können. Geht dieser Wächter verloren, schleicht sich Stilllegung an Stellen ein, die aktiv bleiben sollten, Eizellen verlieren wichtige Entwicklungsbotschaften, frühe Embryonen geraten ins Stocken und die weibliche Fruchtbarkeit nimmt ab. Obwohl die Studie an Mäusen durchgeführt wurde, verdeutlicht sie, wie empfindlich das Gleichgewicht der Chromatin-Markierungen in Eizellen und frühen Embryonen ist und wie kleine Verschiebungen in diesem Gleichgewicht große Folgen für die Fortpflanzung haben können.
Zitation: Kang, J., Liu, P., Ichimura, S. et al. Polycomb repressive-deubiquitinase complex safeguards oocyte epigenome and female fertility by restraining Polycomb activity. Nat Commun 17, 4149 (2026). https://doi.org/10.1038/s41467-026-70845-x
Schlüsselwörter: Eizell-Epigenom, mütterlich-zu-zygotisch-Übergang, BAP1, frühe Embryonalentwicklung, weibliche Fruchtbarkeit