Clear Sky Science · pt
Um modelo mecanístico multihospedeiro da emergência e controle da peste suína africana na Romênia
Por que isso importa para produtores e segurança alimentar
A peste suína africana é uma doença letal em suínos que dizimou milhões de animais pelo mundo, ameaçando a subsistência de agricultores e elevando os preços da carne suína. A Romênia foi um dos países mais afetados na Europa, com surtos atingindo tanto porcos domésticos em quintais de vilarejos quanto javalis nas florestas próximas. Este estudo usa um modelo de computador detalhado para desvendar como o vírus se moveu entre fazendas e a vida selvagem durante a primeira grande onda da epidemia em 2018 — e testa quais medidas de controle poderiam, de fato, ajudar a conter um surto desse tipo.
Dois mundos conectados: porcos de quintal e javalis
O interior da Romênia é pontilhado de vilarejos onde muitas famílias criam alguns porcos em currais simples. Florestas e campos próximos abrigam javalis. Quando a peste suína africana entrou no sudeste da Romênia em 2018, casos surgiram rapidamente em ambos os ambientes. Os pesquisadores trataram cada vila como uma única grande “fazenda” e dividiram a paisagem em parcelas hexagonais que podiam abrigar javalis. Em seguida, usaram relatórios oficiais de fazendas infectadas e carcaças de javalis de junho a dezembro de 2018 para reconstruir como a doença provavelmente saltou de lugar a lugar e entre os dois tipos de hospedeiros.
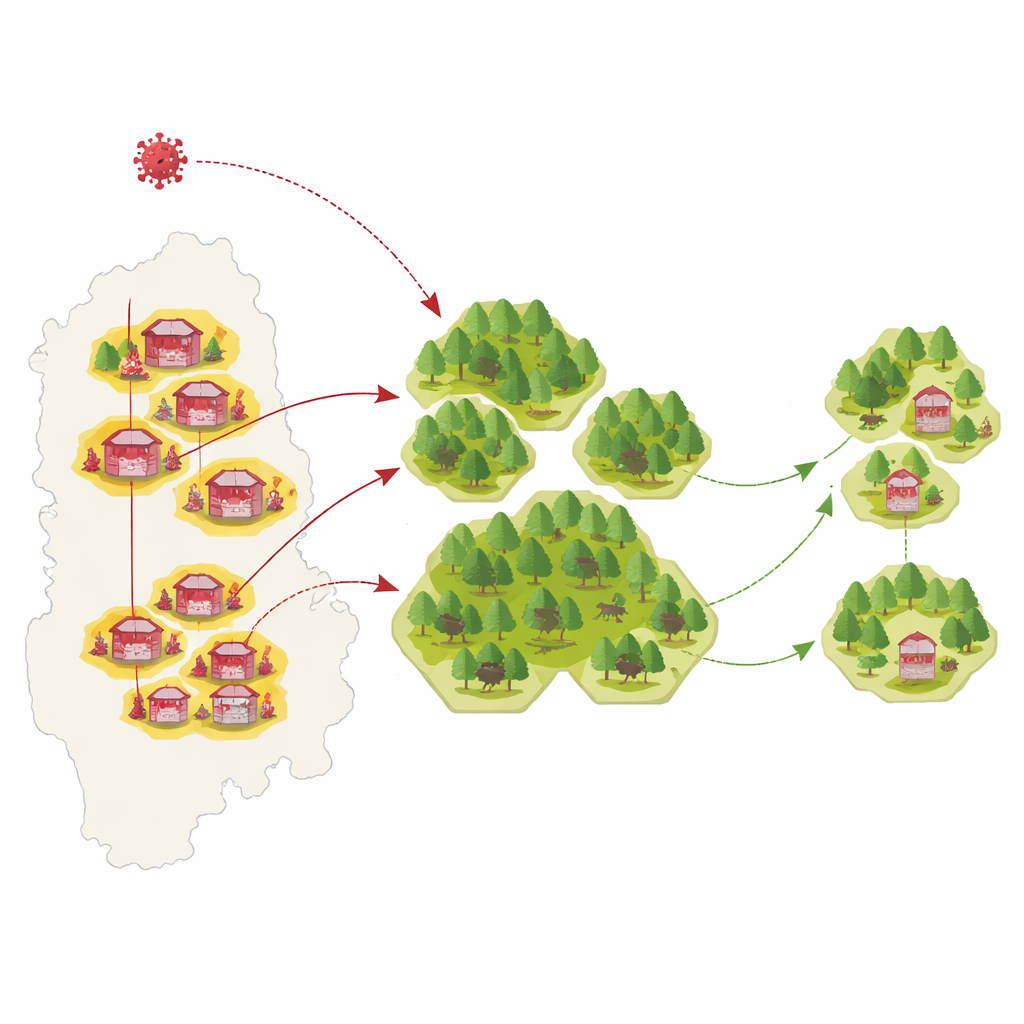
Construindo uma epidemia digital no mapa
A equipe criou um modelo “mecanístico”, isto é, que segue regras simples sobre como a infecção se espalha: quais fazendas ou parcelas de javalis podem entrar em contato, quão rapidamente locais infectados são detectados e por quanto tempo permanecem infecciosos. Testaram 256 versões diferentes do modelo, variando suposições como se as fazendas infectam principalmente os vizinhos mais próximos ou espalham a doença mais amplamente, e se são necessárias introduções de longa distância nos javalis além da propagação local. Mantiveram então apenas as versões que melhor reproduziam as curvas epidêmicas reais — quantas novas fazendas infectadas e parcelas de javalis apareciam a cada semana em cada um dos seis condados.
Quem infectou quem?
Uma vez encontrado o modelo de melhor ajuste, os pesquisadores o usaram para estimar a fonte mais provável de cada nova infecção. Para fazendas de porcos domésticos, calcularam que cerca de três em cada cinco fazendas infectadas estavam ligadas a outras fazendas com surto, um pouco mais de uma em quatro estavam ligadas a áreas de javalis infectadas, e o restante se devia a infecções vindas de fora do sistema modelado, como movimentos de longa distância. Para as parcelas de javalis, a maioria das infecções veio de outras áreas de javalis infectadas, mas uma parcela substancial veio de fazendas. Parcelas florestadas com cobertura arbórea suficiente atuaram como pontos quentes: essas áreas tinham probabilidade muito maior tanto de se infectarem quanto de transmitir a infecção do que terrenos mais abertos. Juntos, esses padrões mostram que as duas populações hospedeiras formaram uma rede fortemente conectada em vez de epidemias separadas.

Testando estratégias de controle hipotéticas
A Romênia já aplicou regras de controle padrão durante a onda de 2018, incluindo abate de porcos em fazendas detectadas e a criação de zonas de vigilância de 10 quilômetros. O modelo permitiu aos autores explorar vários cenários “e se”: remover carcaças de javalis mais rapidamente, melhorar a vigilância passiva em fazendas para que as infecções sejam detectadas mais cedo, e estratégias de abate mais agressivas que removem fazendas inteiras imediatamente ou abatem preventivamente fazendas vizinhas quando casos de javalis são detectados nas proximidades. Embora essas intervenções tivessem tendência a reduzir o tamanho mediano da epidemia nas simulações, os benefícios foram modestos e altamente incertos, e nenhuma delas apresentou forte suporte estatístico para superar claramente a resposta padrão. Realidades sociais, como resistência ao abate preventivo em larga escala de porcos de quintal, limitam ainda mais o que pode ser feito na prática.
Limites do modelo e dos dados
O estudo também ressalta as dificuldades de modelar uma doença do gado no mundo real. A vigilância de javalis foi desigual e provavelmente deixou de registrar muitos casos, especialmente em áreas remotas. Dentro das vilas, havia informação limitada sobre quantas famílias criavam porcos ou como interagiam, de modo que cada vila teve de ser tratada como uma única unidade. No início da epidemia, os esforços de detecção podem ter aumentado rapidamente, mas o modelo assumiu um nível constante de vigilância. Essas lacunas significam que, embora os padrões gerais sejam robustos — particularmente a importância da transmissão entre espécies — as porcentagens precisas apresentam amplas faixas de incerteza.
O que isso significa para surtos futuros
Para não especialistas, a conclusão-chave é que controlar a peste suína africana em locais como a Romênia não pode se focar apenas nas fazendas ou apenas na vida selvagem. Porcos de quintal e javalis se reinfectam continuamente, especialmente em e ao redor de áreas florestadas. O modelo sugere que mesmo versões relativamente fortes das estratégias atuais provavelmente não erradicariam o vírus, a menos que façam parte de uma reavaliação mais ampla que inclua ambos os hospedeiros, melhor vigilância da vida selvagem e atenção realista à cultura e à economia locais. Em vez de prometer erradicação rápida, as autoridades podem precisar planejar o manejo de longo prazo de uma circulação de baixo nível em javalis, enquanto usam maior biossegurança e monitoramento para evitar que a doença reverta para rebanhos domésticos.
Citação: Hayes, B., Vergne, T., Rose, N. et al. A multi-host mechanistic model of African swine fever emergence and control in Romania. Nat Commun 17, 2659 (2026). https://doi.org/10.1038/s41467-026-70769-6
Palavras-chave: Peste suína africana, Criações de porcos na Romênia, Transmissão por javalis, Modelagem de doenças, Controle de doenças do gado