Clear Sky Science · pt
Mecanismos de regulação gênica pelo SRCAP e H2A.Z
Como as células-tronco mantêm suas opções futuras em aberto
Nossos corpos dependem de células-tronco capazes tanto de se renovar quanto de, mais adiante, se especializar em muitos tipos de tecido. Esse equilíbrio delicado é controlado por como o DNA é enrolado e desenrolado dentro do núcleo celular. Este estudo revela como uma máquina molecular de “remodelamento” chamada SRCAP e uma proteína especial de empacotamento do DNA, H2A.Z, trabalham juntas para manter as células-tronco em estado de prontidão entre permanecer iguais e tornar-se algo novo.
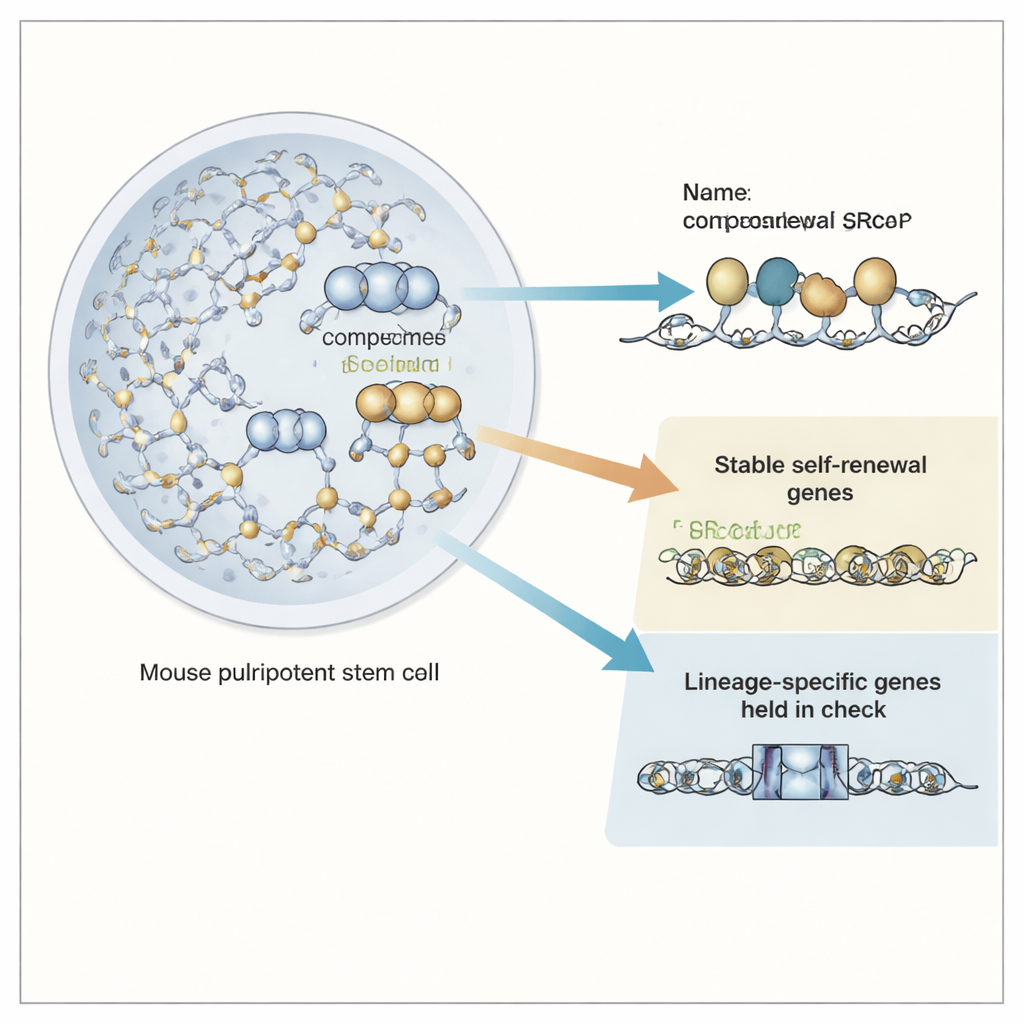
Os carretéis de DNA que controlam a atividade gênica
Dentro de cada célula, o DNA é enrolado em torno de carretéis proteicos chamados nucleossomos, formando a cromatina. A maioria dos nucleossomos usa proteínas padrão, mas alguns carregam uma variante chamada H2A.Z, que é especialmente comum perto de interruptores gênicos, como promotores e enhancers. Em células-tronco pluripotentes de camundongo, sabe-se que H2A.Z é importante tanto para a autorrenovação quanto para a capacidade de diferenciar. O complexo SRCAP é uma grande máquina que troca componentes padrão dos nucleossomos por H2A.Z, mas até agora não estava claro se seus efeitos sobre genes vinham apenas da colocação de H2A.Z ou se o próprio SRCAP tinha papéis adicionais e mais diretos.
Uma troca rápida entre carretéis padrão e variantes
Para ver o que o SRCAP faz em tempo real, os pesquisadores projetaram células-tronco de modo que o SRCAP pudesse ser destruído em poucas horas pela adição de uma pequena molécula. Quando o SRCAP foi removido, H2A.Z desapareceu rapidamente de quase todos os seus locais habituais e foi substituído pela histona padrão, especialmente ao redor de inícios de genes ativos e enhancers. Essa troca rápida ocorreu ao longo do ciclo celular e foi ainda mais rápida durante a divisão celular, sugerindo que o SRCAP está constantemente recarregando H2A.Z à medida que outros processos o deslocam. Curiosamente, o empacotamento geral dos nucleossomos e suas propriedades físicas básicas mudaram bem menos do que o esperado, indicando que os efeitos-chave do SRCAP e de H2A.Z não são simplesmente afrouxar ou apertar o DNA, mas influenciar quem pode se ligar ali.
Contendo reguladores mestres do destino celular
Quando o SRCAP foi degradado, a atividade de centenas de genes mudou em poucas horas. Muitos genes que normalmente estão em um estado “pronto” — frequentemente reguladores importantes de futuros destinos celulares — tornaram-se mais ativos, enquanto muitos genes de manutenção amplamente necessários ficaram menos ativos. Mapear detalhadamente os contatos proteína–DNA mostrou que um grande número de fatores de transcrição, especialmente os chamados fatores pioneiros que podem se ligar à cromatina fechada, de repente ganhou acesso a seus sítios-alvo quando o SRCAP desapareceu. Ainda assim, os níveis desses fatores na célula não mudaram, apontando para o SRCAP como uma barreira física que normalmente os mantém afastados de certos trechos de DNA.
Separando os papéis do SRCAP e de H2A.Z
Para desvincular as funções do SRCAP e de H2A.Z, a equipe construiu uma versão mutante do SRCAP que ainda pode se posicionar nos nucleossomos, mas não consegue mais instalar H2A.Z. Comparando células que expressavam a versão normal ou mutante, com e sem a degradação do SRCAP original, revelou-se duas camadas distintas de controle. A própria H2A.Z atuou principalmente como um freio, ajudando a manter muitos genes específicos de linhagem reprimidos. O SRCAP, em contraste, desempenhou um papel positivo no suporte a muitos genes de manutenção e um papel separado, independente de H2A.Z, em bloquear a ligação de fatores de transcrição em numerosos enhancers. Rastreamento de moléculas únicas de um regulador-chave das células-tronco, NANOG, confirmou que quando o SRCAP é removido, moléculas de NANOG encontram e se ligam aos seus alvos com muito mais frequência, consistente com o SRCAP literalmente atrapalhando seu acesso.
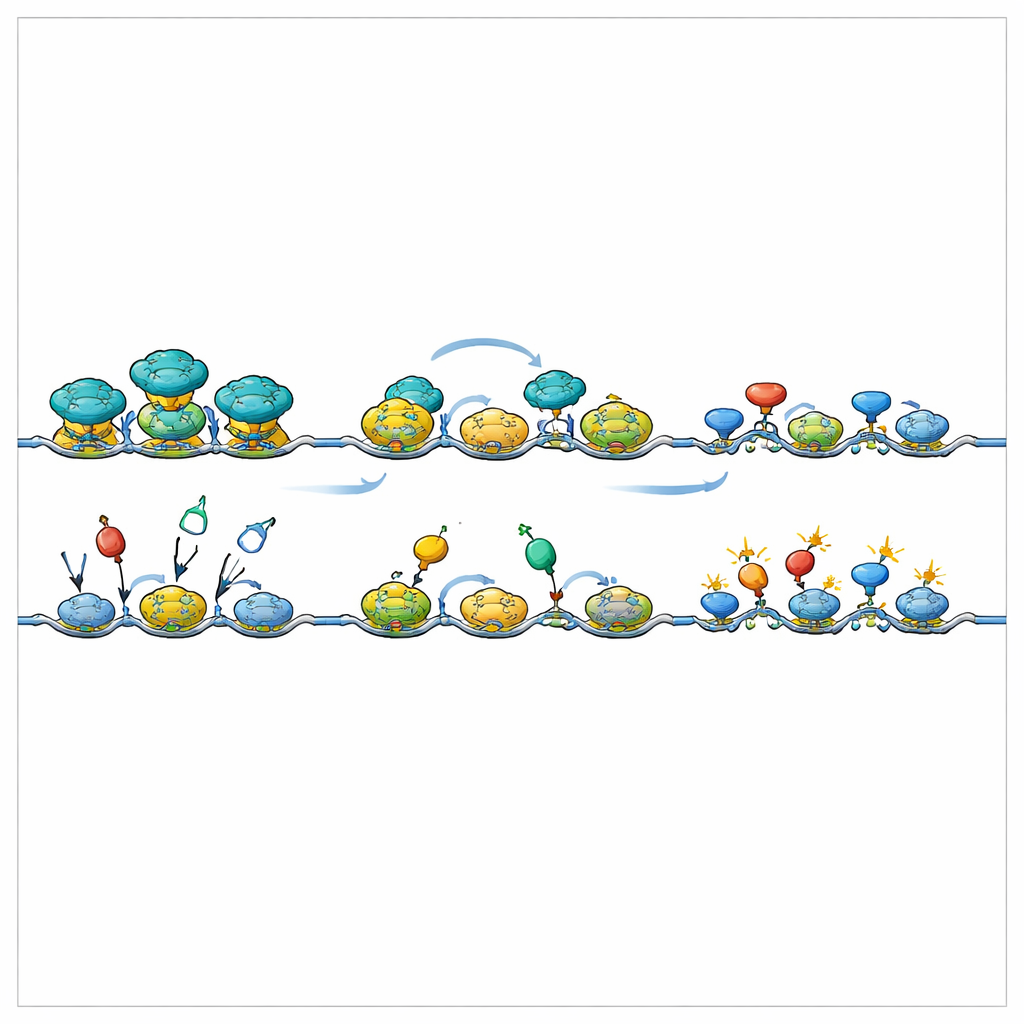
Como um escudo molecular protege a identidade das células-tronco
Em conjunto, essas descobertas mostram o SRCAP como mais do que apenas o instalador de uma peça especial da cromatina. O SRCAP atua como um escudo dinâmico ao longo do DNA, limitando fisicamente quando e onde poderosos fatores de transcrição podem pousar, enquanto H2A.Z ajuda a manter genes de diferenciação sob controle. Ao coordenar esses papéis distintos, o par SRCAP–H2A.Z permite que células-tronco pluripotentes mantenham robustamente sua identidade central e permaneçam prontas para ativar novos programas gênicos quando os sinais adequados chegarem.
Citação: Tollenaere, A., Ugur, E., Dalla Longa, S. et al. Mechanisms of gene regulation by SRCAP and H2A.Z. Nat Commun 17, 3560 (2026). https://doi.org/10.1038/s41467-026-70087-x
Palavras-chave: remodelamento da cromatina, identidade de células-tronco, variante de histona H2A.Z, fatores de transcrição, regulação gênica