Clear Sky Science · it
Meccanismi di regolazione genica mediati da SRCAP e H2A.Z
Come le cellule staminali mantengono aperte le loro possibilità future
I nostri corpi dipendono da cellule staminali in grado sia di rinnovarsi sia, in seguito, di specializzarsi in molti tipi tissutali. Questo delicato equilibrio è controllato da come il DNA è avvolto e svolto all’interno del nucleo cellulare. Questo studio rivela come una macchina molecolare di “rimodellamento” chiamata SRCAP e una proteina speciale per l’impacchettamento del DNA, H2A.Z, lavorino insieme per mantenere le cellule staminali in uno stato di potenziale, tra il rimanere uguali e il diventare qualcosa di nuovo.
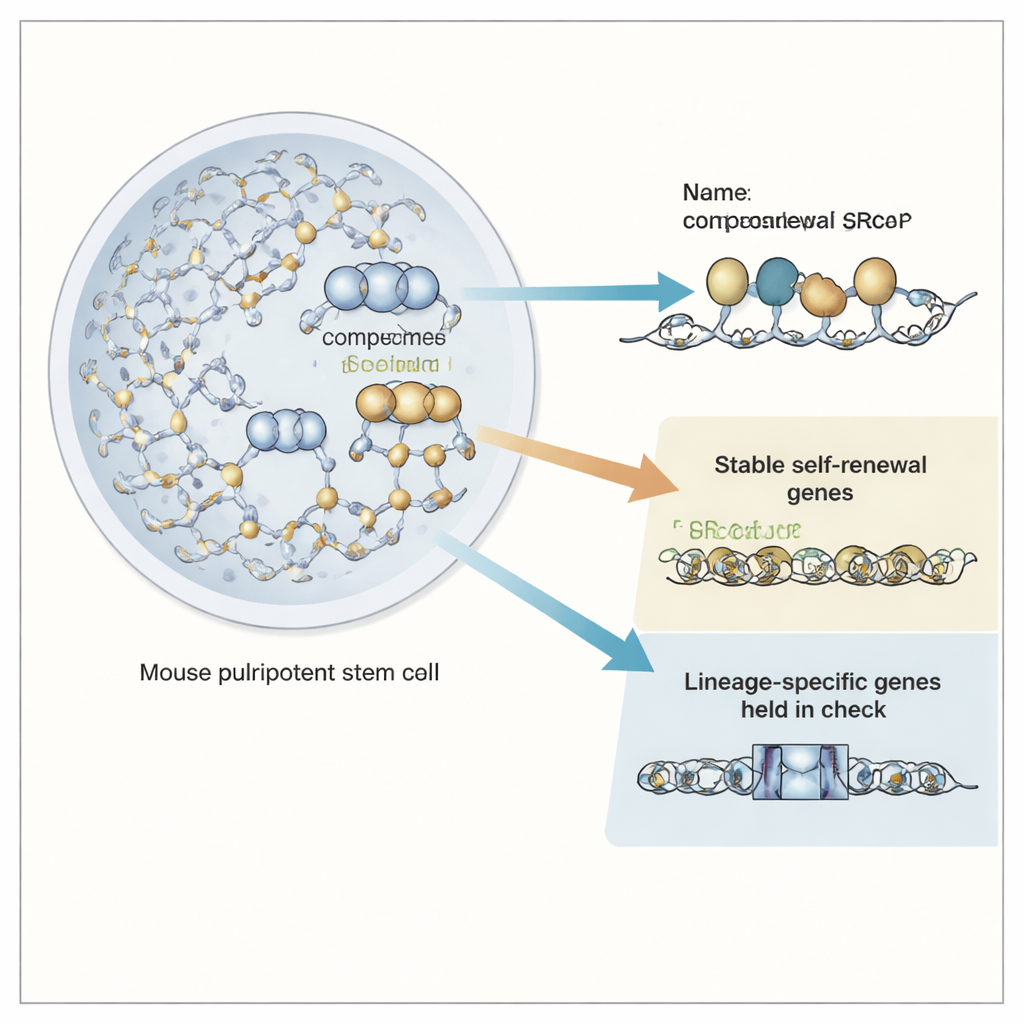
I fusi di DNA che controllano l’attività genica
All’interno di ogni cellula, il DNA è avvolto attorno a fusi proteici chiamati nucleosomi, formando la cromatina. La maggior parte dei nucleosomi utilizza proteine standard, ma alcuni contengono una variante chiamata H2A.Z che è particolarmente comune vicino agli interruttori genici come promotori ed enhancer. Nelle cellule staminali pluripotenti di topo, si sa che H2A.Z è importante sia per l’auto‑rinnovamento sia per la capacità di differenziarsi. Il complesso SRCAP è una grande macchina che sostituisce componenti standard nei nucleosomi con H2A.Z, ma finora non era chiaro se i suoi effetti sui geni derivassero solo dall’inserimento di H2A.Z o se SRCAP avesse anche ruoli addizionali e più diretti.
Un rapido scambio tra fusi standard e varianti
Per osservare cosa fa SRCAP in tempo reale, i ricercatori hanno ingegnerizzato cellule staminali in modo che SRCAP potesse essere distrutto nell’arco di poche ore aggiungendo una piccola molecola. Quando SRCAP è stato rimosso, H2A.Z è scomparso rapidamente da quasi tutti i suoi consueti siti ed è stato rimpiazzato dall’istone standard, specialmente attorno agli inizi dei geni attivi e agli enhancer. Questo rapido ricambio è avvenuto durante tutto il ciclo cellulare ed è stato ancora più veloce durante la divisione cellulare, suggerendo che SRCAP ricarica costantemente H2A.Z mentre altri processi lo rimuovono. È interessante che il livello complessivo di impacchettamento dei nucleosomi e le loro proprietà fisiche di base siano cambiate molto meno di quanto ci si aspettasse, indicando che gli effetti chiave di SRCAP e H2A.Z non sono semplicemente allentare o stringere il DNA, ma influenzare chi può legarsi a quei siti.
Trattenere i regolatori principali del destino cellulare
Quando SRCAP è stato degradato, l’attività di centinaia di geni è cambiata nel giro di poche ore. Molti geni che normalmente si trovano in uno stato “pronto”—spesso regolatori importanti dei futuri destini cellulari—sono diventati più attivi, mentre molti geni di manutenzione generale sono risultati meno espressi. Mappature dettagliate dei contatti proteina–DNA hanno mostrato che un gran numero di fattori di trascrizione, in particolare i cosiddetti fattori pioniere che possono legarsi alla cromatina chiusa, hanno improvvisamente guadagnato accesso ai loro siti target quando SRCAP è scomparso. Tuttavia, i livelli di questi fattori nella cellula non sono cambiati, indicando SRCAP come una barriera fisica che normalmente li tiene lontani da certe porzioni di DNA.
Separare i ruoli di SRCAP e H2A.Z
Per distinguere le funzioni di SRCAP e H2A.Z, il gruppo ha costruito una versione mutante di SRCAP che può ancora posizionarsi sui nucleosomi ma non può più inserire H2A.Z. Il confronto tra cellule che esprimono la versione normale o quella mutante, con e senza degradazione della SRCAP originale, ha rivelato due livelli distinti di controllo. H2A.Z agiva prevalentemente come un freno, contribuendo a mantenere repressi molti geni specifici di linea. SRCAP, al contrario, svolgeva un ruolo positivo nel sostenere molti geni di tipo housekeeping e un ruolo separato, indipendente da H2A.Z, nel bloccare il legame dei fattori di trascrizione in numerosi enhancer. Il tracciamento a singola molecola di un regolatore chiave delle cellule staminali, NANOG, ha confermato che quando SRCAP viene rimosso, le molecole di NANOG trovano e si legano ai loro target con molto maggiore frequenza, coerente con l’idea che SRCAP ostacoli letteralmente il loro accesso.
Come uno scudo molecolare protegge l’identità delle cellule staminali
Nel loro insieme, questi risultati dipingono SRCAP come qualcosa di più del semplice installatore di una parte speciale della cromatina. SRCAP agisce come uno scudo dinamico lungo il DNA, limitando fisicamente quando e dove potenti fattori di trascrizione possono atterrare, mentre H2A.Z aiuta a mantenere sotto controllo i geni della differenziazione. Coordinando questi ruoli distinti, la coppia SRCAP–H2A.Z permette alle cellule staminali pluripotenti di mantenere in modo robusto la loro identità di base pur restando pronte ad attivare nuovi programmi genici quando arrivano i segnali appropriati.
Citazione: Tollenaere, A., Ugur, E., Dalla Longa, S. et al. Mechanisms of gene regulation by SRCAP and H2A.Z. Nat Commun 17, 3560 (2026). https://doi.org/10.1038/s41467-026-70087-x
Parole chiave: rimodellamento della cromatina, identità delle cellule staminali, varianti degli istoni H2A.Z, fattori di trascrizione, regolazione genica