Clear Sky Science · pl
Mechanizmy regulacji genów przez SRCAP i H2A.Z
Jak komórki macierzyste utrzymują otwarte opcje na przyszłość
Nasze ciało polega na komórkach macierzystych, które potrafią zarówno odnawiać się, jak i później specjalizować w różne typy tkanek. Ta delikatna równowaga jest kontrolowana przez to, jak DNA jest nawinięte i rozwijane w jądrze komórkowym. Badanie to ujawnia, jak molekularna „maszyneria remontowa” nazwana SRCAP oraz specjalne białko pakujące DNA, H2A.Z, współdziałają, aby utrzymywać komórki macierzyste w stanie gotowości między zachowaniem tożsamości a przemianą w komórkę o innej funkcji.
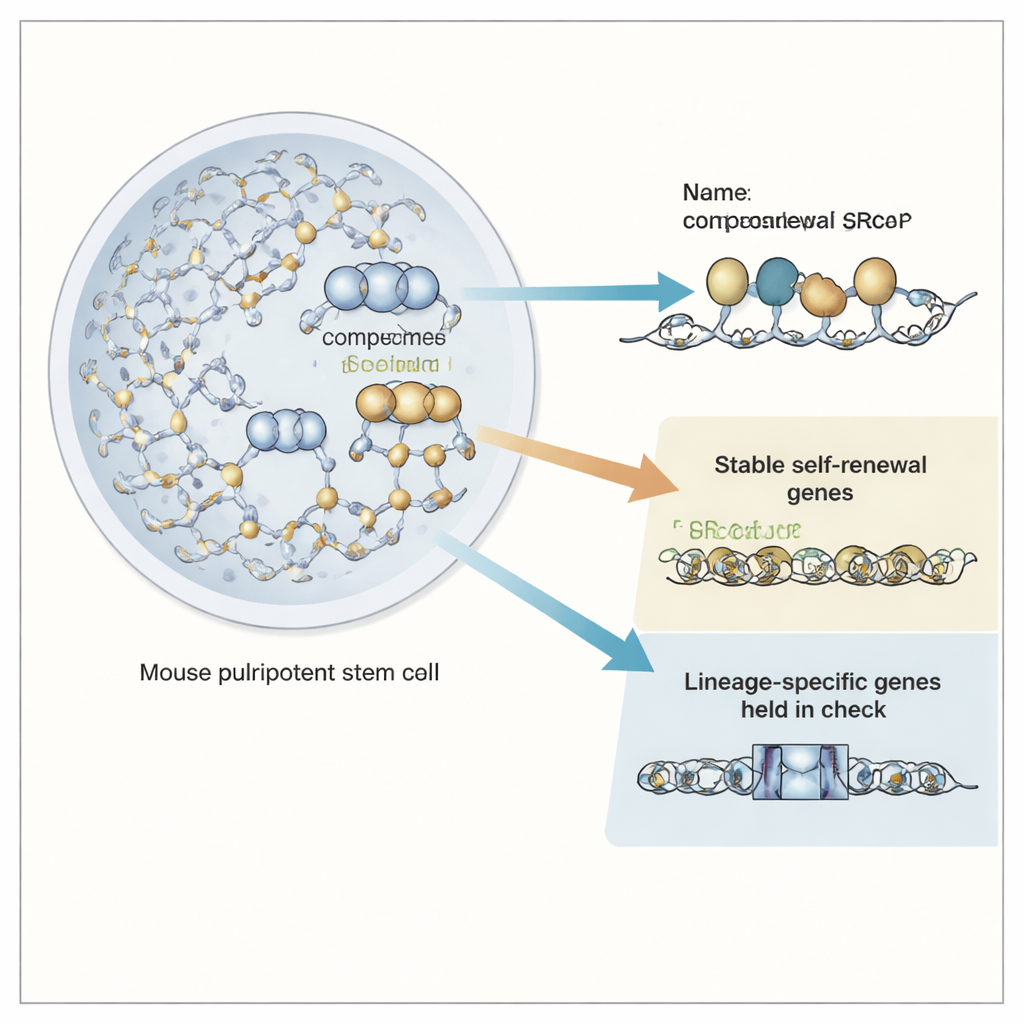
Szpule DNA, które kontrolują aktywność genów
W każdej komórce DNA jest nawinięte na białkowe szpule zwane nukleosomami, tworząc chromatynę. Większość nukleosomów wykorzystuje standardowe białka, ale niektóre zawierają wariant zwany H2A.Z, który jest szczególnie częsty w pobliżu przełączników genowych, takich jak promotory i enhancery. W mysich komórkach pluripotencjalnych wiadomo, że H2A.Z odgrywa ważną rolę zarówno w samoodnawianiu, jak i zdolności do różnicowania. Kompleks SRCAP to duża maszyna, która wymienia standardowe składniki nukleosomów na H2A.Z, ale do tej pory nie było jasne, czy jego wpływ na geny wynika wyłącznie z osadzania H2A.Z, czy też SRCAP sam ma dodatkowe, bardziej bezpośrednie role.
Szybki przełącznik między standardowymi a wariantowymi szpulami
Aby zobaczyć, co SRCAP robi w czasie rzeczywistym, badacze zaprojektowali komórki macierzyste tak, by SRCAP można było zniszczyć w ciągu kilku godzin po dodaniu małej cząsteczki. Po usunięciu SRCAP H2A.Z szybko zniknął z niemal wszystkich swoich zwykłych miejsc i został zastąpiony przez standardowy histon, zwłaszcza w pobliżu aktywnych startów genów i enhancerów. Ta szybka wymiana zachodziła w całym cyklu komórkowym i była jeszcze szybsza podczas podziału komórki, co sugeruje, że SRCAP nieustannie ponownie ładuje H2A.Z, gdy inne procesy go wypychają. Co ciekawe, ogólne upakowanie nukleosomów i ich podstawowe właściwości fizyczne zmieniły się znacznie mniej, niż oczekiwano, wskazując, że kluczowe efekty SRCAP i H2A.Z nie polegają jedynie na poluzowaniu lub zacieśnieniu DNA, lecz na wpływaniu na to, kto może się tam wiązać.
Powstrzymywanie głównych regulatorów losu komórek
Gdy SRCAP został zdegradowany, aktywność setek genów zmieniła się w ciągu kilku godzin. Wiele genów, które zwykle znajduje się w stanie „gotowości” — często ważnych regulatorów przyszłych losów komórek — stało się bardziej aktywnych, podczas gdy wiele powszechnie potrzebnych genów podstawowych zmniejszyło aktywność. Szczegółowe mapowanie kontaktów białko–DNA pokazało, że duża liczba czynników transkrypcyjnych, w szczególności tzw. czynników pionierskich, które potrafią wiązać się z zamkniętą chromatyną, nagle uzyskała dostęp do swoich miejsc docelowych po usunięciu SRCAP. Poziomy tych czynników w komórce nie uległy zmianie, co wskazuje na SRCAP jako fizyczną barierę, która zwykle trzyma je z dala od pewnych odcinków DNA.
Oddzielenie ról SRCAP i H2A.Z
Aby rozdzielić funkcje SRCAP i H2A.Z, zespół zbudował mutantyczną wersję SRCAP, która może nadal osiadać na nukleosomach, ale nie jest już w stanie wstawiać H2A.Z. Porównanie komórek wyrażających normalną lub mutantyczną wersję, z obecnym lub bez degradacji oryginalnego SRCAP, ujawniło dwie odrębne warstwy kontroli. Sam H2A.Z działał głównie jak hamulec, pomagając utrzymać wiele genów specyficznych dla linii w stanie uciszenia. SRCAP, przeciwnie, odgrywał rolę pozytywną we wspieraniu wielu genów „housekeepingowych” oraz oddzielną, niezależną od H2A.Z rolę w blokowaniu wiązania czynników transkrypcyjnych na licznych enhancerach. Śledzenie pojedynczych cząsteczek kluczowego regulatora komórek macierzystych, NANOG, potwierdziło, że po usunięciu SRCAP cząsteczki NANOG znajdują i wiążą swoje cele znacznie częściej, co jest zgodne z obrazem SRCAP jako bariery fizycznie im przeszkadzającej.
Jak molekularna tarcza chroni tożsamość komórek macierzystych
Razem te odkrycia przedstawiają SRCAP jako coś więcej niż tylko instalatora specjalnej części chromatyny. SRCAP działa jako dynamiczna tarcza wzdłuż DNA, fizycznie ograniczając, kiedy i gdzie potężne czynniki transkrypcyjne mogą się pojawić, podczas gdy H2A.Z pomaga utrzymać geny różnicowania pod kontrolą. Koordynując te odrębne role, para SRCAP–H2A.Z pozwala komórkom pluripotentnym odporne utrzymać swoją podstawową tożsamość, a jednocześnie być gotowymi do uruchomienia nowych programów genowych, gdy nadejdą właściwe sygnały.
Cytowanie: Tollenaere, A., Ugur, E., Dalla Longa, S. et al. Mechanisms of gene regulation by SRCAP and H2A.Z. Nat Commun 17, 3560 (2026). https://doi.org/10.1038/s41467-026-70087-x
Słowa kluczowe: remodelowanie chromatyny, tożsamość komórek macierzystych, wariant histonowy H2A.Z, czynniki transkrypcyjne, regulacja genów