Clear Sky Science · pt
Ampliando o panorama genético das doenças metabólicas hereditárias usando sequenciamento de leitura longa e perfilamento transcriptômico
Por que alterações ocultas no DNA importam para doenças raras
Para muitas famílias que vivem com doenças metabólicas hereditárias raras, os testes genéticos mais avançados disponíveis hoje ainda não conseguem fornecer uma resposta clara. Este estudo investiga por que tantos casos permanecem um mistério e mostra como formas mais recentes de ler o DNA e medir a atividade gênica podem revelar falhas ocultas que os testes tradicionais deixam passar. Ao examinar detalhadamente sete pacientes enigmáticos, os pesquisadores revelam tipos incomuns de alterações genéticas e oferecem um roteiro para melhorar o diagnóstico e o cuidado.
Quando os testes genéticos padrão não são suficientes
As doenças metabólicas hereditárias formam um grande grupo de condições nas quais o corpo não processa corretamente certas gorduras, açúcares ou outras moléculas. Os médicos frequentemente as detectam primeiro por exames anormais de sangue ou urina em recém-nascidos ou crianças pequenas. O próximo passo costuma ser analisar as partes codificadoras de proteína do genoma usando exoma ou sequenciamento de genoma de leitura curta. Ainda assim, mesmo com essas ferramentas poderosas, muitos pacientes recebem apenas uma resposta parcial, como uma cópia defeituosa de um gene em uma doença que normalmente exigiria duas, ou nenhuma alteração convincente. Os sete indivíduos deste estudo se enquadravam nessa “lacuna diagnóstica”: testes clínicos e bioquímicos apontavam fortemente para uma doença metabólica, mas os exames genéticos deixavam questões-chave sem resposta.
Lendo o DNA em pedaços maiores e ouvindo o RNA
Para enfrentar esses casos difíceis, a equipe combinou duas abordagens modernas. Primeiro, usaram sequenciamento de leitura longa, uma tecnologia que lê o DNA em fragmentos muito maiores do que os testes padrão, e a direcionaram para genes específicos já suspeitos a partir dos resultados metabólicos. Leitura longa facilita a detecção de alterações estruturais, como segmentos duplicados, inserções profundas e rearranjos complexos. Em segundo lugar, analisaram o RNA, as moléculas produzidas quando genes são ativados, para ver como essas alterações no DNA afetam de fato as mensagens gênicas — se exons são omitidos, pedaços extras são emendados ou os níveis de expressão caem. Juntas, essas ferramentas ofereceram tanto um mapa estrutural quanto uma leitura funcional do panorama genético de cada paciente.
Culpados genéticos incomuns vêm à tona
Essa estratégia combinada compensou. Em seis dos sete pacientes, os pesquisadores descobriram variantes causadoras da doença “faltantes” que testes anteriores não haviam detectado. Eles identificaram um exon duplicado que provavelmente interrompe um gene mitocondrial-chave, e duas alterações intrônicas profundas que criam segmentos extras nas mensagens gênicas e acionam sinais de término prematuro. De forma notável, três pacientes apresentaram novas inserções de fragmentos móveis de DNA chamados elementos transponíveis. Duas dessas inserções ocorreram dentro de genes metabólicos, levando à omissão de exons e a mensagens instáveis. A terceira situava-se logo além de um gene transportador de glicose, em uma região que ajuda a controlar quando e com que intensidade esse gene é ativado. Em vários casos, a equipe usou ensaios laboratoriais sob medida — como minigene e sistemas repórteres — para demonstrar que essas variantes incomuns prejudicavam a função gênica normal.
Como o dobramento 3D do genoma pode causar doença
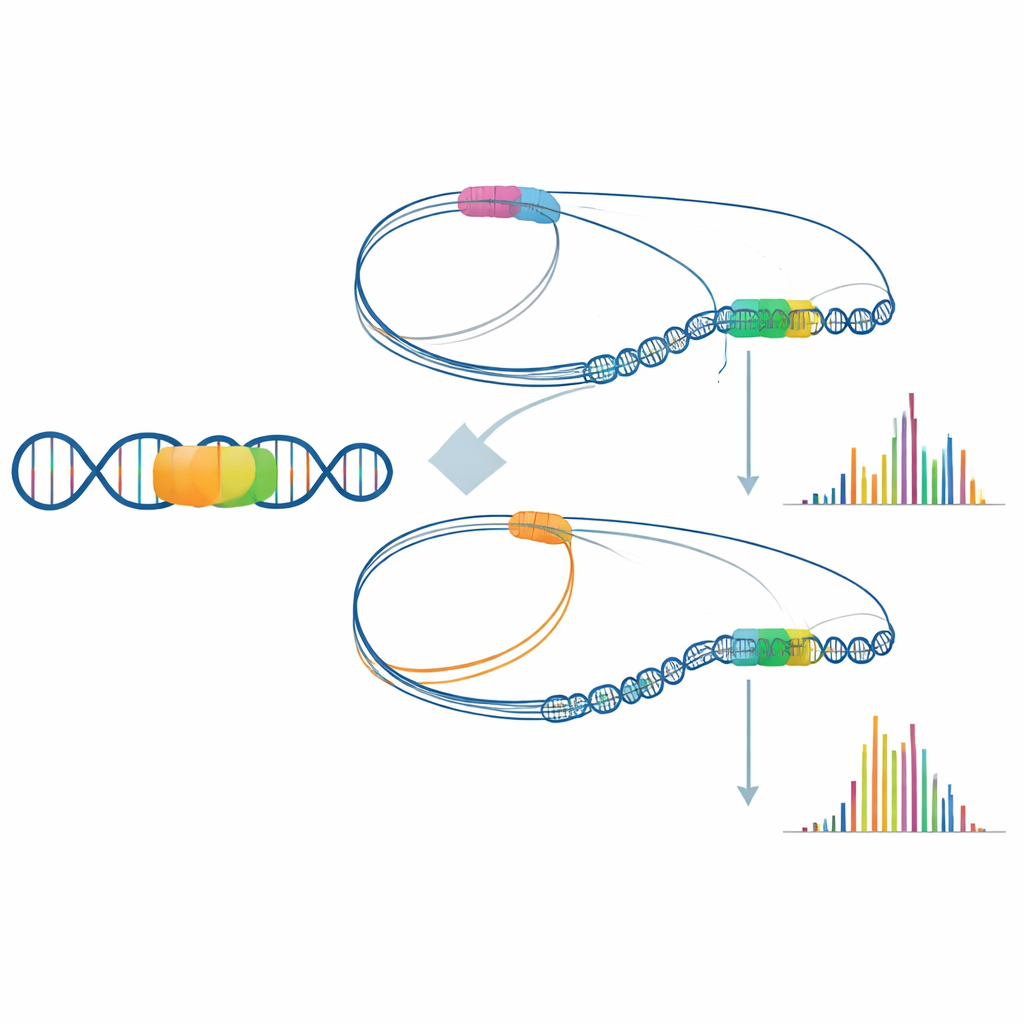
Um caso especialmente elucidativo envolveu o gene que transporta glicose para as células cerebrais. Embora a sequência codificadora do gene estivesse intacta, as células do paciente produziram muito menos RNA desse gene. O sequenciamento de leitura longa revelou uma grande inserção de DNA móvel localizada a vários milhares de bases do gene. Ao mapear o dobramento tridimensional da cromatina ao redor, os pesquisadores mostraram que, em células saudáveis, a região de controle do gene costuma fazer contato com um aglomerado upstream de elementos potenciadores, formando um “núcleo ativo” que sustenta alta expressão. No paciente, esses contatos com potenciadores foram parcialmente redirecionados para o novo local de inserção, enfraquecendo a ligação entre potenciador e gene. Essa reconfiguração sutil da arquitetura do genoma provavelmente contribui para a escassez de energia no cérebro do paciente.
O que isso significa para pacientes e triagem futura
No geral, o estudo demonstra que concentrar o sequenciamento de leitura longa em genes suspeitos, combinado com análises cuidadosas de RNA e ensaios funcionais, pode revelar uma gama mais ampla de alterações causadoras de doenças do que os métodos padrão isolados. Destaca que inserções de DNA móvel, variantes intrônicas profundas e perturbações do dobramento 3D do genoma são contribuidores subestimados para as doenças metabólicas hereditárias. À medida que o teste genômico se torna mais comum, especialmente em recém-nascidos, incorporar essas ferramentas avançadas e construir conjuntos de referência melhores pode ajudar mais famílias a sair da incerteza para um diagnóstico preciso e, em última instância, opções de tratamento mais direcionadas.
Citação: Soriano-Sexto, A., Sánchez-Lijarcio, O., Beccari, L. et al. Expanding the genetic landscape of inherited metabolic diseases using long-read sequencing and transcriptomic profiling. Eur J Hum Genet 34, 543–553 (2026). https://doi.org/10.1038/s41431-025-01995-7
Palavras-chave: doenças metabólicas hereditárias, sequenciamento de leitura longa, elementos transponíveis, organização 3D do genoma, diagnóstico de doenças raras