Clear Sky Science · de
Die genetische Landschaft erblich bedingter Stoffwechselkrankheiten mit Langzeitsequenzierung und Transkriptomprofilen erweitern
Warum versteckte DNA‑Veränderungen bei seltenen Krankheiten wichtig sind
Für viele Familien mit seltenen erblichen Stoffwechselkrankheiten liefern selbst die heute fortschrittlichsten Gentests häufig keine klare Antwort. Diese Studie untersucht, warum so viele Fälle ein Rätsel bleiben, und zeigt, wie neuere Methoden zum Lesen der DNA und zur Messung der Genaktivität versteckte Fehler aufdecken können, die traditionelle Tests übersehen. Am Beispiel von sieben rätselhaften Patienten identifizieren die Forschenden ungewöhnliche Arten genetischer Veränderungen und liefern einen Fahrplan, um Diagnose und Betreuung zu verbessern.
Wenn Standard‑Gentests nicht ausreichen
Erblich bedingte Stoffwechselkrankheiten bilden eine große Gruppe von Erkrankungen, bei denen der Körper bestimmte Fette, Zucker oder andere Moleküle nicht korrekt verarbeiten kann. Ärztinnen und Ärzte entdecken sie oft zuerst durch auffällige Blut‑ oder Urinbefunde bei Neugeborenen oder Kleinkindern. Der nächste Schritt ist meist die Analyse der protein‑kodierenden Regionen des Genoms mittels Exom‑ oder Kurzlese‑Genomsequenzierung. Trotzdem erhalten viele Patientinnen und Patienten trotz dieser mächtigen Werkzeuge nur eine Teilantwort — etwa eine defekte Genkopie in einer Erkrankung, die eigentlich zwei fehlerhafte Kopien erfordert, oder gar kein eindeutiger Befund. Die sieben in dieser Studie untersuchten Personen fielen in diese „diagnostische Lücke“: Klinische und biochemische Befunde deuteten stark auf eine Stoffwechselerkrankung hin, doch die genetische Untersuchung ließ wesentliche Fragen offen.
DNA in längeren Stücken lesen und RNA „zuhören“
Um diese schwierigen Fälle anzugehen, kombinierte das Team zwei moderne Ansätze. Erstens setzten sie Langzeitsequenzierung ein, eine Technologie, die DNA in deutlich größeren Stücken liest als Standardtests, und richteten diese auf die spezifischen Gene aus, die anhand der Stoffwechselbefunde bereits verdächtigt wurden. Lange Reads erleichtern das Erkennen struktureller Veränderungen wie Duplikationen, tiefe Insertionsereignisse und komplexe Umlagerungen. Zweitens analysierten sie RNA — die Moleküle, die entstehen, wenn Gene aktiviert werden — um zu sehen, wie diese DNA‑Veränderungen die Genbotschaften tatsächlich beeinflussen: ob Exons übersprungen werden, zusätzliche Stücke eingefügt werden oder die Expressionsniveaus sinken. Gemeinsam lieferten diese Werkzeuge sowohl eine strukturelle Karte als auch eine funktionelle Auswertung der genetischen Landschaft jedes Patienten.
Ungewöhnliche genetische Ursachen treten zutage
Diese kombinierte Strategie zahlte sich aus. Bei sechs der sieben Patienten entdeckten die Forschenden „fehlende“ krankheitsverursachende Varianten, die frühere Tests übersehen hatten. Sie fanden ein dupliziertes Exon, das wahrscheinlich ein wichtiges mitochondriales Gen stört, und zwei tiefe intronische Veränderungen, die zusätzliche Segmente in Genbotschaften erzeugen und frühe Stopp‑Signale auslösen. Auffällig war, dass drei Patientinnen und Patienten neuartige Insertionsereignisse mobilier DNA‑Fragmente trugen, sogenannte transponierbare Elemente. Zwei davon landeten innerhalb von Stoffwechselgenen selbst und führten zu Exon‑Aussparungen und instabilen Transkripten. Das dritte lag knapp außerhalb eines Glukosetransportergenus in einer Region, die die Steuerung von Zeitpunkt und Stärke der Genexpression beeinflusst. In mehreren Fällen wendete das Team gezielte Laborassays — etwa Mini‑Genkonstrukte und Reportersysteme — an, um zu belegen, dass diese ungewöhnlichen Varianten die normale Genfunktion schädigen.
Wie 3D‑Genom‑Faltung Krankheit auslösen kann
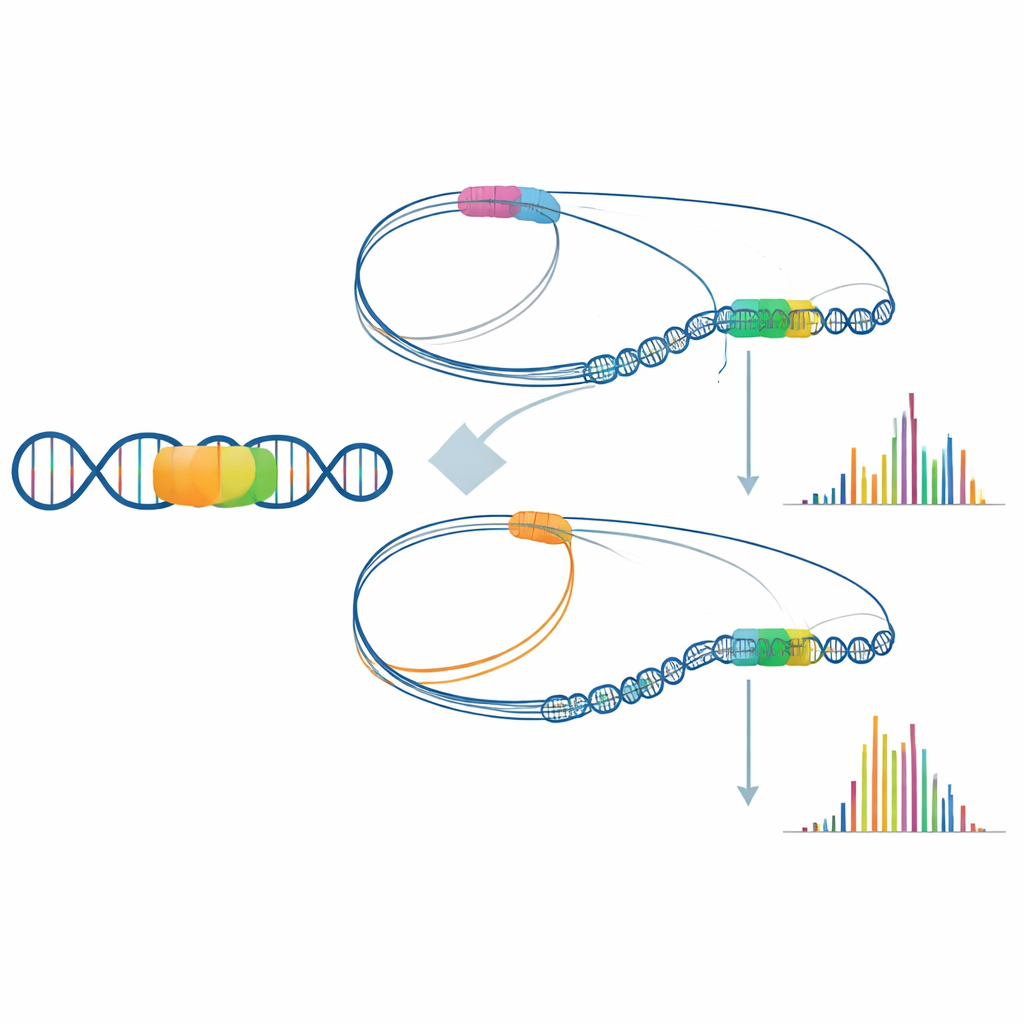
Ein besonders aufschlussreicher Fall betraf das Gen, das Glukose in Gehirnzellen transportiert. Obwohl die kodierende Sequenz des Gens intakt war, produzierten die Zellen des Patienten deutlich weniger dessen RNA. Die Langzeitsequenzierung enthüllte eine große Insertion mobilisierter DNA mehrere Tausend Basen vom Gen entfernt. Durch Kartierung der dreidimensionalen Faltung des umgebenden Chromatins zeigten die Forschenden, dass in gesunden Zellen die Kontrollregion des Gens regelmäßig eine Aufwärtskontaktstelle mit einem Cluster von Enhancern bildet — einen „aktiven Hub“, der hohe Expression unterstützt. Beim Patienten wurden diese Enhancer‑Kontaktmuster teilweise in Richtung der neuen Insertionsstelle umgelenkt, wodurch die Verbindung zwischen Enhancer und Gen geschwächt wurde. Diese subtile Umstrukturierung der Genom‑Architektur trägt wahrscheinlich zur Energiemangelsituation im Gehirn des Patienten bei.
Was das für Patienten und zukünftige Screenings bedeutet
Insgesamt zeigt die Studie, dass die gezielte Langzeitsequenzierung verdächtiger Gene in Verbindung mit sorgfältigen RNA‑ und Funktionstests ein breiteres Spektrum krankheitsverursachender Veränderungen aufdecken kann als Standardmethoden allein. Sie macht deutlich, dass Insertionsereignisse mobilisierter DNA, tiefe intronische Varianten und Störungen der 3D‑Faltung des Genoms unterschätzte Beiträge zu erblichen Stoffwechselkrankheiten leisten. Mit zunehmender Verbreitung genomischer Tests, besonders bei Neugeborenen, könnten die Integration dieser fortschrittlichen Werkzeuge und der Aufbau besserer Referenzdatensätze mehr Familien vom Unsicheren zu einer präzisen Diagnose und letztlich zu gezielteren Therapieoptionen verhelfen.
Zitation: Soriano-Sexto, A., Sánchez-Lijarcio, O., Beccari, L. et al. Expanding the genetic landscape of inherited metabolic diseases using long-read sequencing and transcriptomic profiling. Eur J Hum Genet 34, 543–553 (2026). https://doi.org/10.1038/s41431-025-01995-7
Schlüsselwörter: erblich bedingte Stoffwechselkrankheiten, Langzeitsequenzierung, transponierbare Elemente, 3D‑Genom‑Organisation, Diagnose seltener Krankheiten