Clear Sky Science · es
Ampliando el panorama genético de las enfermedades metabólicas hereditarias mediante secuenciación de lecturas largas y perfilado transcriptómico
Por qué importan los cambios de ADN ocultos en las enfermedades raras
Para muchas familias que conviven con enfermedades metabólicas hereditarias raras, las pruebas genéticas más avanzadas de la actualidad siguen sin ofrecer una respuesta clara. Este estudio explora por qué siguen sin resolverse tantos casos y muestra cómo métodos más recientes para leer el ADN y medir la actividad génica pueden descubrir fallos ocultos que las pruebas tradicionales pasan por alto. Al examinar en detalle a siete pacientes enigmáticos, los investigadores revelan tipos inusuales de alteraciones genéticas y proponen una hoja de ruta para mejorar el diagnóstico y la atención.
Cuando las pruebas genéticas estándar no son suficientes
Las enfermedades metabólicas hereditarias constituyen un grupo numeroso de condiciones en las que el organismo no procesa correctamente ciertas grasas, azúcares u otras moléculas. A menudo se detectan primero mediante pruebas anormales en sangre u orina en recién nacidos o niños pequeños. El siguiente paso suele ser analizar las regiones codificantes de proteínas del genoma mediante exoma o secuenciación genómica de lecturas cortas. Sin embargo, incluso con estas herramientas potentes, muchos pacientes solo obtienen una respuesta parcial, como una copia defectuosa de un gen en un trastorno que debería requerir dos, o ninguna variante convincente en absoluto. Los siete individuos de este estudio entraron en esa “brecha diagnóstica”: pruebas clínicas y bioquímicas apuntaban con fuerza a una enfermedad metabólica, pero las pruebas genéticas dejaron preguntas clave sin resolver.
Leer el ADN en piezas más largas y escuchar el ARN
Para abordar estos casos difíciles, el equipo combinó dos enfoques modernos. Primero, emplearon secuenciación de lecturas largas, una tecnología que lee el ADN en fragmentos mucho mayores que las pruebas estándar, y la focalizaron en los genes específicos ya sospechados por los resultados metabólicos. Las lecturas largas facilitan la detección de cambios estructurales, como duplicaciones de segmentos, inserciones profundas y reordenamientos complejos. Segundo, analizaron el ARN, las moléculas producidas cuando los genes están activos, para ver cómo afectan esas alteraciones del ADN a los mensajes génicos: si se omiten exones, si se incluyen fragmentos extra o si los niveles de expresión disminuyen. Juntos, estos instrumentos ofrecieron tanto un mapa estructural como una lectura funcional del panorama genético de cada paciente.
Salen a la luz culpables genéticos inusuales
Esta estrategia combinada dio resultados. En seis de los siete pacientes, los investigadores identificaron variantes causantes de la enfermedad «faltantes» que las pruebas anteriores no habían detectado. Encontraron un exón duplicado que probablemente interrumpe un gen mitocondrial clave, y dos variantes intrónicas profundas que generan segmentos extra en los mensajes génicos y provocan señales de terminación prematura. De forma llamativa, tres pacientes portaban nuevas inserciones de fragmentos de ADN móvil llamados elementos transponibles. Dos de estas aterrizaron dentro de genes metabólicos, provocando omisión de exones y mensajes inestables. La tercera se ubicó justo más allá de un gen transportador de glucosa, en una región que ayuda a controlar cuándo y con qué intensidad se activa ese gen. En varios casos, el equipo empleó ensayos de laboratorio adaptados —como constructos génicos reducidos y sistemas reporteros— para demostrar que estas variantes inusuales dañaban la función génica normal.
Cómo el plegamiento 3D del genoma puede causar enfermedad
Un caso especialmente revelador involucró el gen que transporta glucosa hacia las células cerebrales. Aunque la secuencia codificante del gen estaba intacta, las células del paciente producían mucho menos ARN de ese gen. La secuenciación de lecturas largas descubrió una gran inserción de ADN móvil situada a varios miles de bases del gen. Al cartografiar el plegamiento tridimensional de la cromatina circundante, los investigadores mostraron que, en células sanas, la región reguladora del gen contacta regularmente un cúmulo aguas arriba de elementos potenciadores (enhancers), formando un «núcleo activo» que sostiene una fuerte expresión. En el paciente, estos contactos con los potenciadores se reorientaron parcialmente hacia la nueva zona de inserción, debilitando el vínculo entre potenciador y gen. Esta reconfiguración sutil de la arquitectura genómica probablemente contribuye a la falta de energía en el cerebro del paciente.
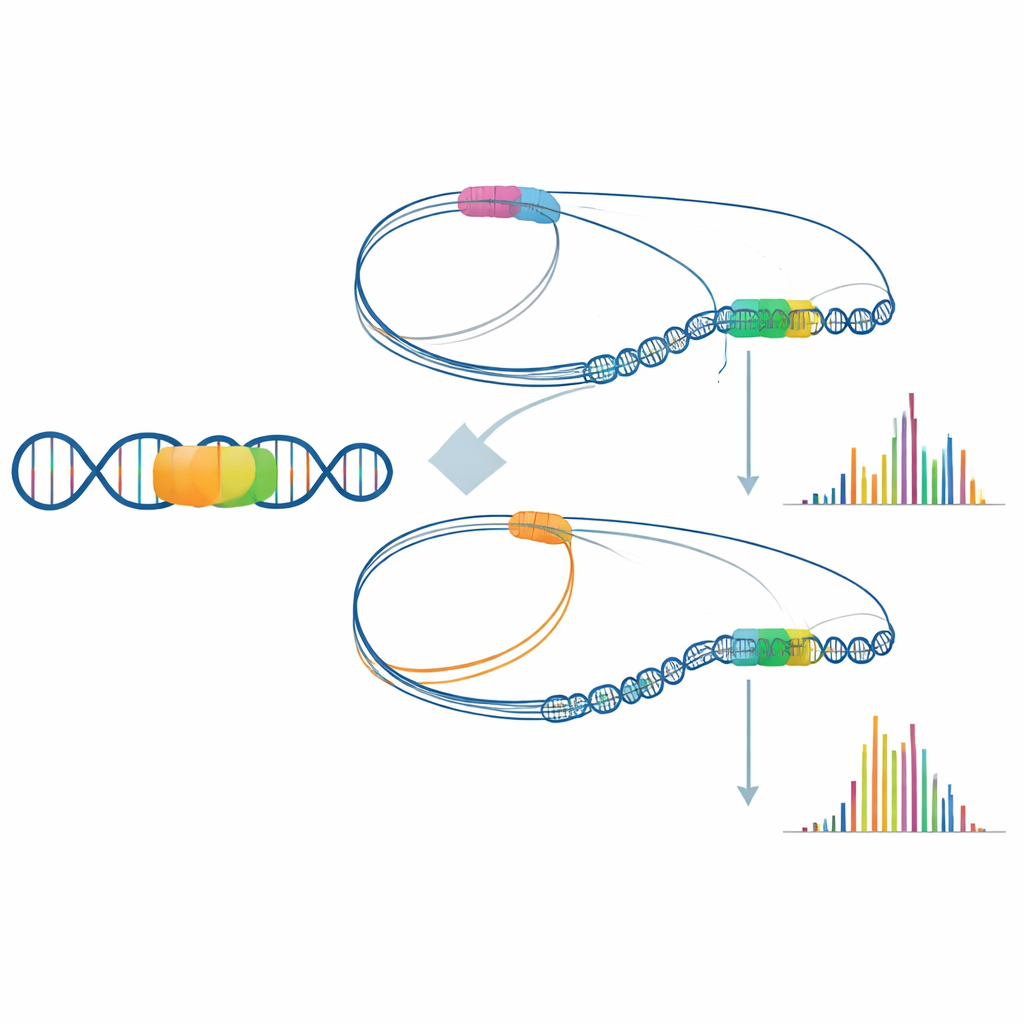
Qué implica esto para los pacientes y la detección futura
En conjunto, el estudio demuestra que centrar la secuenciación de lecturas largas en genes sospechosos, combinado con análisis cuidadosos de ARN y ensayos funcionales, puede revelar una gama más amplia de cambios causantes de enfermedad que los métodos estándar por sí solos. Subraya que las inserciones de ADN móvil, las variantes intrónicas profundas y las alteraciones del plegamiento 3D del genoma son contribuyentes infraestimados a las enfermedades metabólicas hereditarias. A medida que las pruebas genómicas se vuelvan más comunes, especialmente en recién nacidos, incorporar estas herramientas avanzadas y construir mejores conjuntos de referencia podría ayudar a más familias a pasar de la incertidumbre a un diagnóstico preciso y, en última instancia, a opciones de tratamiento más dirigidas.
Cita: Soriano-Sexto, A., Sánchez-Lijarcio, O., Beccari, L. et al. Expanding the genetic landscape of inherited metabolic diseases using long-read sequencing and transcriptomic profiling. Eur J Hum Genet 34, 543–553 (2026). https://doi.org/10.1038/s41431-025-01995-7
Palabras clave: enfermedades metabólicas hereditarias, secuenciación de lecturas largas, elementos transponibles, organización 3D del genoma, diagnóstico de enfermedades raras