Clear Sky Science · pt
Aumentação de CST1 mediada por NFATC2 impulsiona o crescimento e a metástase do colangiocarcinoma
Por que esta história sobre câncer de fígado importa
O colangiocarcinoma intra-hepático é um câncer letal que se origina nos pequenos ductos biliares dentro do fígado. Frequentemente é descoberto tardiamente, se espalha rápido e responde mal aos tratamentos padrão. Este estudo revela uma cadeia molecular oculta que ajuda essas células tumorais a evitar o envelhecimento, crescer sem controle e metastizar para órgãos distantes. Ao expor essa cadeia, o trabalho aponta para novas formas pelas quais os médicos podem frear ou interromper esse câncer de difícil tratamento.
Um olhar mais atento sobre um câncer de fígado silencioso, mas letal
O colangiocarcinoma representa apenas uma fração dos cânceres de fígado, mas causa um número desproporcional de mortes por câncer no mundo. Uma razão é que os sintomas iniciais são vagos ou ausentes, então muitos pacientes só são diagnosticados quando a doença já está avançada. Os autores começaram vasculhando grandes bancos públicos de expressão gênica, juntamente com amostras tumorais do próprio hospital, à procura de genes que consistentemente estivessem mais ativos nos tumores dos ductos biliares do que no tecido normal e que também previssem pior sobrevida dos pacientes. Entre centenas de genes alterados, um se destacou: CST1, que codifica uma pequena proteína secretada chamada cistatina SN. Pacientes cujos tumores apresentavam níveis elevados de CST1 viveram significativamente menos, marcando CST1 tanto como um sinal de alerta quanto como um potencial fator motor da doença.
Como uma única proteína aumenta crescimento e disseminação
Para testar o papel de CST1, os pesquisadores usaram linhagens celulares de câncer de ducto biliar nas quais puderam aumentar ou reduzir os níveis de CST1. Quando forçaram as células a produzir mais CST1, elas se multiplicaram mais rápido, movimentaram-se com mais facilidade através de barreiras porosas e invadiram com maior eficiência um gel que imita o tecido circundante. Quando reduziram CST1, o crescimento celular desacelerou, as células pararam em uma fase inicial do ciclo celular e a capacidade de migrar e invadir diminuiu. Em camundongos, tumores geneticamente modificados para superproduzir CST1 formaram nódulos maiores no fígado e geraram mais metástases nos pulmões, enquanto tumores com CST1 reduzido cresceram mais devagar e se espalharam menos. Juntos, esses experimentos mostram que CST1 não é apenas um marcador passivo, mas um promotor ativo do crescimento tumoral e da disseminação.
Desligando o envelhecimento celular para escapar dos freios naturais
As células normais possuem um sistema de segurança embutido chamado senescência: quando acumulam dano suficiente, entram em um estado de repouso permanente e deixam de se dividir. Isso atua como uma barreira contra o câncer. A equipe descobriu que diminuir CST1 nas células cancerosas reativou esse sistema de segurança. Células com CST1 reduzido mostraram sinais clássicos de senescência, incluindo mudanças de formato, aumento da atividade de uma enzima associada à senescência e alterações nos fatores inflamatórios que secretaram. Surpreendentemente, embora CST1 também alterasse o manejo de certas pequenas moléculas usadas na construção do DNA, tentativas de restaurar o crescimento fornecendo blocos de construção extras falharam. Isso sugere que o poder principal de CST1 não está em alimentar a síntese de DNA, mas em ajudar as células tumorais a contornar o programa de senescência que as manteria sob controle.
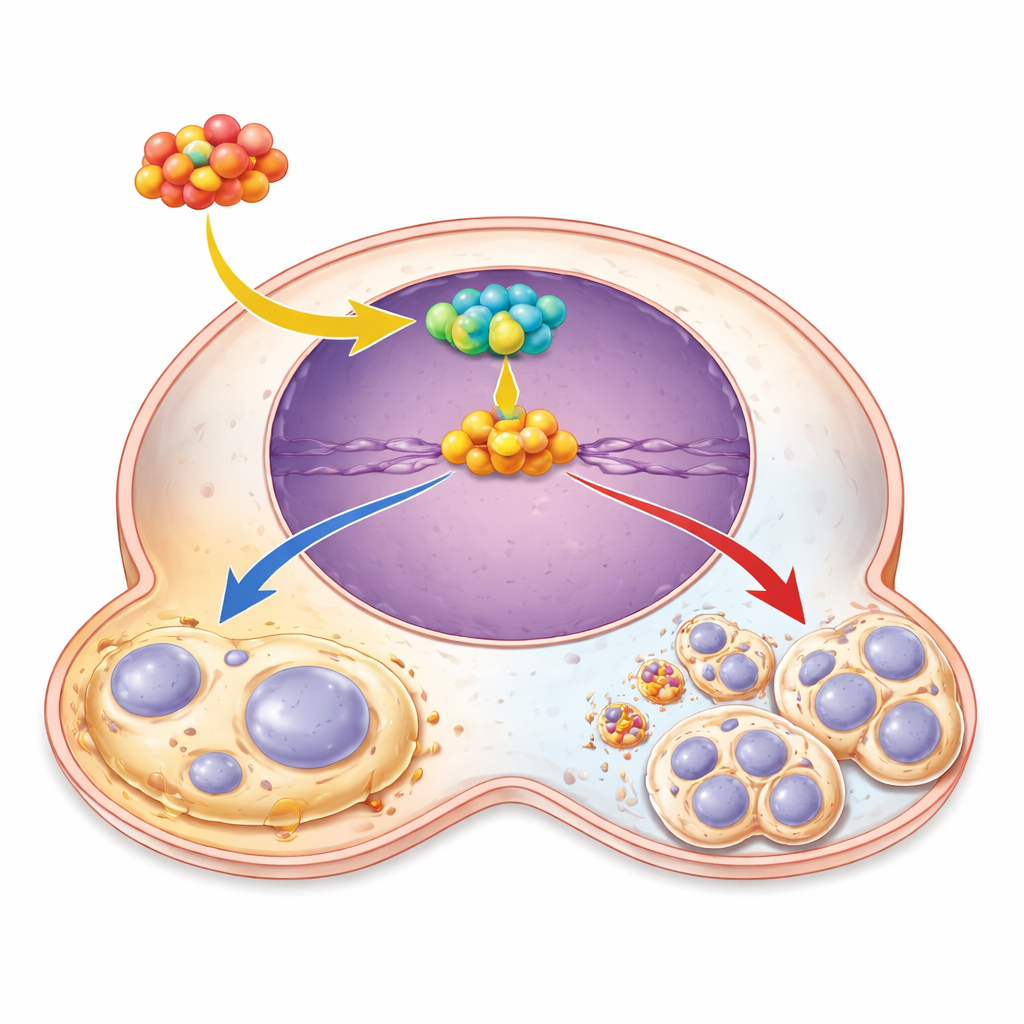
Um circuito oncogênico: de NFATC2 a CST1 a SOX4
Investigando mais a fundo, os pesquisadores montaram um revezamento molecular em três etapas dentro das células cancerosas. No topo está NFATC2, um fator de transcrição que se liga ao DNA e ativa genes específicos. Eles demonstraram que NFATC2 se ancora diretamente na região de controle do gene CST1 e aumenta sua atividade. Quando os níveis de NFATC2 eram altos, CST1 aumentava; quando NFATC2 era silenciado, os níveis de CST1 caíam e os comportamentos promotores de tumor enfraqueciam. A jusante de CST1, identificaram outro ator-chave, o fator de transcrição SOX4, que já foi associado à inibição da senescência em outros cânceres. CST1 elevou os níveis de SOX4, e quando CST1 foi reduzido, a adição de SOX4 em excesso foi suficiente para restaurar o crescimento celular e reduzir os sinais de senescência. Isso posiciona SOX4 como o executor principal dos efeitos anti-envelhecimento e pró-crescimento de CST1.
O que isso significa para tratamentos futuros
Ao mapear esse revezamento NFATC2–CST1–SOX4, o estudo revela como as células do câncer dos ductos biliares desativam seus freios internos de envelhecimento, permitindo crescimento e disseminação desenfreados. Para um leigo, a mensagem é que esses tumores sequestram uma pequena rede de proteínas para manter as células jovens e em divisão contínua. Interromper essa cadeia em qualquer ponto — bloquear o controle de NFATC2 sobre CST1, reduzir o próprio CST1 ou cortar SOX4 — poderia restaurar a tendência natural da célula de desacelerar e parar. Embora sejam necessários mais trabalhos antes que essas descobertas se traduzam em novos fármacos, CST1 em particular surge como um alvo promissor para terapias e como um marcador que pode ajudar a identificar pacientes de maior risco.
Citação: Zhao, W., Zhao, J., Li, K. et al. NFATC2-mediated CST1 upregulation drives cholangiocarcinoma growth and metastasis. Cell Death Discov. 12, 187 (2026). https://doi.org/10.1038/s41420-026-03036-8
Palavras-chave: colangiocarcinoma, CST1, senescência celular, metástase do câncer, via NFATC2 SOX4