Clear Sky Science · fr
La surexpression de CST1 médiée par NFATC2 favorise la croissance et les métastases du cholangiocarcinome
Pourquoi cette histoire de cancer du foie compte
Le cholangiocarcinome intra‑hépatique est un cancer mortel qui prend naissance dans les petits canaux biliaires du foie. Il est souvent découvert tard, se propage rapidement et répond mal aux traitements standards. Cette étude met au jour une chaîne moléculaire dissimulée qui aide ces cellules tumorales à échapper au vieillissement, à croître sans frein et à se disséminer vers des organes distants. En révélant cette chaîne, le travail ouvre la voie à de nouvelles stratégies pour ralentir ou stopper ce cancer difficile à traiter.
Un regard approfondi sur un cancer du foie discret mais mortel
Le cholangiocarcinome représente seulement une fraction des cancers du foie, mais il est responsable d’un nombre disproportionné de décès par cancer dans le monde. Une des raisons est que les symptômes initiaux sont vagues ou absents, de sorte que de nombreux patients sont diagnostiqués une fois la maladie avancée. Les auteurs ont commencé par analyser de larges bases de données publiques d’expression génique, ainsi que des échantillons tumoraux de leur propre hôpital, pour chercher des gènes systématiquement plus actifs dans les tumeurs des canaux biliaires que dans les tissus normaux et qui prédisent aussi une mauvaise survie. Parmi des centaines de gènes altérés, un s’est détaché : CST1, qui code pour une petite protéine sécrétée appelée cystatine SN. Les patients dont les tumeurs présentaient des niveaux élevés de CST1 avaient une survie nettement plus courte, faisant de CST1 à la fois un signe d’alerte et un possible moteur de la maladie.
Comment une seule protéine stimule croissance et dissémination
Pour tester le rôle de CST1, les chercheurs ont utilisé des lignées cellulaires de cancer des canaux biliaires dans lesquelles ils pouvaient augmenter ou diminuer l’expression de CST1. Lorsqu’ils ont forcé les cellules à produire davantage de CST1, celles‑ci se multipliaient plus vite, traversaient plus facilement des barrières poreuses et envahissaient plus aisément un gel mimant le tissu environnant. En réduisant CST1, la croissance cellulaire ralentissait, les cellules étaient bloquées en phase précoce du cycle cellulaire et leur capacité de migration et d’invasion chutait. Chez la souris, les tumeurs génétiquement modifiées pour surproduire CST1 formaient des nodules hépatiques plus volumineux et semaient davantage de métastases pulmonaires, tandis que les tumeurs avec CST1 réduit croissaient plus lentement et se propageaient moins. Ensemble, ces expériences montrent que CST1 n’est pas seulement un marqueur accessoire, mais un promoteur actif de la croissance tumorale et de la dissémination.
Désactiver le vieillissement cellulaire pour échapper aux freins naturels
Les cellules normales possèdent un système de sécurité intrinsèque appelé sénescence : lorsqu’elles accumulent suffisamment de dommages, elles entrent dans un état de repos permanent et cessent de se diviser. Cela constitue une barrière contre le cancer. L’équipe a découvert que diminuer CST1 dans les cellules cancéreuses réactivait ce système de sécurité. Les cellules avec CST1 réduit présentaient des signes classiques de sénescence, notamment des modifications de forme, une activité accrue d’une enzyme liée à la sénescence et des modifications des facteurs inflammatoires qu’elles sécrétaient. De manière surprenante, bien que CST1 modifie aussi la façon dont les cellules gèrent certains petits précurseurs de l’ADN, les tentatives pour restaurer la croissance en apportant des précurseurs supplémentaires ont échoué. Cela suggère que la principale capacité de CST1 ne réside pas dans l’alimentation de la synthèse d’ADN, mais dans son aide aux cellules tumorales pour contourner le programme de sénescence qui, autrement, les maintiendrait sous contrôle.
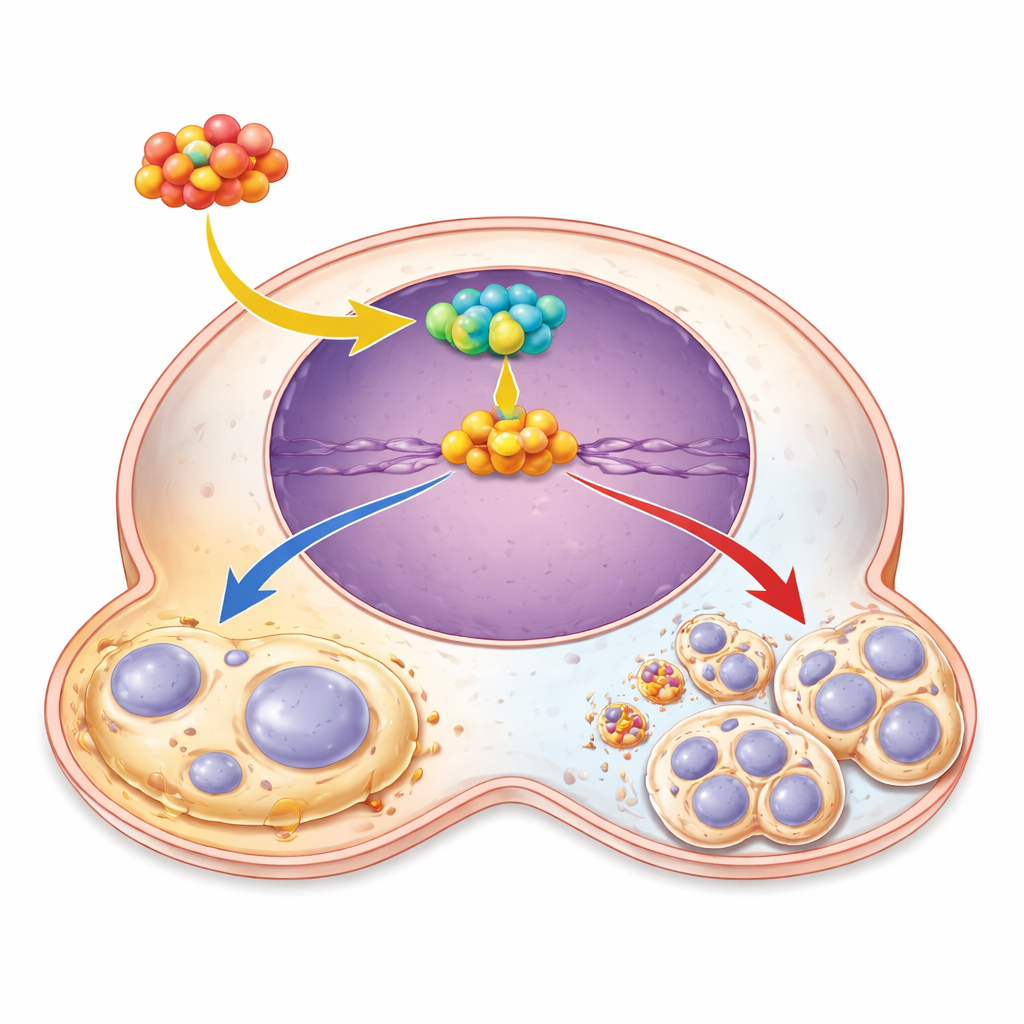
Un relais oncogénique : de NFATC2 à CST1 puis à SOX4
En creusant plus loin, les chercheurs ont reconstitué un relais moléculaire en trois étapes à l’intérieur des cellules tumorales. Au sommet se trouve NFATC2, un facteur de transcription qui se lie à l’ADN et active des gènes spécifiques. Ils ont montré que NFATC2 se fixe directement sur la région régulatrice du gène CST1 et en augmente l’activité. Lorsque les niveaux de NFATC2 étaient élevés, CST1 augmentait ; lorsqu’on silencait NFATC2, CST1 chutait et les comportements promoteurs de tumeur s’affaiblissaient. En aval de CST1, ils ont identifié un autre acteur clé, le facteur de transcription SOX4, déjà associé à la suppression de la sénescence dans d’autres cancers. CST1 augmentait les niveaux de SOX4, et lorsque CST1 était inhibé, l’ajout de SOX4 suffisait à restaurer la croissance cellulaire et à réduire les signaux de sénescence. Cela place SOX4 comme l’exécuteur principal des effets anti‑vieillissement et pro‑croissance de CST1.
Ce que cela signifie pour les traitements futurs
En cartographiant ce relais NFATC2–CST1–SOX4, l’étude révèle comment les cellules de cancer des canaux biliaires désactivent leurs freins internes liés au vieillissement, permettant une croissance et une dissémination incontrôlées. Pour un public non spécialiste, le message est que ces tumeurs détournent un petit réseau de protéines pour maintenir les cellules éternellement jeunes et en division. Perturber cette chaîne à n’importe quel étage — bloquer le contrôle de CST1 par NFATC2, réduire CST1 lui‑même ou couper SOX4 — pourrait restaurer la tendance naturelle des cellules à ralentir et à s’arrêter. Bien que des travaux supplémentaires soient nécessaires avant que ces connaissances se traduisent en nouveaux médicaments, CST1 apparaît en particulier comme une cible thérapeutique prometteuse et comme un marqueur susceptible d’aider à identifier les patients à risque plus élevé.
Citation: Zhao, W., Zhao, J., Li, K. et al. NFATC2-mediated CST1 upregulation drives cholangiocarcinoma growth and metastasis. Cell Death Discov. 12, 187 (2026). https://doi.org/10.1038/s41420-026-03036-8
Mots-clés: cholangiocarcinome, CST1, sénescence cellulaire, métastases cancéreuses, voie NFATC2 SOX4